脑缺血是中风的主要原因,约占所有脑血管意外的80%。脑缺血会触发急性神经炎症反应,这种反应会加剧缺血性脑损伤,并形成有害的循环。在脑缺血后,小胶质细胞迅速迁移到损伤部位,通过产生炎症细胞因子和细胞毒性物质加剧脑组织损伤。因此,抑制小胶质细胞释放促炎因子成为治疗缺血性脑血管疾病的关键策略。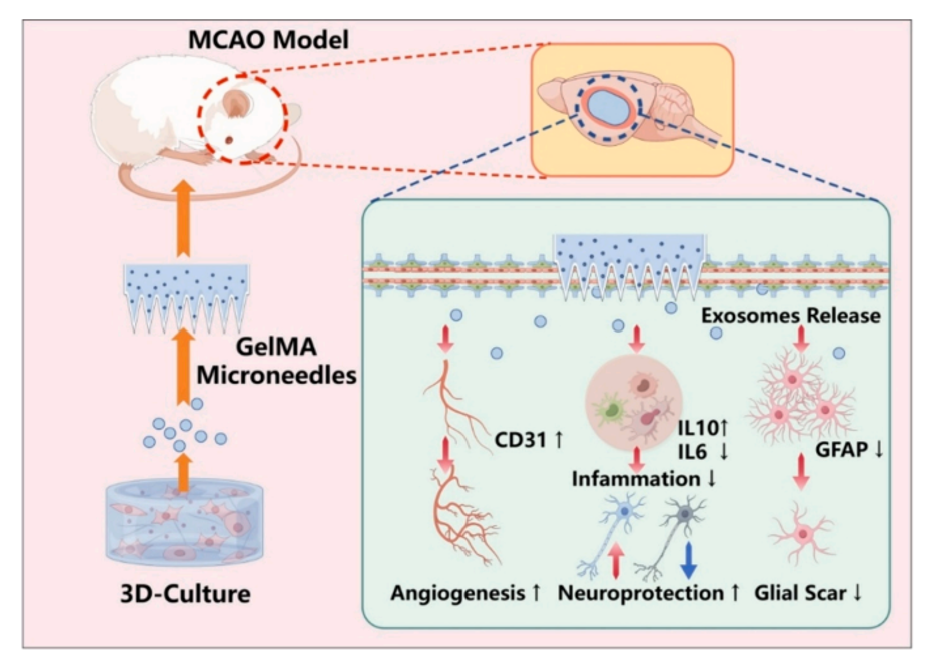
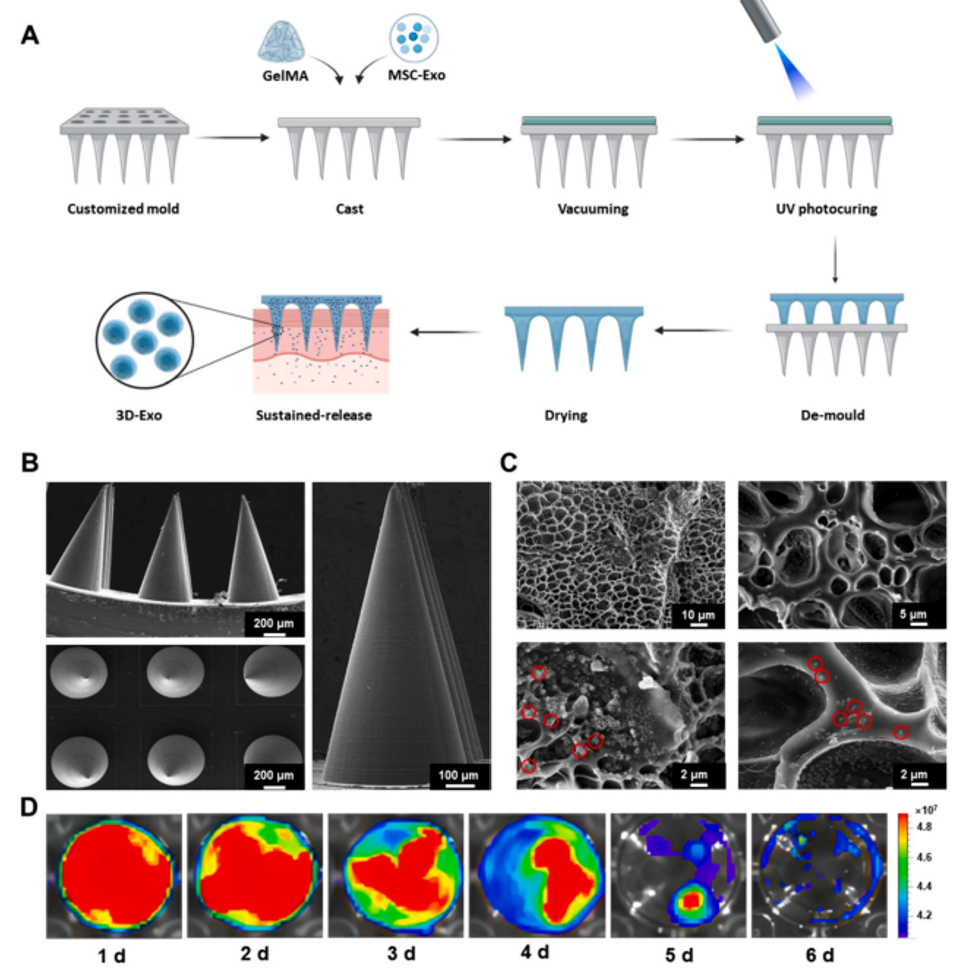
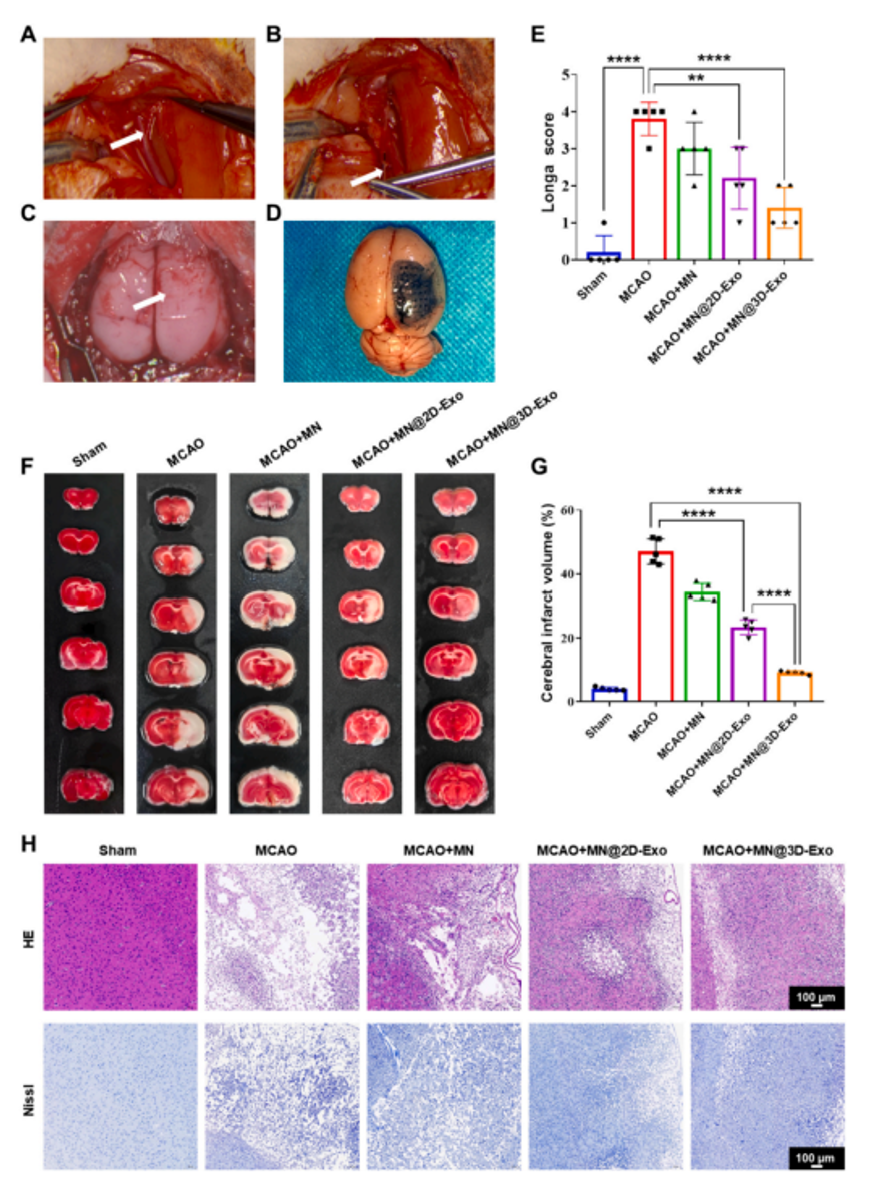
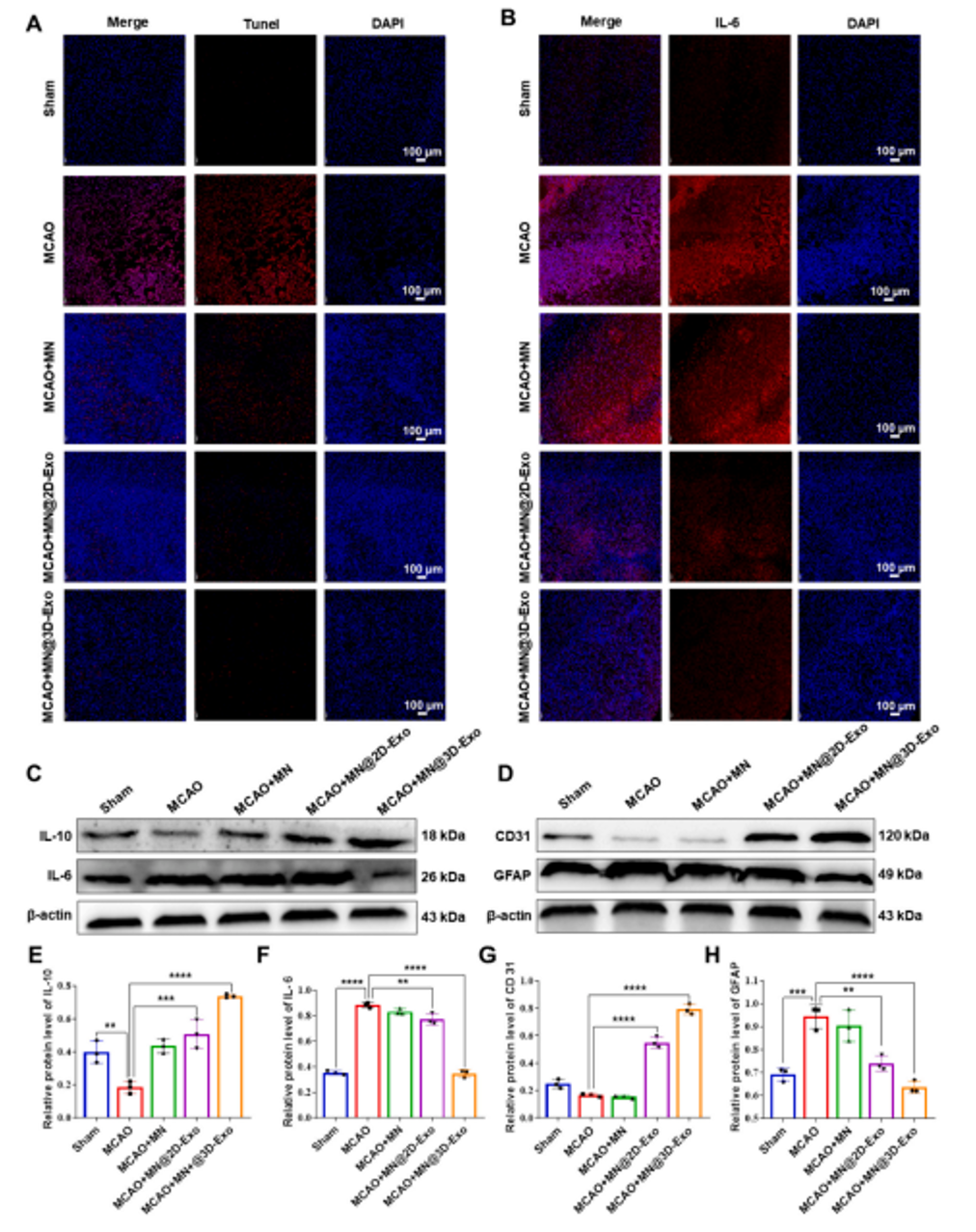
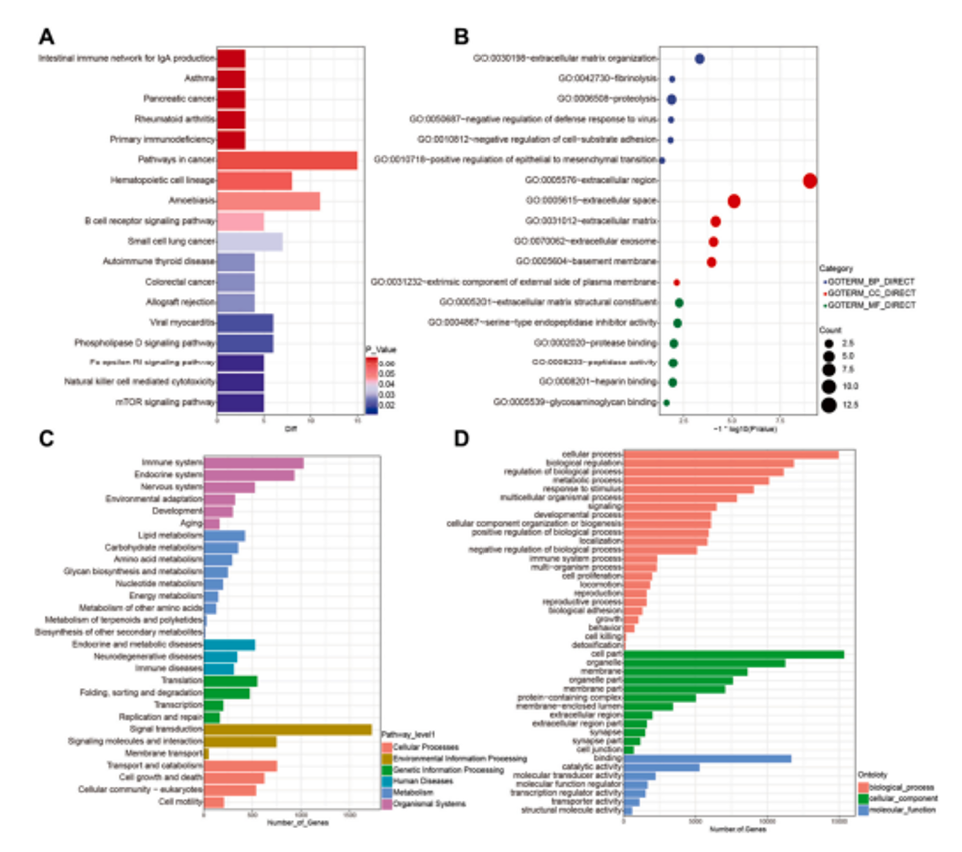
近期,天津医科大学万春晓、山东第一医科大学韩敏研究团队开发了一种结合了间充质干细胞(Mesenchymal Stem Cells, MSCs)的三维(3D)培养技术来生成外泌体(Exosomes, Exo),并利用甲基丙烯酰化明胶(Gelatin methacryloyl, GelMA)微针(microneedles)作为药物递送系统,以增强外泌体在脑损伤区域的靶向性和治疗效果。相关内容以“Gelatin methacryloyl microneedle loaded with 3D-MSC-Exosomes for theprotection of ischemia-reperfusion”为题发表在International Journal of Biological Macromolecules杂志上(2024 Jun 25;275(Pt 1):133336)。该研究使用了EFL的GelMA(EFL-GM-60)、LAP(EFL-LAP)光引发剂以及固化环(EFL-SCR-3D-24-2)多种产品。甲基丙烯酰化明胶(GelMA)为双键改性明胶,其可通过紫外及可见光在光引发剂作用下交联固化成胶。GelMA兼具天然和合成生物材料的特征,具有适于细胞生长和分化的三维结构、优异的生物相容性和细胞反应特性,其可替代人工基底膜或其他天然胶原蛋白水凝胶。此外,GelMA具备良好的温敏凝胶特性和可降解性,其机械性能可调,能够提供多种黏弹特性,已广泛应用于细胞3D培养、组织工程、生物3D打印等研究领域。图1 GelMA-微针(GelMA-MN)的制备、特征及体外释放MSC-Exo的情况为了评估GelMA微针持续长期释放MSC-Exo的能力,作者使用硅胶模具制备了装载有MSC-Exo的GelMA微针。然后,通过使用扫描电子显微镜观察到微针贴片上规则排列着GelMA微针,并且它们的表面装载了大量外泌体。此外,体外观察释放的MSC-Exo浓度变化表明其存在时间几乎持续了一周。综上所述,GelMA微针提供保护作用的外泌体的能力,确保在较长时间内维持有效浓度。图2 大脑中动脉闭塞(MCAO)模型的构建及损伤情况的评估此外,研究人员建立了大鼠大脑中动脉闭塞(MCAO)模型,并进行了脑部MRI和3D重建。实验中,通过植入装载MSC-Exo的GelMA微针(GelMA-MN@MSC-Exo),使用Longa评分评估了大鼠MCAO后的的行为变化,结果表明,与Sham组相比,MCAO组的大鼠Longa评分显著升高,显示出明显的功能障碍。而装载2D-Exo和3D-Exo的微针组大鼠的Longa评分显著降低,尤其是3D-Exo组的改善更为显著,表明MSC-Exo能显著改善大鼠的脑损伤和行为功能。通过TTC染色和组织病理学评估,3D-Exo组在减少梗死体积和改善组织形态方面表现更佳,Nissl染色也显示3D-Exo组在保护神经元结构方面更为有效。这些结果表明,3D-Exo具有更优越的神经保护效果,能显著减轻大鼠MCAO后的脑损伤。图3 评估GelMA-MN@3D-Exo对MCAO大鼠的修复作用MSC-Exo对MCAO后炎症、血管生成和瘢痕形成的影响为进一步验证MSC-Exo对大鼠MCAO后细胞凋亡、神经炎症、血管生成和胶质瘢痕的影响,研究人员采用免疫荧光和wb实验检测了大鼠脑损伤部位相关因子的表达。结果显示,与Sham组相比,MCAO组的GFAP蛋白表达显著增加,表明胶质细胞活化和瘢痕形成,而MN@3D-Exo组的GFAP表达则显著降低。TUNEL染色显示MCAO组凋亡细胞数量增加,而MN@2D-Exo和MN@3D-Exo组均能显著减少凋亡细胞数量,其中3D-Exo组的减少更为显著。IL-6染色和wb结果表明,MCAO组IL-6蛋白表达增加,而MN@3D-Exo组则能显著降低其表达,表明3D-Exo具有抗炎作用。CD31染色和wb的结果显示,与Sham组相比,MCAO组CD31蛋白表达降低,而MN@3D-Exo组则能显著增加CD31蛋白表达,表明3D-Exo能促进血管生成。此外,wb实验结果还显示,3D-Exo组中IL-10和CD31的水平显著上调,而IL-6和GFAP的水平则下调。这些结果表明,MN@3D-Exo能够在减轻神经炎症、促进脑血管生成和改善胶质瘢痕方面发挥作用,为MCAO后脑损伤的修复提供了新的治疗策略。对MSC-Exo进行蛋白质质谱测序和miRNA测序的生物信息学分析进一步对3D-Exo组中上调蛋白和miRNAs进行了功能富集分析。结果显示,在3D-Exo蛋白组中,细胞外基质组织、细胞外区域和细胞外泌体显著富集。此外,在3D-Exo miRNAs组中,诸如免疫系统、神经系统、复制与修复、免疫系统过程和细胞增殖等信号通路也显著富集。综上所述,本研究成功开发了一种基于3D培养的间充质干细胞外泌体(3D-MSC-Exo)和GelMA微针的创新治疗系统,用于治疗缺血再灌注(I/R)引起的脑损伤。通过在大鼠大脑中动脉闭塞(MCAO)模型中的实验,证明了3D-MSC-Exo在减轻神经炎症、促进血管生成、减少胶质瘢痕形成方面具有显著效果,并通过GelMA微针实现了这些外泌体的持续释放和保护。分子机制分析揭示了3D-Exo中上调的蛋白和miRNAs在细胞外基质组织、免疫和神经系统信号通路中的富集,为3D-MSC-Exo的神经保护作用提供了深入的分子层面理解,从而为临床治疗缺血性脑损伤提供了一种新的、有前景的治疗策略。Gelatin methacryloyl microneedle loaded with 3D-MSC-Exosomes for the protection of ischemia-reperfusion, Int J Biol Macromol. 2024 Jun 25;275(Pt 1):133336. doi: 10.1016/j.ijbiomac.2024.133336.文章来源:https://doi.org/10.1016/j.ijbiomac.2024.133336外泌体资讯网 NT J BIOL MACROMOL|天津医科大学万春晓、山东第一医科大学韩敏研究团队:GelMA微针实现缺血再灌注损伤的保护