骨肉瘤(Osteosarcoma, OS)是最常见的原发性恶性骨肿瘤,具有较高的肺转移倾向,是OS相关死亡和治疗失败的主要原因。OS转移患者的预后通常较差,5年总生存率约为20%。当前,OS肺转移仍缺乏新的可靠诊断标志物、治疗靶点和有效的治疗策略,阐明肺转移的潜在机制仍然是一个巨大挑战。
在“种子和土壤”转移理论提出后,肿瘤转移不仅取决于原发性肿瘤细胞自身的迁移和侵袭能力,还取决于靶器官的微环境。转移前微生境(Pre-metastatic Niches, PMN)自2005年首次提出以来,在肿瘤转移领域引起了越来越多的关注,它被认为和原发性肿瘤共同促进肿瘤转移的发生。
原发性肿瘤的细胞外囊泡(Extracellular vesicles, EVs)是细胞分泌的特殊脂质双层膜囊泡,在PMN形成中起着极其重要的作用。EVs可以用于递送活性物质(包括脂质、蛋白质、核酸和完整的细胞器等),是诊断和治疗方法的潜在循环生物标志物靶点。在与宿主细胞直接融合后,EVs传递生物信息并介导细胞间信号以重塑PMN。
近日,南京中医药大学常州附属医院徐建达团队在Biomedicine & Pharmacotherapy杂志上发表题为“Review of Pre-metastatic Niches Induced by Osteosarcoma-derived Extracellular Vesicles in Lung Metastasis: A Potential Opportunity for Diagnosis and Intervention”的综述,主要介绍了骨肉瘤源性细胞外囊泡在骨肉瘤肺转移前微环境中的调控作用机制,并系统总结了新的相关预防策略。此外,作者还从阻碍EVs诱导PMN形成的角度讨论了靶向治疗预防OS肺转移的潜在挑战。南京中医药大学常州附属医院徐建达、江苏理工学院范振敏为共同通讯作者,南京中医药大学常州附属医院夏中玉、盐城工学院许伟、江苏大学张红梅为文章第一作者。
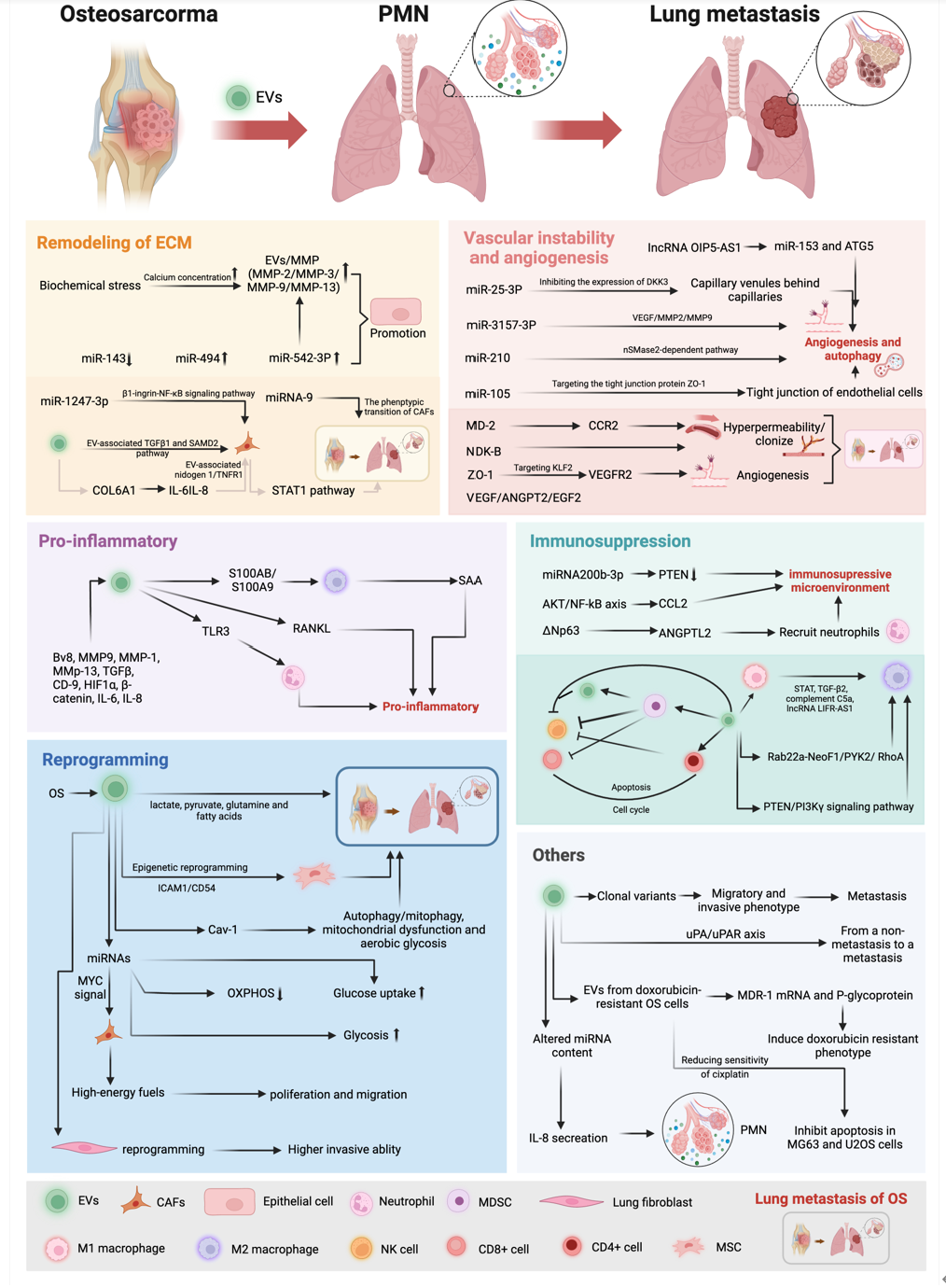
该综述系统介绍了OS源性EVs诱导肺转移PMN形成的潜在机制,具体概括为细胞外基质的重塑、血管再生、血管通透性增强、促炎反应、免疫抑制和重编程机制等。
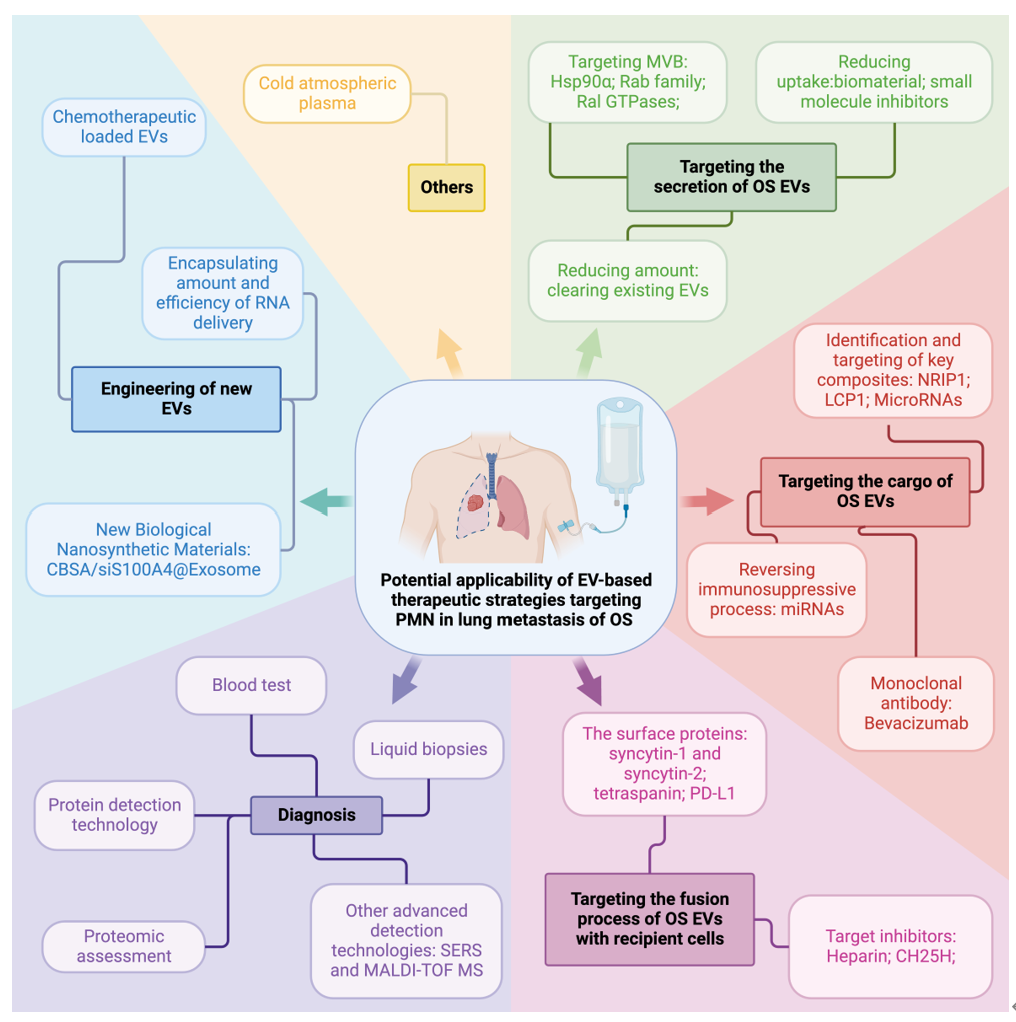
同时,该研究也总结了基于EVs的靶向PMN治疗策略在OS肺转移治疗中的潜在挑战。一系列治疗策略包括靶向EVs分泌过程、靶向EVs内含成分、靶向OS-EVs与受体细胞融合过程、诊断以及新EV的工程化设计等。以及液体活检、血液检测、蛋白质检测技术、蛋白质组学评估和其他先进的检测技术用于评估和诊断PMN的形成和远处转移。