小细胞外囊泡(sEV)正迅速成为液体活检分析的新兴范式。sEV是尺寸介于40-160纳米的脂质小泡,参与细胞间通讯、迁移、血管新生及肿瘤细胞生长等关键生理过程。越来越多证据表明,sEV蛋白表达水平与肿瘤的发生和发展密切相关,因此揭示其蛋白谱将有助于无创性早期诊断和疾病进程监测。
然而,要深入探析sEV蛋白与肿瘤相关的表达特征,高效分离和灵敏检测sEV至关重要。传统分离方法耗时、操作繁琐、效率较低,且样品消耗量大,严重限制了应用。现有的分析方法大多还需对样品进行囊泡富集,进一步增加了过程复杂性。因此,迫切需要开发一种简单、高效、灵敏的新型sEV分离分析技术。
2024年8月18日,厦门大学朱志教授/苏蕊主任医师团队在Analytical Chemistry以封面文章在线发表题为“Fast Isolation and Sensitive Multicolor Visual Detection of Small Extracellular Vesicles by Multifunctional Polydopamine Nanospheres”的研究论文(Anal. Chem.,2024,https://doi.org/10.1021/acs.analchem.4c02062),报道了该团队利用纳米材料和基于膜过滤的方法,设计了一种在复杂的生物样本中使用适配体功能化聚多巴胺纳米球快速分离和高灵敏度多色可视化检测sEV的策略(SIMPLE)。第一作者张桂华,通讯作者朱志/苏蕊。
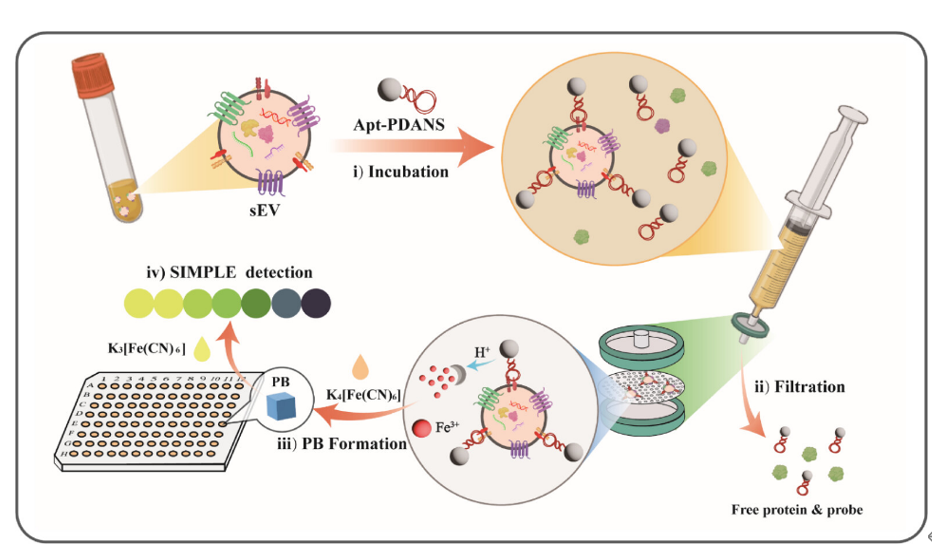
在这项研究中,作者首先将sEV与功能化适配体聚多巴胺纳米球(Apt-PDANS)共同培养,利用刚性纳米粒子实现sEV的快速膜过滤分离。尺寸较大的Apt-PDANS-sEV复合物被保留在滤膜上,而较小的游离蛋白质和游离Apt-PDANS则被过滤去除。随后,滤膜被转移至孔板中,在酸性条件下,滤膜上的Apt-PDANS-sEV释放出大量Fe³⁺,并与K₄[Fe(CN)₆]反应形成普鲁士蓝(PB)。生成的普鲁士蓝的颜色深浅依赖于sEVs所结合的Apt-PDANS的数量。此外,为了提高可视化的分辨率,添加显色剂K₃[Fe(CN)₆],实现了由黄色到蓝色的显著剂量依赖性颜色变化。
Apt-PDANS不仅可以作为“分离助剂”,通过过滤实现sEV的快速分离,还可以作为sEV多色可视化分析的报告信号。通过改变适配体的蛋白质识别序列,实现源自不同细胞的sEV上五种蛋白质标记物灵敏分析。结果表明,sEV蛋白质的表达表现出显著的异质性。此外,所构建的蛋白质谱在区分健康供体与癌症患者时展现出较高的准确性与特异性,进一步强调了SIMPLE策略在癌症分子诊断中的巨大潜力。
外泌体资讯网 Anal Chem|厦门大学朱志教授/苏蕊主任医师团队:多功能聚多巴胺纳米球助力细胞外囊泡的快速分离和灵敏多色可视化分析





