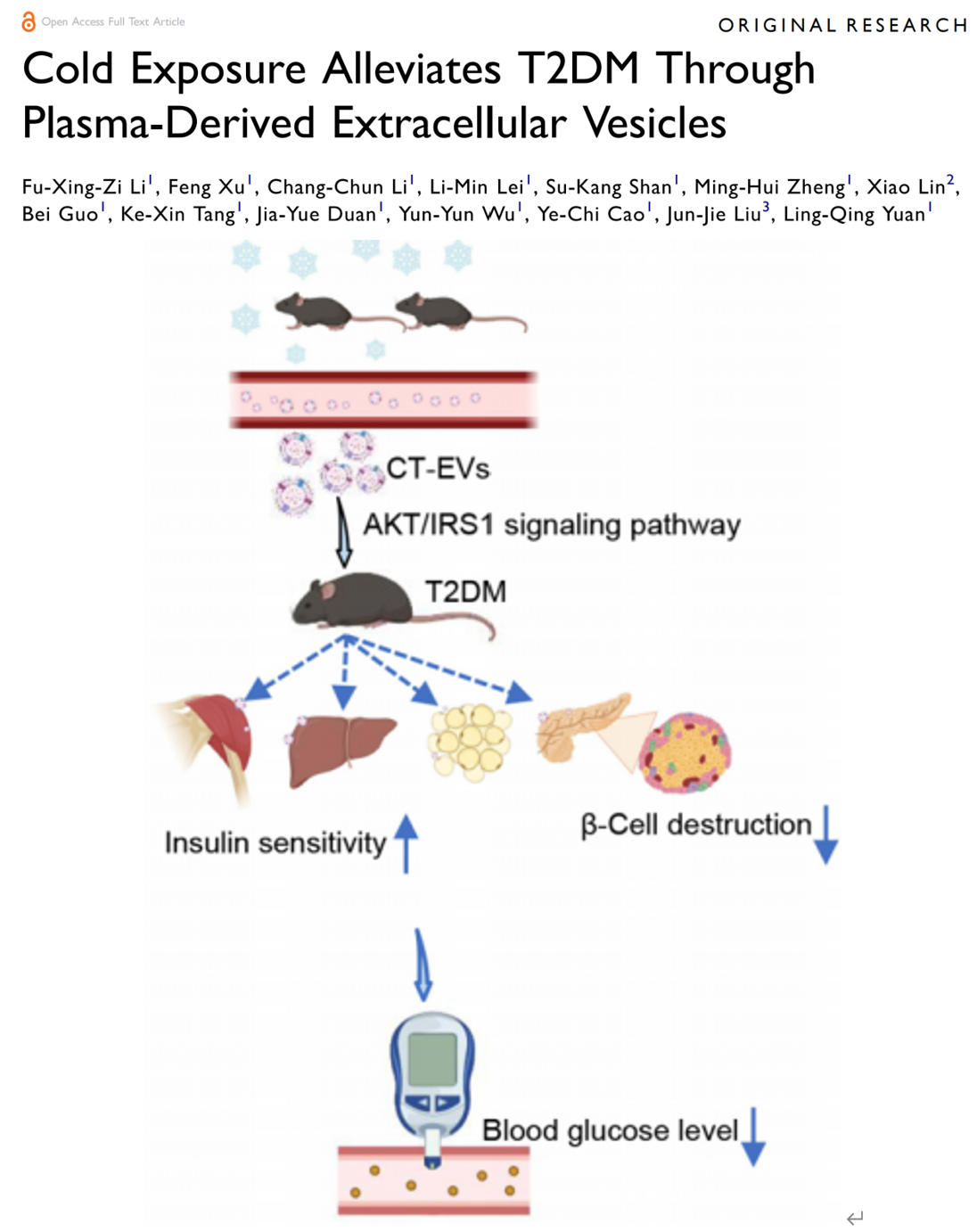
研究发现寒冷对于机体存在一定的益处,例如冬泳和冷水浸泡可对身体产生良性的影响。真实世界中,寒冷地区糖尿病患病率较热带发病率低,寒冷暴露是否可以缓解糖尿病的发生发展是一个是否有趣的话题。
近日,中南大学袁凌青教授/主任医师团队在INTERNATIONAL JOURNAL OF NANOMEDICINE杂志上发表题为“Cold Exposure Alleviates T2DM Through Plasma-Derived Extracellular Vesicles”的论文 (2024 Oct 2:19:10077-10095),主要介绍了长期冷暴露能够减轻T2DM小鼠模型的糖尿病。研究者通过将寒冷暴露小鼠的血浆输注给室温饲养的T2DM小鼠,证实寒冷暴露的小鼠血浆可以降低T2DM小鼠的血糖并增加其胰岛素敏感性。研究者发现来自冷暴露小鼠血浆中的细胞外囊泡(EVs)能够提升T2DM小鼠的胰岛素敏感性,并减轻β细胞的破坏作用。这可能是解释寒冷地区糖尿病发病率较低的一个重要原因。该论文第一作者李付杏子博士,通讯作者袁凌青教授,均来自于中南大学湘雅二医院代谢内分泌科。
该团队研究了寒冷暴露(CT,4–8°C)或室温(RT,22–25°C)对T2DM小鼠的影响。收集了小鼠的血液和器官样本,进行全自动生化检测、ELISA、HE染色、免疫组化和免疫荧光实验。通过流式细胞术结合2-NBDG评估葡萄糖摄取情况。通过Western blot分析了AKT、p-AKT、IRS1和p-IRS1等信号通路的变化。结果发现CT或CT小鼠血浆来源的细胞外囊泡(CT-EVs)显著降低了T2DM小鼠的血糖水平,并改善了胰岛素敏感性。这种治疗增强了葡萄糖代谢、全身胰岛素敏感性和胰岛素分泌功能,同时促进了肝脏和肌肉中的糖原积累。此外,CT-EVs治疗通过抑制β细胞凋亡,保护了T2DM小鼠胰岛免受链脲佐菌素破坏。CT-EVs还保护了胰岛,增加了脂肪细胞和肝细胞中p-IRS1和p-AKT的表达。相关体外实验也进一步证实了其促进胰岛素敏感性的作用。
最后作者使用Label-free蛋白质组学分析用于表征和量化RT-EVs和CT-EVs中的蛋白质。RT-EVs和CT-EVs之间的差异表达蛋白(p<0.05;|log2fold change|≥1.5)以火山图的形式展示。19种蛋白质在CT-EVs中的含量远高于 RT-EVs,而54种蛋白质在CT-EVs中的含量远低于RT-EVs。CT-EVs相对于RT-EVs中最为丰富的10种蛋白质和最为稀少的10种蛋白质的表达比例如图所示。为分类CT-EVs相对于RT-EVs中高度富集的蛋白质,进行了GO注释,根据其亚细胞定位进行分类发现其中 36.8% 的蛋白质来源于细胞外,38.7% 来源于细胞质。其余蛋白质则来源于细胞膜(5.7%)、内质网(5.7%)、细胞骨架(2.8%)、细胞核(4.7%)或线粒体(4.7%)。对上调蛋白质的GO生物学过程富集分析表明,CT-EVs富含参与运输、正向调节葡萄糖代谢过程、脂质代谢、胰岛素受体信号通路等相关的蛋白质,这表明CT-EVs在糖脂代谢和胰岛素敏感性方面具有功能性作用。KEGG通路富集分析显示,与RT-EVs相比,CT-EVs中上调的蛋白质参与了β细胞受体信号通路和PI3K-Akt信号通路,而CT-EVs中下调的蛋白质则涉及胰腺分泌、胰岛素抵抗或糖酵解/糖异生。这些发现表明,CT-EVs 选择性地富集了各种功能性蛋白质。
总之,该研究表明,冷暴露可能对T2DM的发展具有潜在的有益影响,主要是通过冷暴露下小鼠血浆来源的细胞外囊泡发挥抗糖尿病作用。这一现象可能有助于解释寒冷地区糖尿病患病率较低的原因。
外泌体资讯网 Int J Nanomed|中南大学湘雅二医院代谢内分泌科袁凌青教授研究员团队:寒冷暴露通过血浆来源的细胞外囊泡缓解2型糖尿病