近年来,细胞外囊泡(EVs)在诸如肿瘤、心血管疾病和神经退行性疾病等的诊疗方面显示出巨大潜力,特别是在卒中治疗领域,临床前研究结果极大的驱动了临床转化的可能。然而,由于单纯细胞外囊泡靶向能力有限,损伤区域较低的递送效率严重的限制了细胞外囊泡疗法的临床转化前景。为了克服上述挑战,制备工程化细胞外囊泡用于靶向递送,且无创、稳定、定量的监控这一靶向过程是进一步提高细胞外囊泡疗效的客观需求。常用的细胞外囊泡工程化策略主要包括基因工程和化学修饰。基因工程中由于病毒载体具有安全性问题而影响细胞外囊泡的临床使用。化学修饰允许使用广泛的配体或示踪剂直接通过偶联或脂质组装途径与细胞外囊泡膜反应。然而,由于细胞外囊泡膜表面的复杂性可能限制反应效率,且共价修饰需要引入化学物质来诱导或催化化学键,可能导致细胞外囊泡结构上,表面电位和功能改变。此外,在细胞外囊泡表面通过物理吸附手段直接偶联示踪探针,如碘-125,存在标记不稳定的问题,生理条件下碘-125易于从细胞外囊泡表面上脱标记。通过电穿孔法或超声法在细胞外囊泡表面包封靶向蛋白和示踪小分子可能影响细胞外囊泡膜的完整性,并导致细胞外囊泡内内容蛋白和RNA的损失。因此,急需开发一种简易且有效的策略,在不影响细胞外囊泡生物学活性的同时来持续的提高细胞外囊泡靶向递送能力。多巴胺(PDA)作为一种蚌类分泌的黏连蛋白吸引了研究者的广泛注意,由于其自组装能力和活泼的化学活性,使得其作为一种优良的包覆材料用于诊疗剂的构建。与其他复杂的工程化方法不同,多巴胺仅需要在弱碱性条件下温和搅拌,即可在细胞外囊泡表面形成一层超薄且致密的包覆层。多巴胺包覆层上广泛形成的儿茶酚-儿茶酚偶联结构非常易于螯合多种显像或诊疗剂金属离子,如Fe3+、Gd3+、Pt4+等。多巴胺还可以通过希夫碱或迈克尔加成反应直接与卤素、巯基或氨基反应,进一步提高了细胞外囊泡与放射性核素、抗生物团聚分子或单分子层的偶联效率,进而再接枝靶向分子。此外,多巴胺还可以在生理条件下中和活性氧(ROS),所以多巴胺包覆层还可以用于保护细胞外囊泡膜不受卒中条件下或工程化标记过程中的恶劣环境影响。基于上述特点,上海交通大学汤耀辉联合海军军医大学第一附属医院张璐团队在Journal of Extracellular Vesicles杂志上(中科院1区,5年影响因子 19.6)发表题为“A facile polydopamine-based platform for engineering extracellular vesicles with brain-targeting peptide and imaging probes to improve stroke outcome”的研究论文(2025.14(1): e70031)。通过构建多巴胺的表面功能化平台,实现细胞外囊泡表面的靶向肽和多模态成像探针的共修饰。利用该平台在M2型小胶质细胞来源的细胞外囊泡(M2-EVs)表面共同标记了神经靶向肽RVG29和多模态探针,实现了卒中小鼠的M2-EVs的靶向递送,并从全身尺度到细胞水平上动态的可视化了这一靶向递送过程。通过比较尾静脉、鼻腔注射和动脉注射途径,确定了动脉注射能够实现最高效的工程化细胞外囊泡靶向递送,有效的通过抑制神经元凋亡来提高治疗效果。
在机制方面,细胞外囊泡miRNA测序揭示了大量抗凋亡相关的miRNAs显著上调,包括miR-221-3p和miR-423-3p,均通过p38/ERK信号通路在卒中过程中发挥了抗凋亡效果。综上所述,该平台提供了一个简易且有效的手段用于细胞外囊泡的多功能工程化,实现了细胞外囊泡治疗效果的提高及疗效的多尺度可视化评估,显示出极有价值的临床转化前景。上海交通大学生物医学工程学院的博士生施晓婧,海军军医大学第一附属医院核医学科的张璐助理研究员,以及上海交通大学生物医学工程学院的博士生吴胜菊位列共同第一作者,上海交通大学生物医学工程学院的汤耀辉是论文的通讯作者。该研究受到了国家重点研发计划(2019YFA0112000,#2022YFA1603600),国家自然基金(82071284, 82371307, 81901804 , 82172529, 82271320),上海市教委青年领军科学家培养计划(ZXWH1082101),中央高校基本科研基金(YG2023ZD02,SUITM-202306),上海扬帆计划(23YF1420700)的资助。
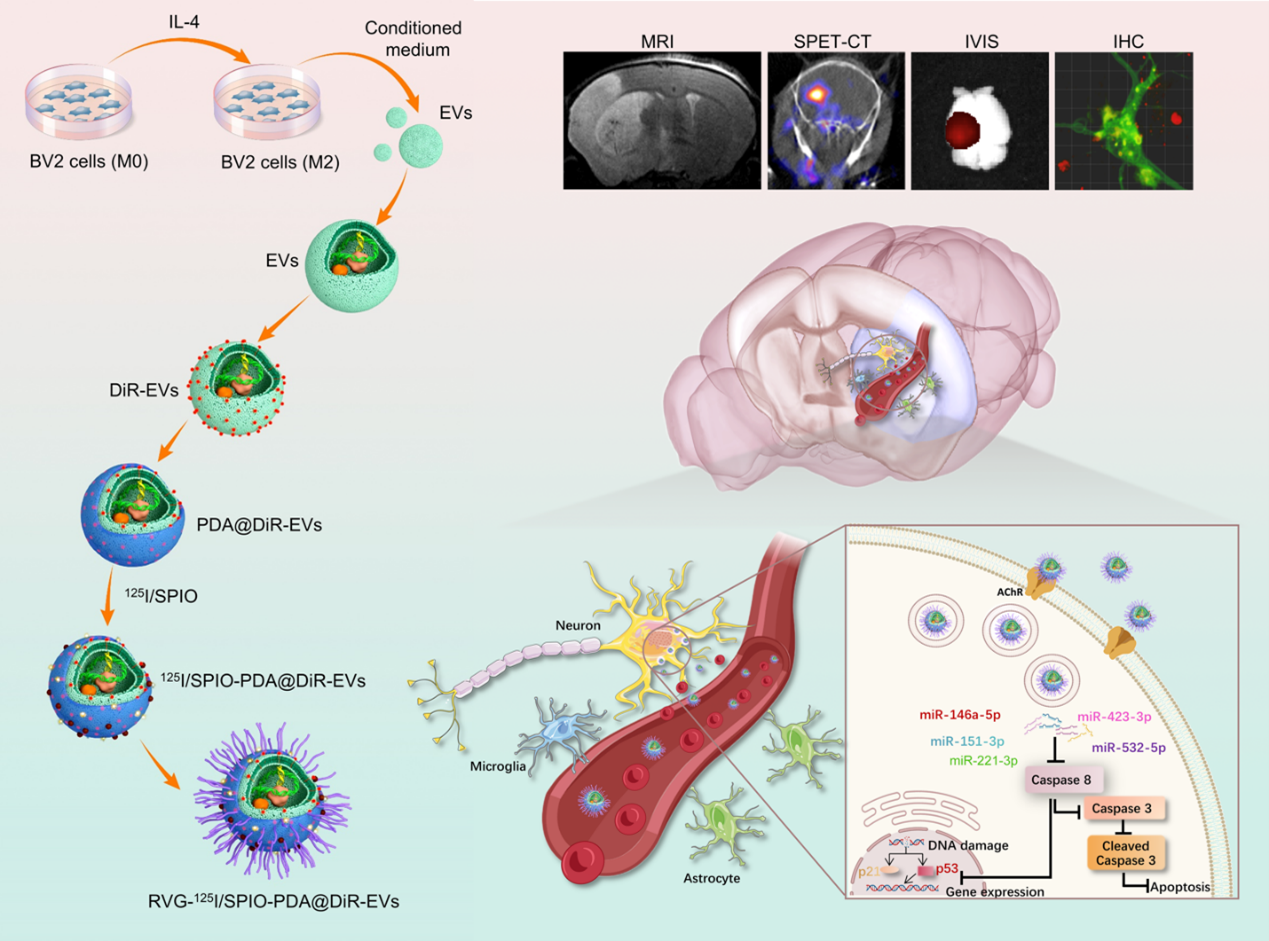
图1.多巴胺功能化平台,实现了在M2型小胶质细胞来源细胞外囊泡表面共标记神经靶向肽RVG29和多模态显像探针。该平台不仅提高了细胞外囊泡的神经靶向能力,还可以通过SPECT/MRI/荧光显像实现全身尺度到细胞水平上动态可视化这一靶向过程。在超急性卒中期对小鼠模型进行颈动脉注射工程化细胞外囊泡得到了最佳治疗效果。此外,通过miRNA测序分析,鉴定出miR-221-3p和miR-423-3p在M2型细胞外囊泡中显著上调,并通过p38/ERK信号通路发挥抗凋亡效果。参考文献:A simple polydopamine-based platform for engineering extracellular vesicles with brain-targeting peptide and imaging probes to improve stroke outcome, Journal of Extracellular Vesicles 2024,14(1): e70031原文链接:https://doi.org/10.1002/jev2.70031
外泌体资讯网 JEV|上海交大汤耀辉/海军军医大学一附属院张璐:基于多巴胺平台制备同时修饰靶向肽和多种显像探针的工程化EV促进其对卒中的治疗





