外泌体是由细胞内吞体衍生的小型细胞外囊泡,负责细胞间物质交流与信息传递,尤其在肿瘤发生与发展中扮演重要角色;同时,肿瘤微环境也会影响外泌体的分泌。先前的研究表明,机械力可以促进外泌体的释放;然而,机械力与外泌体分泌之间的直接关系尚待进一步探讨,目前仍缺乏关于机械力调控外泌体释放的直接证据和动态细节。近期,中国科学院长春应用化学研究所王宏达研究团队利用高分辨率成像技术直接观察了机械力对外泌体释放的实时促进性影响,并揭示了机械力诱导的肌动蛋白重排是外泌体释放的关键因素。相关研究成果以“Visualization of Mechanical Force Regulation of Exosome Secretion Using High Time-Spatial Resolution Imaging”为题于1月6日在线发表在国际知名学术期刊Analytical Chemistry杂志上(2025 Jan 21;97(2):1210-1220)。该论文的第一作者为中国科学院长春应用化学研究所博士研究生季鑫,通讯作者为中国科学院长春应用化学研究所徐海娇副研究员和王宏达研究员。
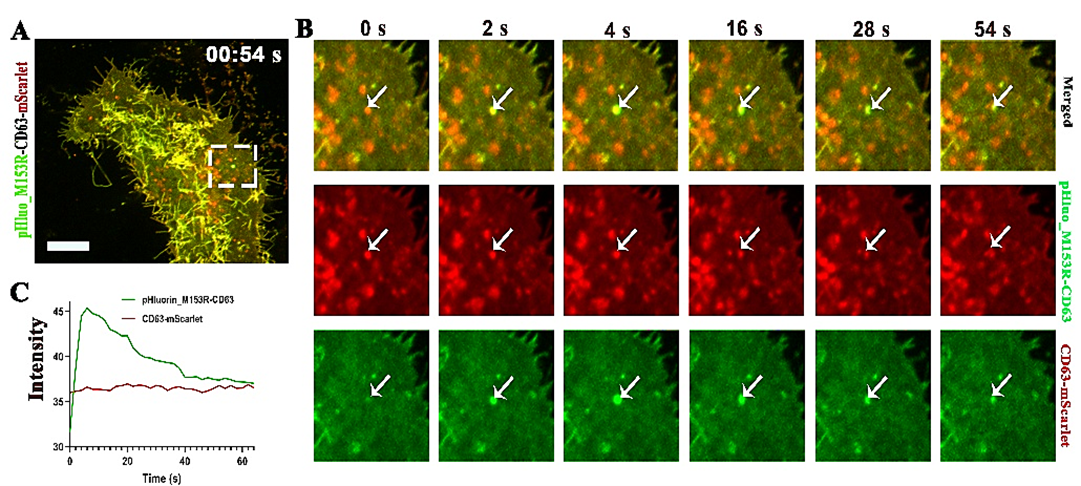
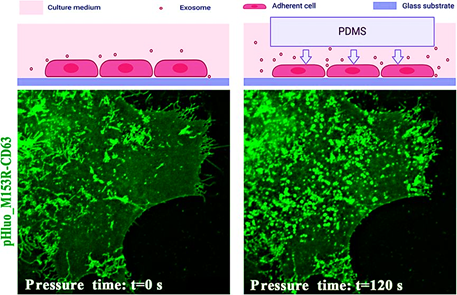
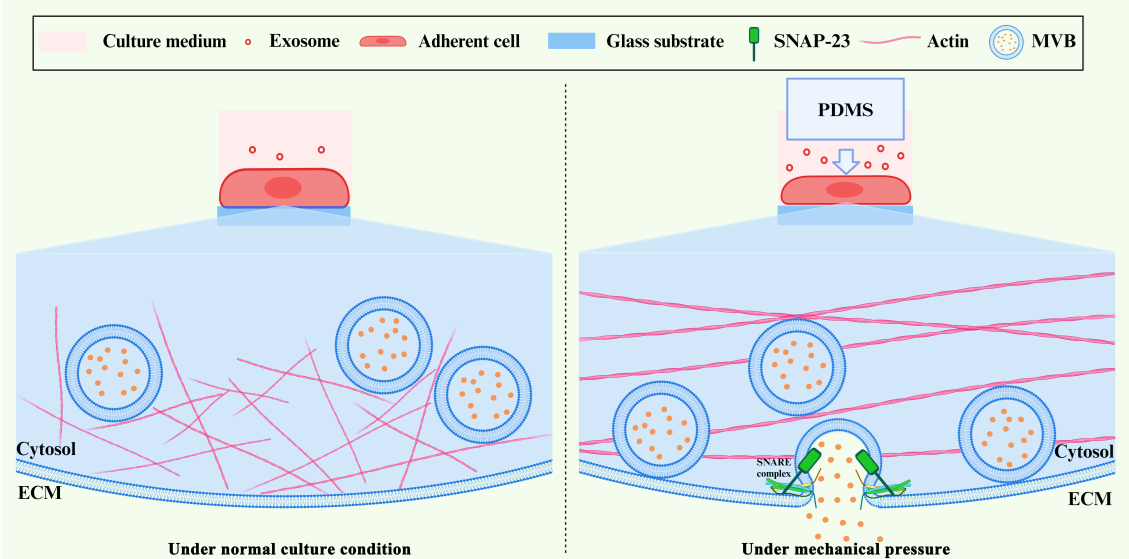
癌细胞相较于正常细胞产生更多的外泌体,这些外泌体对肿瘤微环境产生潜在影响,从而促进肿瘤发生与转移;同时,肿瘤微环境也会诱导外泌体的分泌,以帮助细胞抵御应激。因此,深入理解肿瘤微环境中的致癌信号对外泌体释放的调节机制,对于抑制相关疾病的发展至关重要。机械力变化是肿瘤微环境中的重要特征,影响癌症发展进程,包括肿瘤细胞的形态重塑、侵袭和迁移。除了接触细胞之间以及细胞和细胞外基质之间的信号传递;近期研究还表明,机械力能够刺激外泌体的分泌,从而实现非接触细胞之间的远程信号传递。然而,现有外泌体释放分析方法主要集中于从长期培养物中收集细胞上清液后的生化研究。这种方法往往忽略了外泌体释放的动态信息和细胞外囊泡的潜在异质性。因此,到目前为止,缺乏直接证据表明机械力变化是外泌体释放的触发因素,这也限制了对其调节机制的理解。直接成像多泡体(MVB)与质膜(PM)融合过程是可视化外泌体释放的有效方法。CD63是一种典型的外泌体标志蛋白,存在于多泡体及其内部囊泡中,广泛用于追踪外泌体分泌。在这项研究中,研究人员利用基于CD63双标记报告基因的(pHluo_M153R-CD63-mScarlet)的高速转盘式共聚焦显微镜,在单囊泡水平上跟踪了单个MVB从融合前的锚定到与质膜融合以释放外泌体的动态过程。随后,研究人员使用自制的PMDS薄片对HeLa细胞施加机械压力,通过荧光动态成像在单细胞水平上原位实时捕捉到机械压力刺激促进外泌体大量释放的情景。进一步,该团队探索了机械压力对外泌体释放的潜在调控机制。研究人员发现相比对照组,承受机械压力的细胞中的肌动蛋白有重排成应力纤维的现象。通过活细胞原位成像观察到,肌动蛋白呈应力纤维形态的细胞中,多泡体与质膜的锚定和融合事件显著增多。这些研究结果支持以下模型:机械压力通过诱导肌动蛋白骨架重排,促进多泡体与质膜的锚定和融合,从而增强外泌体的释放。这凸显了肌动蛋白细胞骨架组织形貌、机械压力和外泌体释放之间错综复杂的相互作用,为研究外泌体在机械力刺激下的分泌机制提供了重要见解。这项研究揭示了机械力刺激与外泌体释放之间的密切关系,为以更直观的方式探索外部刺激对外泌体分泌的影响奠定了基础。未来,研究团队将继续深入探讨机械力调控外泌体释放的分子机制,从而为药物发现提供新靶点。这一研究成果的发表,标志着我们在理解外泌体生物学和肿瘤微环境调控方面迈出了重要一步,为未来的基础研究和临床应用提供了新的方向。Visualization of Mechanical Force Regulation of Exosome Secretion Using High Time-Spatial Resolution Imaging, Anal Chem. 2025 Jan 6. doi:10.1021/acs.analchem.4c04690外泌体资讯网 Anal Chem|中国科学院长春应用化学研究所王宏达团队:利用高时空分辨率成像技术捕获机械力调控外泌体释放的时空动态