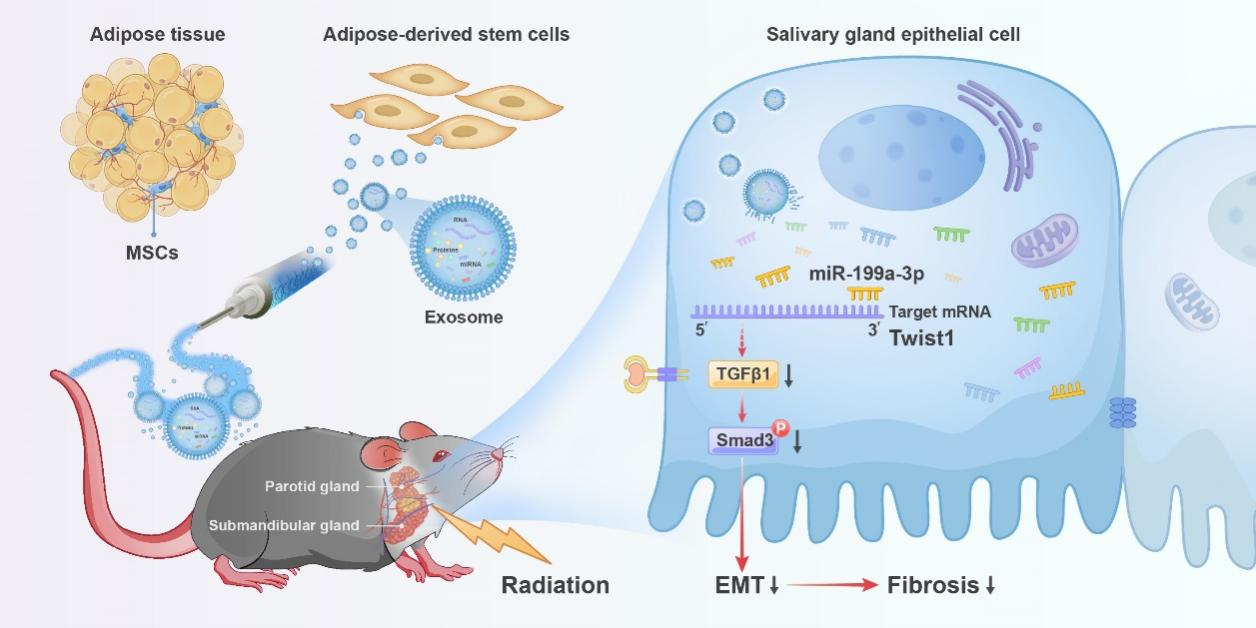
放疗在头颈部肿瘤的综合治疗中占有重要地位, 目前临床采用多种手段使放疗趋于精准化,可一定程度上减少放射后不良反应。然而,高达80%的头颈部肿瘤患者在放疗后可逐渐出现唾液腺(salivary gland, SG) 损伤和功能减退,并发口干、严重龋齿及黏膜炎症等并发症,显著降低肿瘤患者放疗后的生活质量。唾液腺纤维化常作为疾病的最终病理转归,会严重影响腺体内功能细胞的唾液分泌作用,与疾病的临床症状密不可分。目前临床仅能通过催涎剂、黏膜润滑剂进行姑息治疗,或应用生物活性因子(如IGF-1)缓解口干症状,尚无有效逆转放射性唾液腺损伤的治疗方法。目前,已有多种间充质干细胞用于放射性唾液腺损伤治疗,包括骨髓间充质干细胞、牙髓干细胞、脂肪干细胞(adipose derived stem cell, ADSC)和唾液腺干细胞等。研究证明干细胞疗效主要在于其旁分泌作用,即细胞释放分子信号物质(如蛋白质、激素、生长因子等)到周围环境中,影响相邻或非相邻的细胞的功能和行为。探索干细胞旁分泌产物对放射性唾液腺损伤疾病的作用及疗效机制可为该类生物活性物质的临床转化奠定基础。日前,中山大学光华口腔医院林正梅教授和苏心韵研究员团队于Theranostics杂志上发表了题为“Exosomes of human adipose stem cells mitigate irradiation injury to salivary glands by inhibiting epithelial-mesenchymal transition through miR-199a-3p targeting Twist1 and regulating the TGFβ1/Smad3 pathway”的论文(2025 Jan 2;15(5):1622-1641)。该研究首次提出使用脂肪干细胞外泌体(ADSC-exosomes, ADSC-Exos)治疗放射性唾液腺损伤疾病,并进一步探索了外泌体中效用分子miRNA的作用机制。硕士研究生郭小童为论文的第一作者,林正梅教授和苏心韵研究员为论文的共同通讯作者。
该研究从临床棘手的放射性唾液腺损伤疾病入手,探究外泌体对唾液腺功能减退及纤维化的治疗作用及分子机制。作者首先通过构建动物疾病模型,证明ADSC-Exo增强唾液腺功能并促进组织再生,同时抑制放射性唾液腺纤维化。进一步应用第二代测序技术加以生物信息学分析,推测与纤维化相关的TGFβ信号通路可能是治疗放射性唾液腺损伤疾病的关键策略,并揭示了ADSC-Exo中的潜在效应分子miR-199a-3p。最后通过一系列体外实验,证明ADSC-Exo通过miR-199a-3p靶向Twist1,调控TGFβ1/Smad3轴抑制放射性唾液腺纤维化。至此,ADSC-Exo的作用机制基本被阐明,该研究为改善放射性唾液腺损伤和纤维化提供分子治疗靶点。Exosomes of human adipose stem cells mitigate irradiation injury to salivary glands by inhibiting epithelial-mesenchymal transition through miR-199a-3p targeting Twist1 and regulating TGFβ1/Smad3 pathway.Theranostics. 2025 Jan 2. 15 (5): 1622-1641.外泌体资讯网 Theranostics | 中山大学光华口腔医院林正梅/苏心韵:人源脂肪干细胞外泌体治疗放射性唾液腺损伤并抑制腺体纤维化