新冠、甲流、乙流等呼吸道病毒的快速传播凸显了对广谱抗病毒疗法的迫切需求。传统中和药物(如抗体、重组蛋白)依赖非共价结合,易因病毒突变失效,且需频繁给药维持血药浓度。宿主细胞表面ACE2受体是新冠病毒入侵的关键靶点,但其天然亲和力有限,难以阻断高突变病毒株。
近日,深圳湾实验室饶浪团队联合北京大学、广州医科大学等机构,在Cell Biomaterials期刊发表题为“Antiviral covalent ACE2 vesicle spray”的突破性研究。该研究成功开发出一种基于共价工程化ACE2纳米囊泡的抗病毒喷雾(nanoSpray),可实现不可逆结合新冠病毒(SARS-CoV-2)及其变异株,显著提升肺部滞留时间,并在动物实验中展现出优异的治疗效果,这一成果有望为应对呼吸道病毒感染提供新的策略。
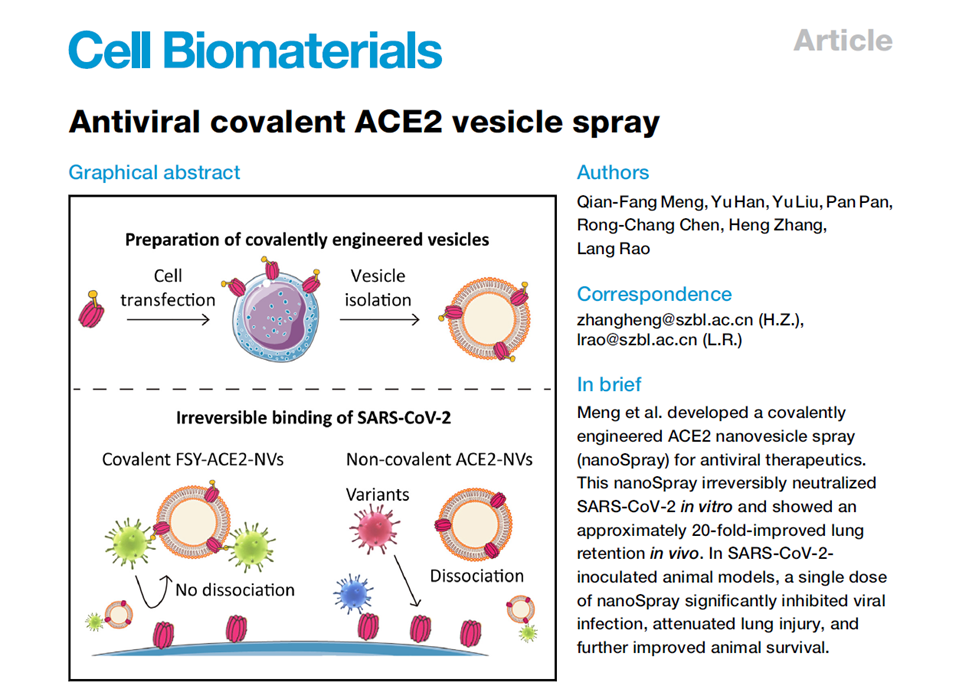
图1. 新型共价工程化抗呼吸道病毒喷雾
在这项研究中,作者通过基因密码扩展技术,将人工氨基酸氟磺酸-L-酪氨酸(FSY)定点插入ACE2蛋白,构建共价工程化的ACE2纳米囊泡(FSY-ACE2-NVs)。该囊泡可通过“硫氟交换点击化学”与病毒刺突蛋白RBD结构域形成不可逆结合,阻断病毒入侵宿主细胞。
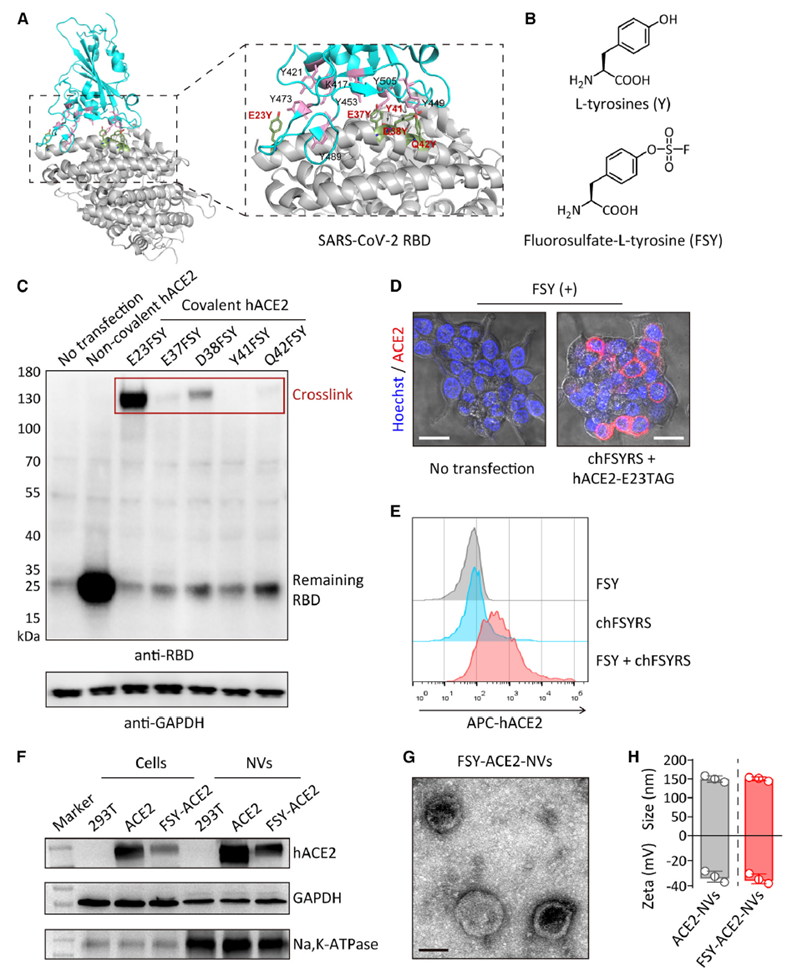
图2. 共价工程化抗病毒纳米喷雾的制备及表征
核心优势
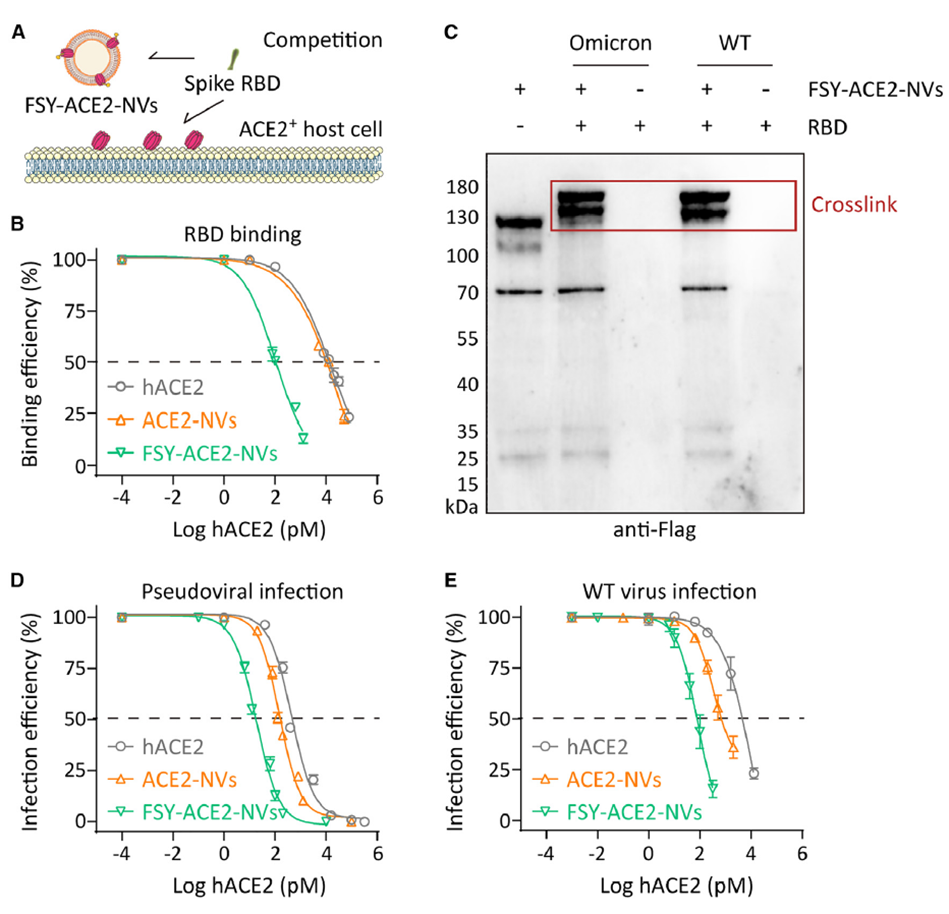
广谱高效:实验显示,FSY-ACE2-NVs对野生型病毒和奥密克戎变种的中和效率分别较传统ACE2蛋白提升60倍和5倍,IC50值低至19.95 pM。长效滞留:喷雾中添加黏膜粘附剂透明质酸(HA)后,纳米囊泡在肺部的滞留时间延长约20倍,单次给药可持续作用96小时。便捷储存:冻干配方可在4℃下稳定储存超1个月,活性保持90%以上,便于运输与使用。
图3. 共价工程化抗病毒纳米喷雾可实现不可逆结合新冠病毒及其变异株
动物实验验证
在表达人源ACE2的转基因小鼠模型中,单次吸入FSY-ACE2-NVs喷雾:
使野生型病毒感染存活率从0%提升至90%,肺部病毒载量降低10倍;对奥密克戎变种感染,预防性给药可完全阻断病毒入侵,治疗组存活率达100%;显著减轻肺部炎症损伤,抑制细胞因子风暴。

图4. 共价工程化抗病毒纳米喷雾预防与治疗SARS-CoV-2感染
该研究首次将共价化学与囊泡递送技术结合,为应对新冠病毒变异及未来新发呼吸道病毒提供了创新平台。下一步将优化多靶点共价结合设计,以应对病毒关键位点突变,并推动临床转化。此项技术有望成为日常防护与治疗的重要工具,助力呼吸道病毒混合感染防控。
该研究由深圳湾实验室饶浪、Heng Zhang团队联合北京大学、广州医科大学等机构完成。
原文链接:
https://doi.org/10.1016/j.celbio.2025.100017