癌症疫苗通过递送免疫原性抗原,在癌症预防和治疗中受到广泛关注。然而,传统疫苗常因表位范围有限而难以达到预期效果。个性化癌症疫苗通过利用患者自身肿瘤材料触发针对独特抗原的个性化强效免疫反应,展现出更优的疗效。与传统方法相比,此类疫苗显示出显著优势。然而,体外制备的复杂流程、低产量、次优疗效及高昂成本阻碍了其临床应用。
原位自体疫苗接种(ISV)策略为癌症免疫治疗提供了一种新方法,能够克服上述挑战,并带来更广泛、持久的治疗益处。ISV策略的核心吸引力在于其使用“现成”组分(如光动力疗法(PDT)和TLR7/8激动剂等免疫佐剂。这些成分直接递送至肿瘤部位,既能杀死癌细胞,又能刺激免疫细胞。其主要目标是通过放疗等治疗手段诱导垂死癌细胞释放独特抗原,这些抗原随后被激活的免疫细胞摄取,从而引发系统性免疫反应。简而言之,ISV疗法虽对所有患者采用标准化方案,却能根据个体癌症特征引发个性化免疫反应。此外,与mRNA疫苗等个性化疫苗相比,ISV理论上能暴露患者更广泛的肿瘤抗原,可能诱导更强效、全面的免疫反应,从而有效攻击肿瘤并降低复发风险。
垂死癌细胞释放的肿瘤源性细胞外囊泡(TEVs)携带多种肿瘤细胞独特抗原,可作为ISV的载体。然而,这些囊泡的低释放率及其携带的免疫抑制蛋白(如程序性死亡配体1(PD-L1)和CD47)对ISV治疗构成了重大挑战。这些蛋白通过与免疫细胞相互作用抑制免疫激活。因此,提升ISV衍生TEV疗法的免疫原性和释放效率是亟待解决的关键问题。近期研究表明,诱导肿瘤细胞内质网应激可产生有效激活树突状细胞(DCs)的囊泡,但该方法释放效率低且不适用于ISV。通过程序性细胞死亡机制(如坏死性凋亡和焦亡)将癌细胞转化为囊泡,是一种新型ISV策略。这种方法将原发肿瘤转化为个性化癌症免疫治疗的抗原库。然而,程序性细胞死亡通常伴随活性氧(ROS)的爆发性生成。在高ROS和DNA损伤条件下,肿瘤细胞可能激活应激保护机制,增加细胞外囊泡中PD-L1和CD47等免疫抑制蛋白的负载,从而抵消抗肿瘤免疫反应。
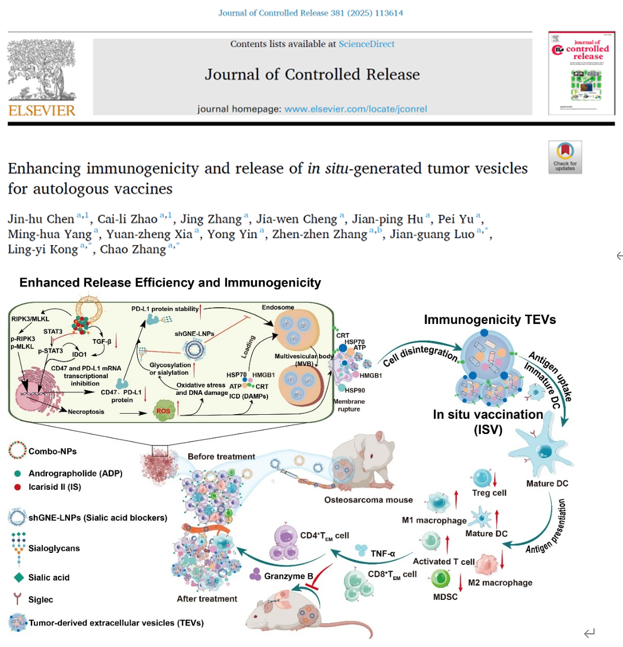
针对以上问题,中国药科大学罗建光/孔令义/张超团队在Journal of Controlled Release杂志上发表题为“Enhancing immunogenicity and release of in situ-generated tumor vesicles for autologous vaccines”的研究论文(2025 Mar 9:381:113614),主要介绍了一种由穿心莲内酯(Andrographolide,免疫增强剂)、淫羊藿次苷II(Icariside II,免疫抑制缓解剂)及靶向唾液酸合成关键酶GNE的shRNA组成的肿瘤ISV策略(Combo-NPs@shGNE)(图1)。该策略通过诱导坏死性凋亡、抑制唾液酸合成及调节囊泡货物负载,显著提升TEV的免疫原性和释放效率,为癌症免疫治疗提供了创新性解决方案。该论文的第一作者为中国药科大学博士研究生陈金虎和硕士研究生赵彩莉,通讯作者为中国药科大学罗建光教授、孔令义教授和张超副研究员。
图1 基于原位肿瘤囊泡的免疫增效策略示意图
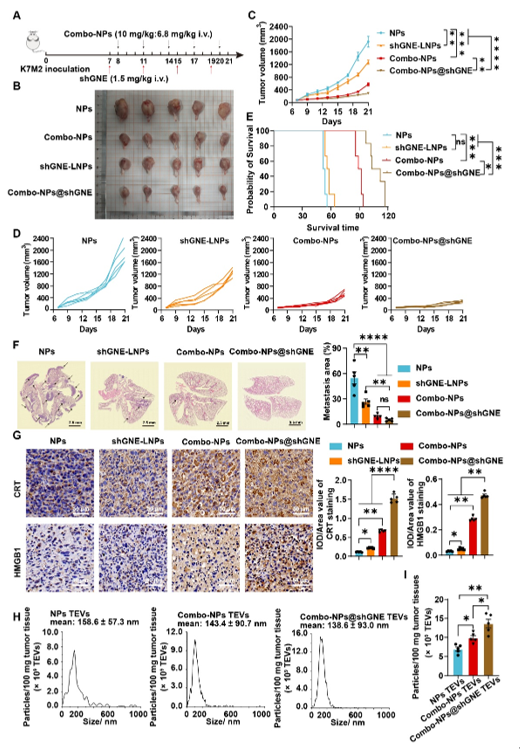
该研究提出了一种新型肿瘤原位疫苗策略,通过纳米颗粒递送系统联合调控肿瘤细胞死亡机制与糖基化代谢,显著提升TEVs的免疫原性与释放效率,为个性化癌症免疫治疗提供创新方案。研究团队开发了由穿心莲内酯、淫羊藿苷II和靶向唾液酸合成关键酶GNE的shRNA组成的纳米复合体系。该策略通过诱导坏死性凋亡触发肿瘤细胞免疫原性死亡,同时抑制唾液酸生物合成,双重调控TEVs的蛋白载物组成。一方面减少免疫抑制蛋白PD-L1和CD47的膜表面负载,阻断"Not Eat Me"信号;另一方面促进损伤相关分子模式(DAMPs)如HMGB1和HSP70的富集,增强抗原提呈能力。实验表明,该方案使TEVs释放效率提升至56.44%,并在骨肉瘤和乳腺癌模型中显著抑制肿瘤生长和肺转移,延长小鼠生存期(图2)。其创新性体现在:(1)首创坏死性凋亡与糖基化代谢协同调控机制,突破传统单一死亡模式引发的代偿性免疫抑制;(2)通过唾液酸合成通路干预精准调控TEVs表面糖基化修饰,解决外泌体PD-L1的免疫逃逸难题;(3)开发多功能纳米载体,实现药物/基因的肿瘤靶向共递送与微环境重塑,促进树突状细胞成熟及CD8+ T细胞浸润,将"冷肿瘤"转化为"热肿瘤",为突破实体瘤免疫治疗耐受难题提供了兼具转化可行性和临床适应性的解决方案,在个体化肿瘤疫苗开发领域具有重要应用前景。
图2 穿心莲内酯/淫羊藿次苷II/shGNE联合诱导高免疫原性肿瘤源性细胞外囊泡的释放
参考文献:
Enhancing immunogenicity and release of in situ-generated tumor vesicles for autologous vaccines. Journal of Controlled Release, 2025, 381: 113614. https://doi.org/10.1016/j.jconrel.2025.113614
外泌体资讯网 J CONTROL RELEASE|基于肿瘤EVs的免疫增效策略:穿心莲内酯/淫羊藿次苷II/shGNE联合促进原位自体疫苗构建