细胞外囊泡(EVs)是由大多数细胞分泌的纳米级囊泡,广泛存在于各种体液中。它们携带亲本细胞的蛋白质、核酸等生物活性物质,在细胞间通信中扮演关键角色。EVs能够选择性地识别受体细胞并调节其生物活性,影响其生理和病理生理过程。近年来,EVs在肿瘤发生、增殖与转移中的作用备受注意,有望成为癌症液体活检中的重要生物标志物,用于癌症的早期诊断、治疗和监测。然而,EVs体积小、密度低、成分复杂,这给有效分离和准确定量带来了重大挑战。
为应对上述挑战,南京医科大学附属南京医院何帮顺教授团队构建了一种创新的外泌体检测平台,该平台将基于金属有机框架(MOF)的DNA生物条形码技术与G-四链体/滚环扩增(RCA)反应相结合,实现了肿瘤相关EVs的超灵敏检测。该研究于近日以“Ultrasensitive Detection of Extracellular Vesicles Based on Metal-Organic Framework DNA Biobarcodes Triggered G-Quadruplex Coupled with Rolling Circle Amplification Assay”为题在线发表于ACS Sensors杂志上(doi: 10.1021/acssensors.4c0338)。文章第一作者为南京医科大学硕士生毕雯,通讯作者为南京医科大学附属南京医院何帮顺教授、南京大学宋玉君教授和皖南医学院高彦峰博士。
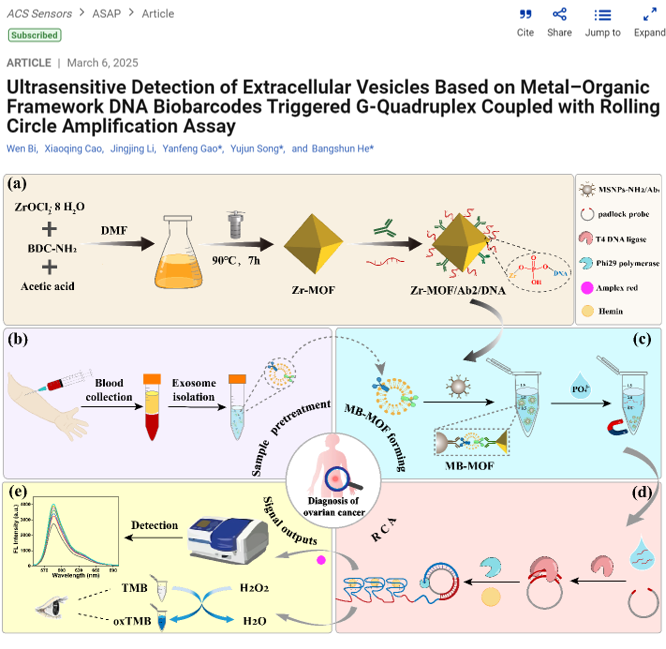
图1. MOF-DNA生物条形码与G-quadruplex/RCA系统结合
用于EVs超灵敏检测的示意图
在这项研究中,研究人员将MOF-DNA生物条形码策略与G-quadruplex/RCA系统相结合,成功开发了一种超灵敏检测癌症相关EVs的新型纳米生物传感器。该技术利用功能化的锆基MOF(Zr-MOF)纳米颗粒作为信号转化器,将难以测量的EVs含量转化为易于定量的DNA条形码,进而触发后续的G-四链体/RCA反应,进一步实现了信号的放大,并通过荧光法和比色法进行信号检测,实现了EVs的超灵敏和可视化检测。
该平台的创新性在于,它不仅实现了外泌体的信号转换,还极大地提高了EVs生物标志物的检测灵敏度,在最佳实验条件下实现了低至100 EVs/mL的检测限。而且利用该策略检测EVs,整个过程在5小时内就能完成,与传统的检测方法相比,该方法不仅耗时短,而且操作简单、不需要借助复杂仪器就能完成可视化检测,有利于即时检测(POCT)的进行。总体而言,该策略实现了EVs标志物的准确、快速、超灵敏检测,在卵巢癌(OvCa)临床诊断中显示出巨大的潜力。除此之外,该检测方法的设计思路具有通用性,通过简单地替换Zr-MOF上修饰的抗体,该生物传感器就可以推广到更多种类疾病肿瘤标志物、细菌、细胞和其他小分子物质的定量检测,为临床疾病诊断提供了一种新的研究手段和思路。
参考文献:
Ultrasensitive Detection of Extracellular Vesicles Based on Metal-Organic Framework DNA Biobarcodes Triggered G-Quadruplex Coupled with Rolling Circle Amplification Assay. ACS sensors, 6 Mar. 2025, doi:10.1021/acssensors.4c03384.
外泌体资讯网 ACS Sensors|南京医科大学附属南京医院何帮顺教授团队:新型MOF-DNA传感器实现肿瘤外泌体超灵敏检测