肥胖已成为全球性公共健康问题,其中30-49岁中年人群的肥胖相关全因死亡率显著高于其他年龄段。这一特殊现象与脂肪组织的年龄依赖性功能紊乱密切相关。作为人体最大的能量储存器官和内分泌器官,白色脂肪组织(WAT)在维持全身糖脂代谢稳态中发挥核心作用。研究表明,WAT是机体衰老的"前哨站",其功能衰退早于其他代谢器官,而脂肪祖细胞(adipose progenitor cells, APCs)在这一过程中起关键驱动作用。脂肪组织衰老的特征性改变包括:1、慢性低度炎症(inflammaging):作为WAT中最大的免疫细胞群体,脂肪组织巨噬细胞(adipose tissue macrophages, ATMs)参与炎症调控;2、细胞间通讯异常:细胞外囊泡(extracellular vesicles, EVs)作为携带蛋白质、脂质和microRNA(miRNA)等生物分子的膜性囊泡,在细胞间信号传递中发挥重要作用。尽管EVs在多种代谢疾病发病机制中的作用已被证实,但其在中年肥胖中的具体调控机制尚不明确。近期研究提示,APCs来源的EVs可能通过调控ATMs功能参与年龄相关性肥胖的发生发展,这一假说为阐明中年肥胖的分子机制提供了新思路。
2025年3月20日,华中科技大学同济医学院王从义教授团队在Nature Communications发表重磅研究,首次揭示脂肪祖细胞来源的外泌体通过miR-145 - SELL轴调控巨噬细胞极化,这成为中年肥胖的关键驱动因素。该研究为肥胖干预提供了全新治疗靶点。该论文的第一作者为华中科技大学周庆博士、高佳博士、吴国娆博士及美国贝勒医学院王晨玮博士,通讯作者为华中科技大学王从义教授、成都市第三人民医院刘雁军教授、山西白求恩医院刘师伟教授。
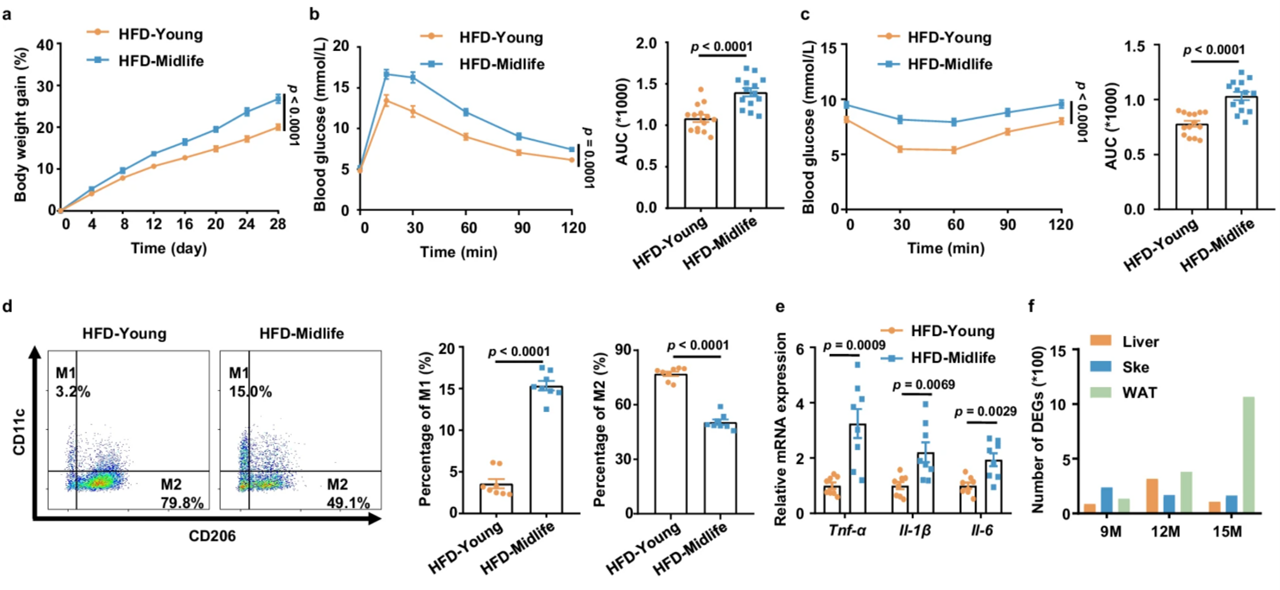
该研究首先证实,相较于年轻个体,12月龄小鼠在高脂饮食(HFD)条件下表现出更显著的体重增加趋势,葡萄糖耐量受损,胰岛素敏感性显著降低。小鼠附睾脂肪组织中促炎巨噬细胞显著增加,以上结果表明中年个体对肥胖的易感性显著增加(图1)。
图1:中年小鼠对肥胖的易感性显著增加
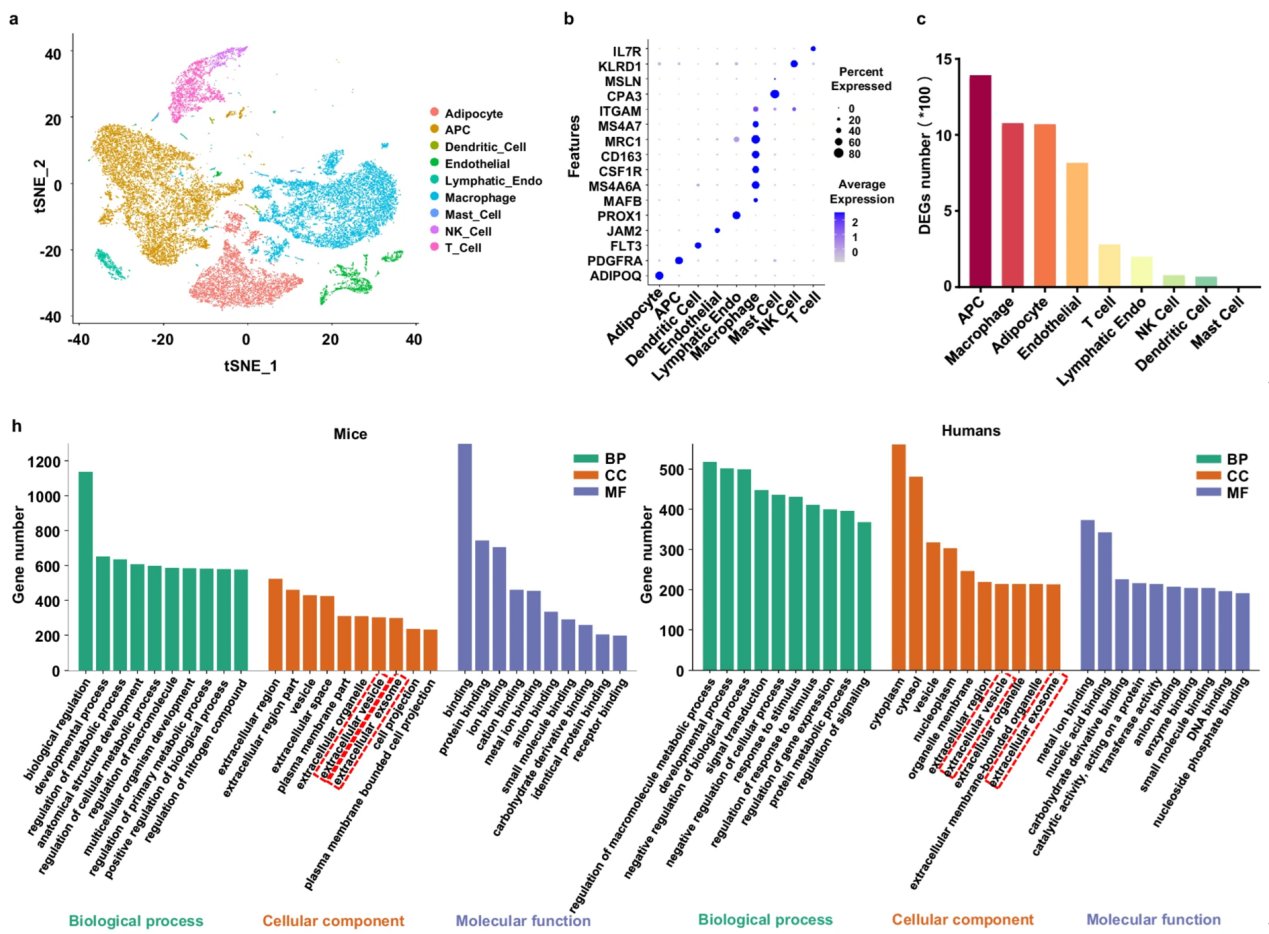
研究团队进一步结合单细胞测序和RNA测序分析发现,APCs是中年受试者 WAT 功能改变最显著的细胞亚群,中年个体(小鼠12月龄/人类30-49岁)白色脂肪组织中APCs功能显著退化,表现为衰老标志物(p16、p21等)表达升高,增殖分化能力下降,进一步分析发现APCs及其分泌的胞外囊泡(EVs)在中年肥胖中扮演了重要角色(图2)。
图2:年轻个体和中年个体的 WAT 样本单细胞测序及RNA-seq 分析
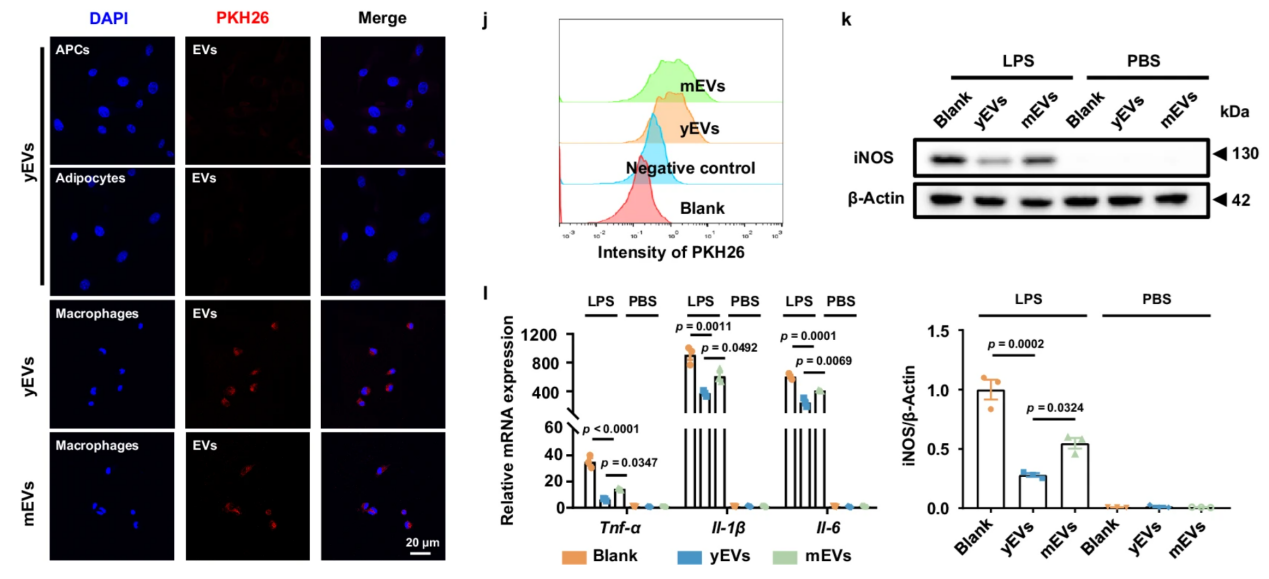
研究团队通过荧光标记和流式细胞术证实,APC-EVs主要被脂肪组织巨噬细胞(ATMs)摄取。年轻APC-EVs可显著抑制巨噬细胞M1型极化(促炎表型),而中年APC-EVs此功能明显减弱(图3)。
图3:荧光及流式检EVs的吞噬,炎症相关的蛋白和基因的检测
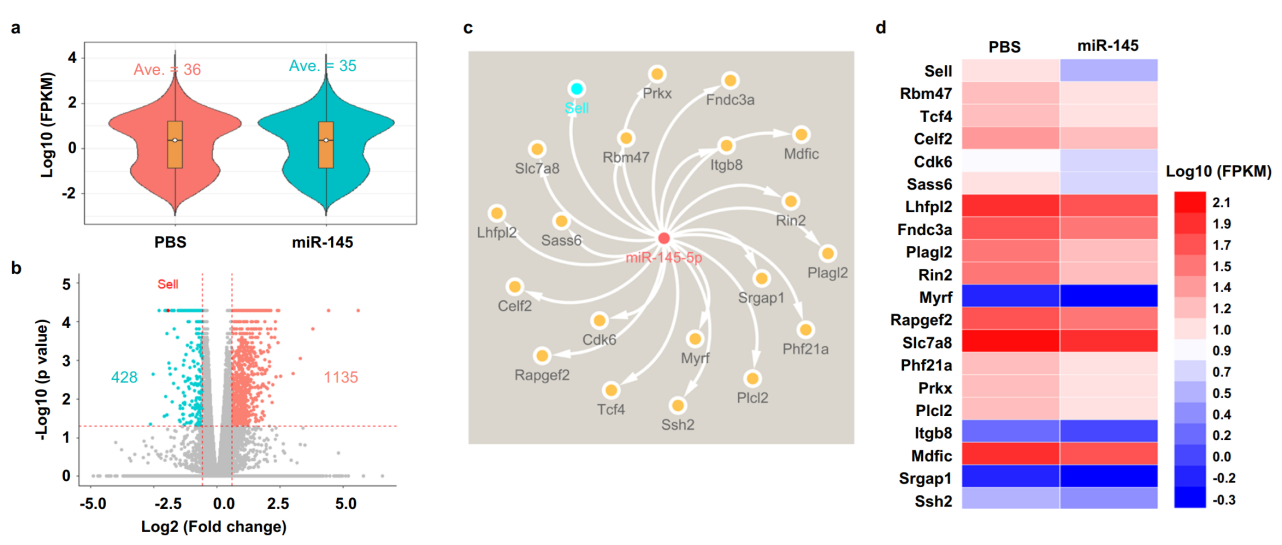
机制研究表明,EVs中的miR-145通过靶向抑制SELL表达,阻断NF-κB信号通路,从而遏制巨噬细胞炎症反应。在中年个体中,脂肪祖细胞衰老,其分泌的胞外囊泡中miR-145水平显著下降,导致SELL-NF-κB轴过度激活,促进M1型巨噬细胞极化,加剧脂肪组织“炎性衰老”(inflammaging)和胰岛素抵抗,最终导致肥胖的发生。相比之下,年轻APCs来源的EVs则通过上调miR-145-5p水平,有效抑制M1型巨噬细胞极化,维持代谢健康(图4)。
图4:PBS和miR-145 mimics处理组靶基因预测及潜在差异表达靶基因的热图
为实现研究成果的临床转化,基于以上发现,研究人员开发了一种新型递送系统——特异性靶向肽的阳离子脂质体(miR-145@tar-lip)。通过静脉注射给药,该系统能够精准地将治疗性miRNA递送至目标细胞群。实验结果显示,在中年肥胖小鼠模型中,miR-145@tar-lip治疗显著降低了小鼠脂肪组织衰老标志物水平及炎症因子(TNF-α、IL-6等)的表达,有效改善中年个体代谢异常(图5)。
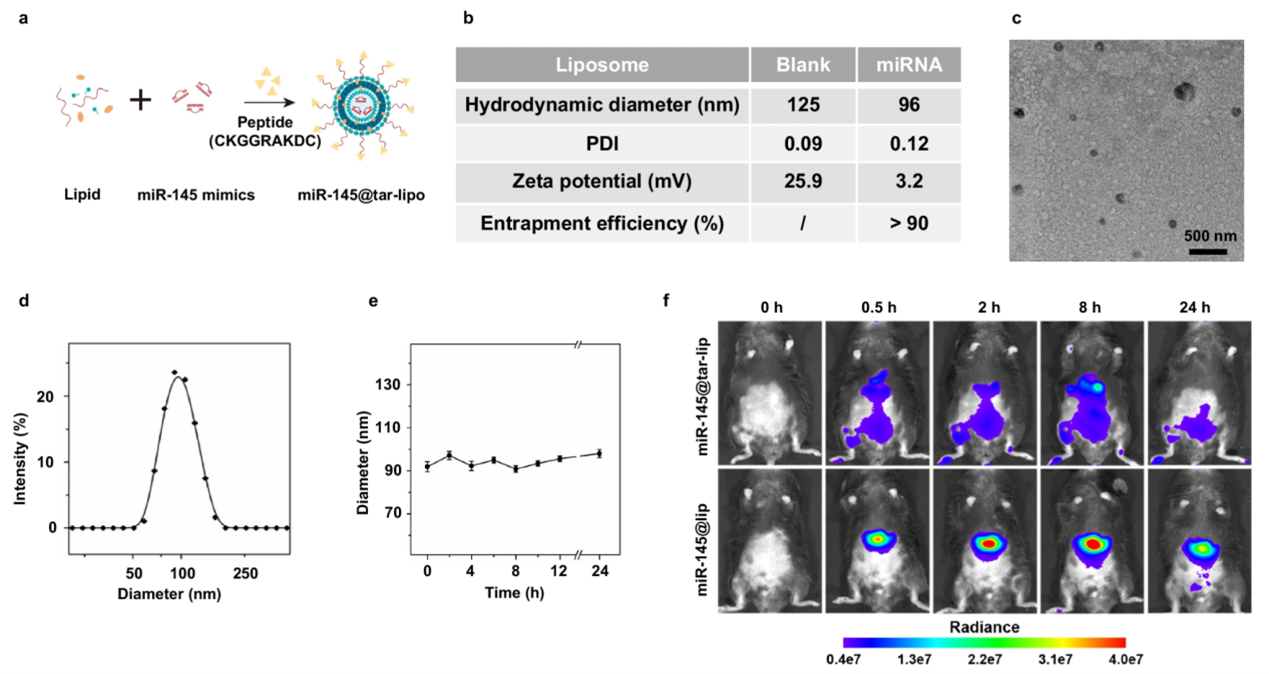
图5:miR-145@tar-lip 通过肽 (CKGGRAKDC)与脂质体(miR-145@lip)表面结合的示意图
综上所述,这项研究揭示了APC来源的细胞外囊泡中miR-145-5p通过抑制SELL-NF-κB信号轴,抑制脂肪组织巨噬细胞M1极化,调节中年个体肥胖的发生发展,在中年肥胖发病机制中发挥关键作用。该研究揭示miR-145-5p可作为干预中年代谢紊乱的新靶标,为中年人群的代谢调控提供新思路(图6)。
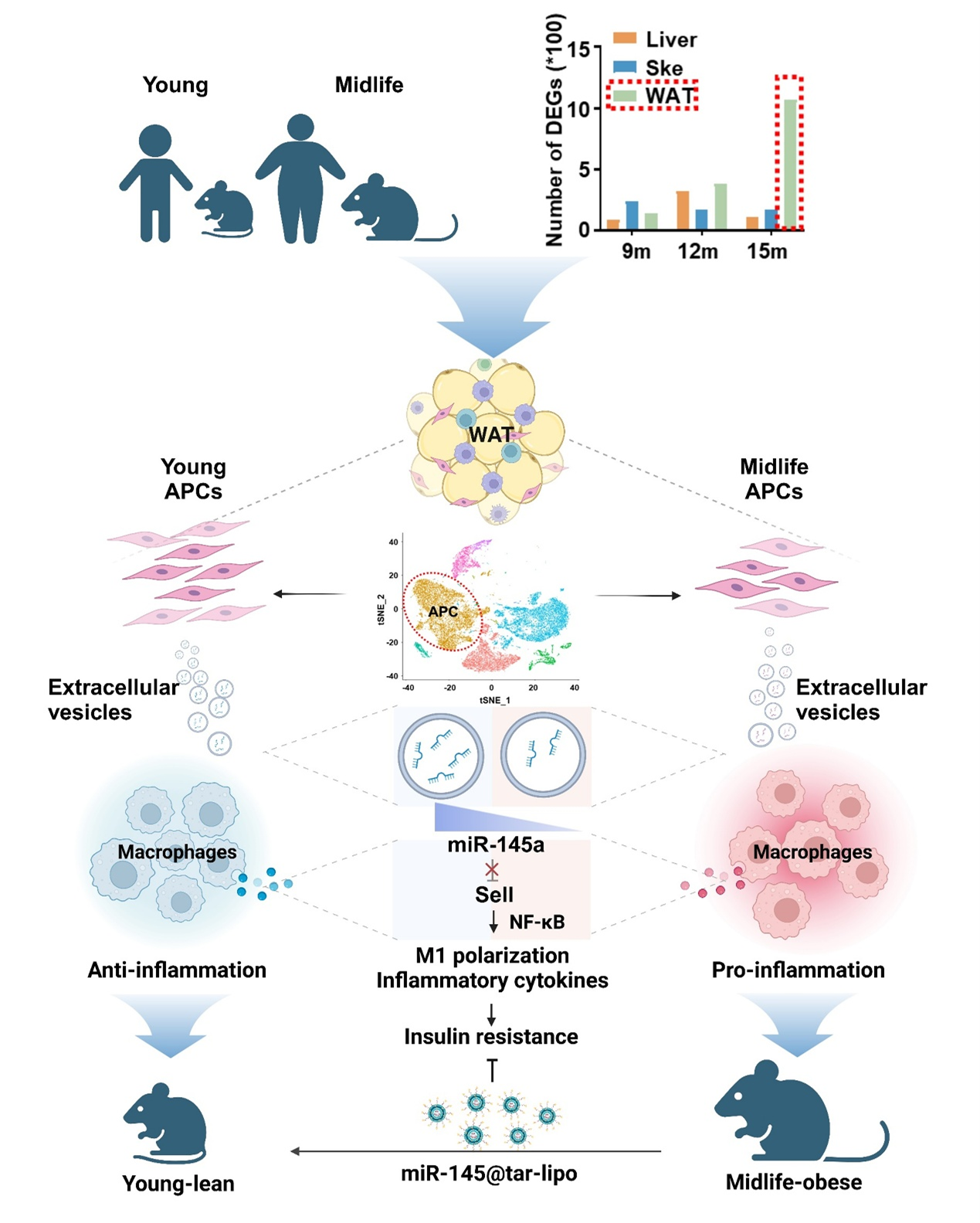
图6:miR-145在APC来源的细胞外囊泡中调控中年肥胖的模式图
参考文献:
Adipose progenitor cell-derived extracellular vesicles suppress macrophage M1 program to alleviate midlife obesity. Nat Commun 2025. DOI: 10.1038/s41467-025-57444-y.
外泌体资讯网 Nat Commun|华中科技大学王从义教授团队:脂肪祖细胞来源的细胞外囊泡通过抑制巨噬细胞M1极化缓解中年肥胖