糖尿病皮肤缺损由于其长期高血糖导致微血管基底膜增厚,内皮细胞功能受损导致血管灌注困难,造成局部缺氧微环境导致组织修复困难,是糖尿病最严重且治疗费用最高的慢性并发症之一。胞外囊泡(EVs)在血管生成和组织修复中具有重要调控作用,为糖尿病皮肤缺损治疗提供了新思路。
近期,上海交通大学医学院附属第九人民医院王旭东教授、赵灿灿助理研究员在Materials Today Bio杂志上发表了题为"PTEN/PI3K/AKT pathway activation with hypoxia-induced human umbilical vein endothelial cell exosome for angiogenesis-based diabetic skin reconstruction"的研究论文(2025 Mar 11;32:101651.)。该研究系统探讨了低氧条件下HUVEC来源外泌体的促血管生成机制,重点阐明了其通过PTEN/PI3K/AKT信号通路激活促进糖尿病皮肤血管新生和组织再生的分子机理。研究者通过体内外实验证实,低氧预处理可显著增强HUVEC外泌体的促血管生成能力,这种增强效应与PTEN/PI3K/AKT信号通路的激活密切相关。第一作者是上海交通大学医学院附属第九人民医院李臻明、吴昊和白宇昊。
糖尿病作为一种快速增长的慢性代谢性疾病,其高血糖状态会导致严重的健康风险和并发症。其中,伤口愈合障碍是糖尿病患者的重大临床挑战,约25%的糖尿病患者受此困扰,造成沉重的经济和心理负担。伤口愈合是一个包含止血、炎症、增殖和重塑四个阶段的复杂过程,而糖尿病伤口由于血管新生受损,表现出血管分布减少和毛细血管密度降低,导致伤口闭合显著延迟。
外泌体是直径70-150nm的天然亚细胞囊泡,几乎由所有细胞类型分泌,富含蛋白质、核酸、脂质和代谢物,在促进组织再生方面展现出巨大潜力,其内容物会受到来源细胞所处条件的影响而发生改变。人脐静脉内皮细胞(HUVECs)作为血管生成的关键参与者,在组织修复过程中发挥着至关重要的作用,其分泌的外泌体在促进血管新生方面或许也具有独特优势和潜在的应用前景。该研究开展了低氧诱导的HUVECs来源外泌体 (Hp-Exo)功能化的GelMa水凝胶用于糖尿病皮肤伤口治疗。将HUVECs培养在低氧环境下,其获取的外泌体内容物缺氧诱导因子-1α(HIF-1α)发生显著富集,进而增强其血管新生功能;糖尿病小鼠伤口模型也进一步证实了Hp-Exo通过促血管生成实现对皮肤伤口的加速治疗。该研究也揭示了miRNAs通过PI3K/AKT通路在调控伤口愈合中的重要作用。该研究有望为提供新的思路和依据。
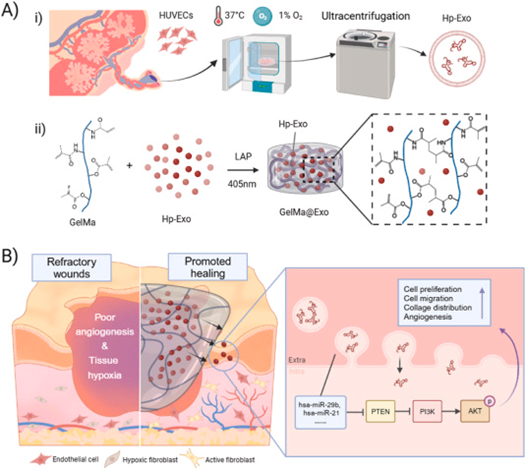
图1. 研究思路图
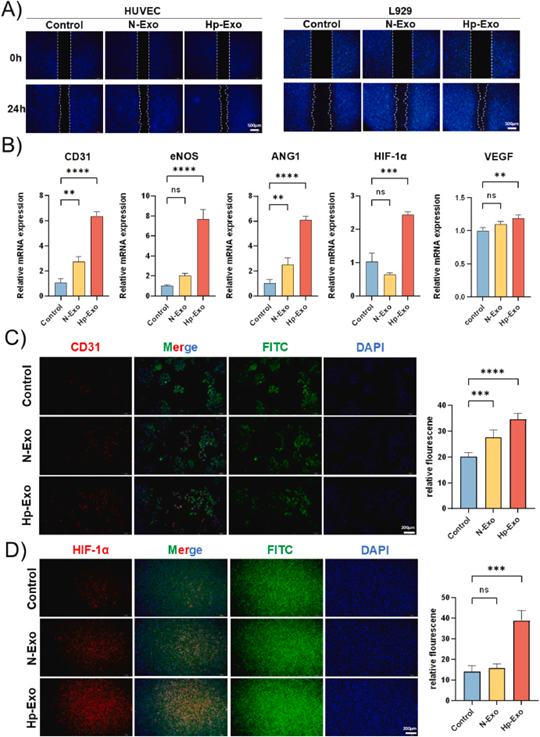
图2. 细胞划痕实验、Transwell实验以及血管形成实验发现Hp-Exo能显著促进细胞迁移以及体外血管形成。进一步qRT-PCR检测发现Hp-Exo显著上调PECAM-1/CD31、eNOS、ANG1、HIF-1α和VEGF等血管生成相关标志物的表达,表明Hp-Exo通过调控这些关键因子增强内皮细胞功能。
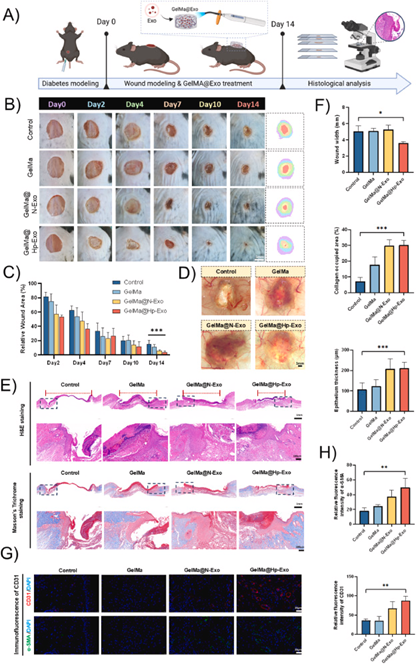
图3. 构建糖尿病型小鼠全层皮肤缺损模型,评估了负载低氧预处理外泌体(Hp-Exo)的GelMa水凝胶(GelMa@Hp-Exo)对糖尿病伤口愈合的治疗效果。结果显示,GelMa@Hp-Exo组上皮层增厚、胶原沉积更有序,血管标志物CD31和平滑肌标志物α-SMA表达显著上调。最终表明,GelMa@Hp-Exo通过增强血管生成显著促进糖尿病伤口愈合。
参考文献:
PTEN/PI3K/AKT pathway activation with hypoxia-induced human umbilical vein endothelial cell exosome for angiogenesis-based diabetic skin reconstruction. Mater Today Bio. 2025 Mar 11; 32: 101651.
外泌体资讯网 Materials Today Bio|上海交大医学院附属九院王旭东/赵灿灿:缺氧诱导HUVEC外泌体促糖尿病皮肤重建的血管生成