复杂的生物过程通常通过多类大分子自组装而成的纳米结构进行,例如核糖体(蛋白质和RNA)或包膜病毒(蛋白质、核酸和脂质)。针对核酸或蛋白质的自组装结构设计已经开发出了很多方法,但是用于工程化杂交生物材料的策略才开始出现。来自美国犹他大学的研究人员在最新的Nature上发表文章报道了自组装蛋白质纳米笼(nanocages)的设计,它们以一种类似于一些病毒的方式从人类细胞释放到小囊泡中。研究人员将这种生物材料称为“包膜蛋白纳米笼”(EPNs)。EPN的生物发生需要三个不同功能的蛋白质序列元件:膜结合、自组装和转运所需的内体分选复合物(ESCRT)。具有这些功能元件的各种合成蛋白诱导EPN的形成,突出了设计策略的模块性和普适性。生物化学分析和冷冻电子显微镜显示,编号为EPN-01的设计,由含有多个蛋白质纳米笼的小(〜100 nm)囊泡组成, 与60亚基自组装支架结构的设计十分匹配。掺入水泡性口炎病毒糖蛋白(VSV-G)的EPNs可以与靶细胞融合并递送其内容物,从而将货物从一个细胞转移到另一个细胞。这些结果表明蛋白质如何被编程以指导杂交生物材料的形成,并执行复杂的任务,建立EPNs作为一类设计的、模块化的,遗传编码的纳米材料,可以在细胞之间转移分子。该方法在药物递送方面有很重要的应用前景。
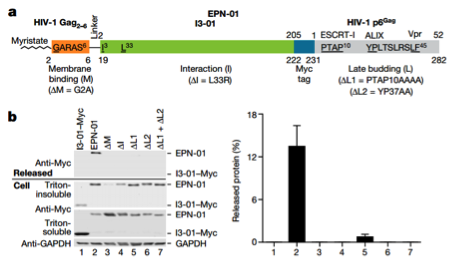
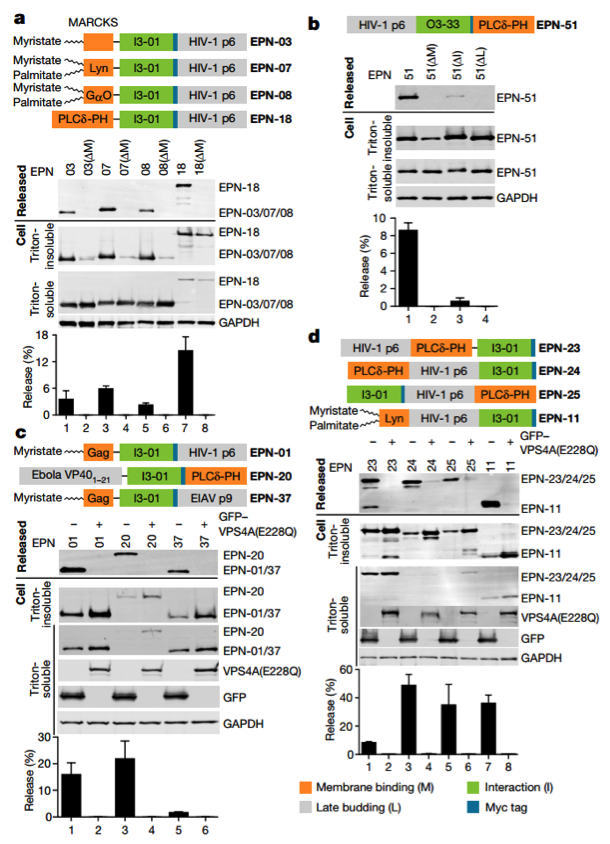
图1 | EPN的释放需要这三种功能元件(可以看到这里需要TSG101/ESCRT-I-, ALIX-结合位点,而TSG101/ESCRT-I, ALIX与外泌体的形成密切相关)
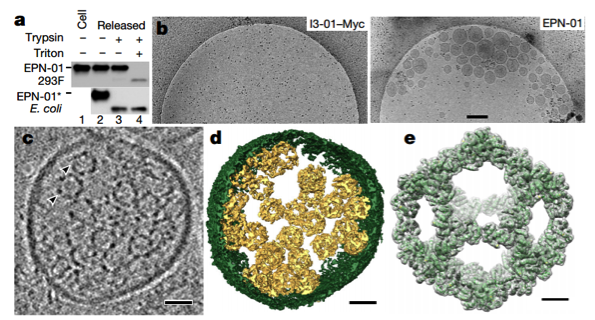
图2 | EPNs是由细胞来源的膜包被的,其中包含多个蛋白纳米笼。b\c\d图都是小膜泡包被着很多个蛋白纳米笼,e图是蛋白纳米笼的三维重构图(Scale bars, 300 nm (b), 25 nm (c, d) and 5 nm (e))
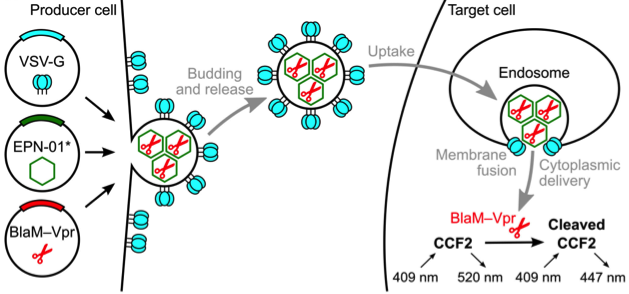
图3 | EPNs可包装大分子并将它们传递到靶细胞(Scale bar, 25 nm)
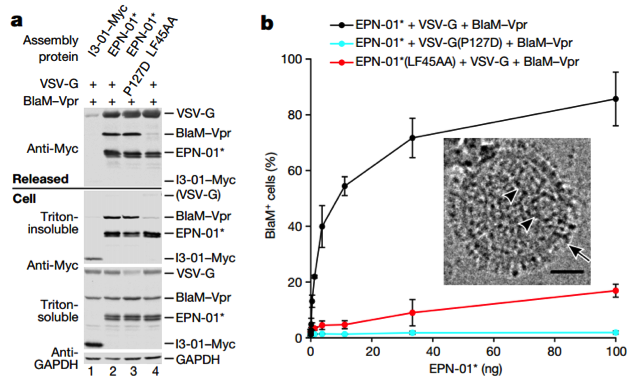
图4 | 多种功能元件和蛋白结构参与了EPN的形成
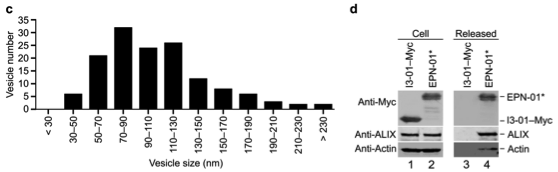
从图二可以看出该研究所设计的蛋白nanocages大概20-30 nm大小,它们是包被在一个小膜泡中的,每个小膜泡中可包含有很多个蛋白nanocages。这些小膜泡大概多大呢?补充材料中有答案,如下图左侧。大概50-150 nm的大小,基本符合外泌体的大小,而且从下图右侧可以看出这些小膜泡表达外泌体的标志蛋白ALIX。但是该文并没有说这些小膜泡就是外泌体。
参考文献:
Votteler, J., et al. (2016). "Designed proteins induce the formation of nanocage-containing extracellular vesicles." Nature 540(7632): 292-295. IF=38.138
版权归外泌体之家所有,欢迎转载,但请注明出处和原文链接!