背景:心源性细胞(Cardiosphere-derived cells,CDCs)会通过特异性的巨噬细胞(MΦ)极化从而为急性心肌梗死(MI)提供心脏保护作用。在本研究中,来自希德斯-西奈心脏研究所的研究人员证明CDC分泌的外泌体(CDCexo)为CDC治疗过程中的缺血后适应提供心脏保护作用。
方法:研究人员对大鼠和猪通过缺血再灌注诱导急性心梗模型,然后向冠状动脉内输注CDCexo,并且以惰性成纤维细胞外泌体(Fbexo)作为阴性对照。两天后,对梗死面积进行量化。从心脏组织或骨髓中分离巨噬细胞进行下游分析。使用RNA测序来确定巨噬细胞(MΦ)中的外泌体含量和基因表达谱的变化。
结果:再灌注后,CDCexo(而不是Fbexo)的输注降低了大鼠和猪心肌梗死模型的梗死面积。此外,CDCexo会减少梗死组织内CD68阳性的巨噬细胞的数量,并改变了巨噬细胞的极化状态,这类似于CDCs诱导巨噬细胞的作用。相对于Fbexo,CDCexo内富集了几种miRNA(包括miR-146a、miR-181b和miR-126)。对CDCexo诱导的巨噬细胞的全转录组数据的反向通路分析发现,miR-181b在CDC引起的巨噬细胞极化过程中的变化显著(p=1.3x10的-21次方),而且蛋白激酶Cδ(PKCδ)是该miRNA的下游靶点。另外,为惰性Fbexo选择性地包裹miR-181b后,也能改变巨噬细胞表型,并在大鼠心梗模型中赋予心脏保护的作用。 PKCδ抑制后的巨噬细胞的过继转移为心脏提供了保护作用。
结论:研究人员的数据验证了miR-181b从CDCs到巨噬细胞的外源转移降低PKCδ转录水平的假设,这是再灌注后CDCs的心脏保护作用的分子基础。
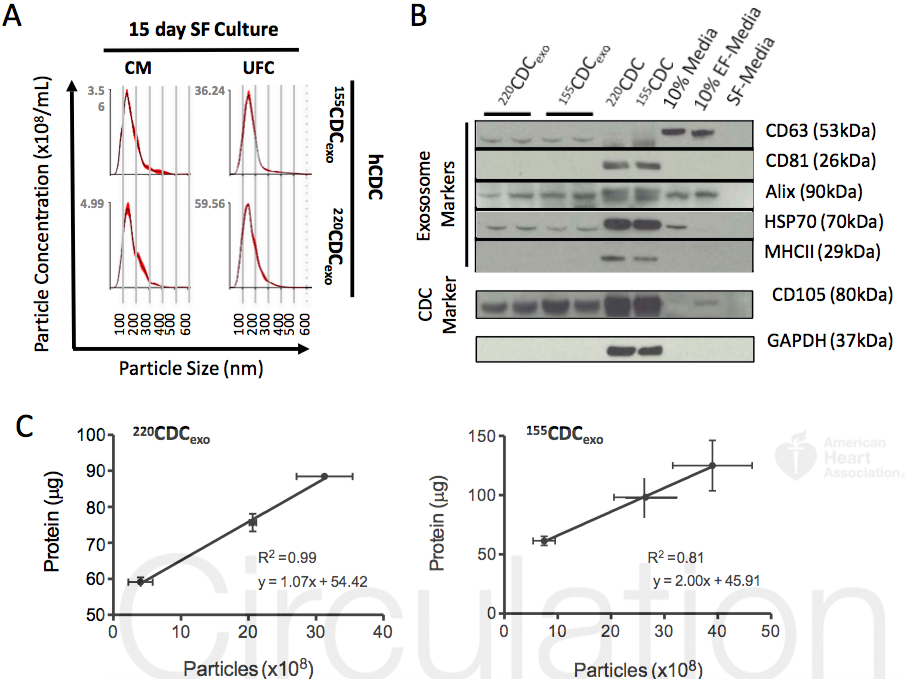
图1:CDC外泌体的提取与鉴定
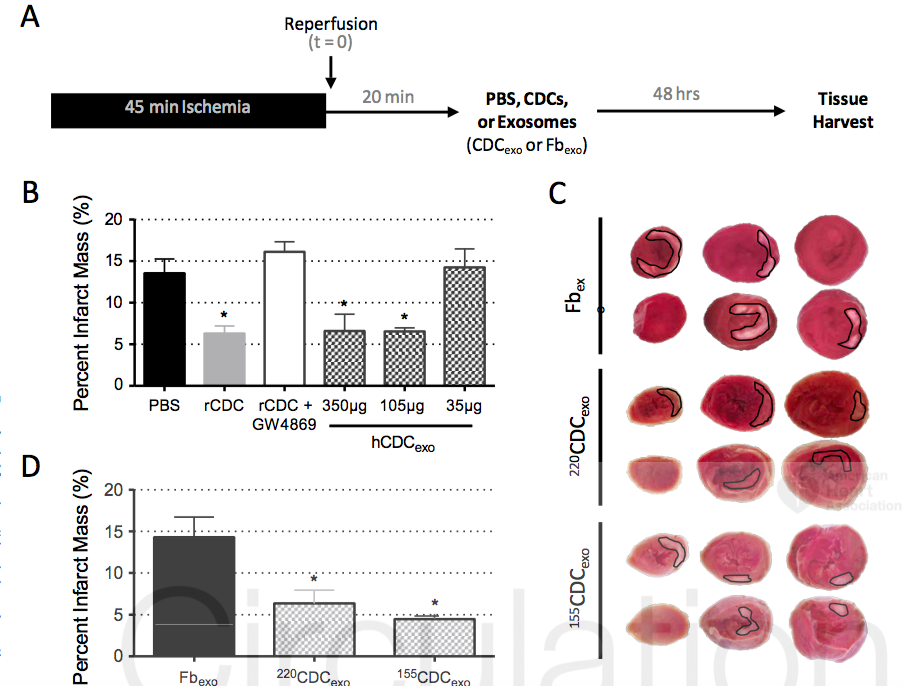
图2:向大鼠冠状动脉输注CDC外泌体能够降低再灌注后的心肌损伤
参考文献:de Couto G, Gallet R, Cambier L, Jaghatspanyan E, Makkar N, Dawkins JF, Berman BP, Marbán E. Exosomal microRNA Transfer into Macrophages Mediates Cellular
Postconditioning. Circulation. 2017 Apr 14.PubMed PMID: 28411247.(IF=17.047)