Exosomes,大家都知道,中文名外泌体,因其形态而得名,直径为30-150nm,是一种能被大多数细胞分泌的微小膜泡,人体中几乎所有类型的细胞均能产生外泌体,外泌体几乎存在于所有的组织、细胞间隙、体液中。
外泌体中含有很多组分,有MHC-1/2蛋白,也有一些蛋白、脂类也能被包裹到外泌体中,另外还有核酸,包括miRNA、DNA、lncRNA、mRNA等,在生命科学扮演者越来越重要的角色,以下是近期发表的涉及到Exosomes和小RNA相关研究的几篇文章,与大家分享一下。
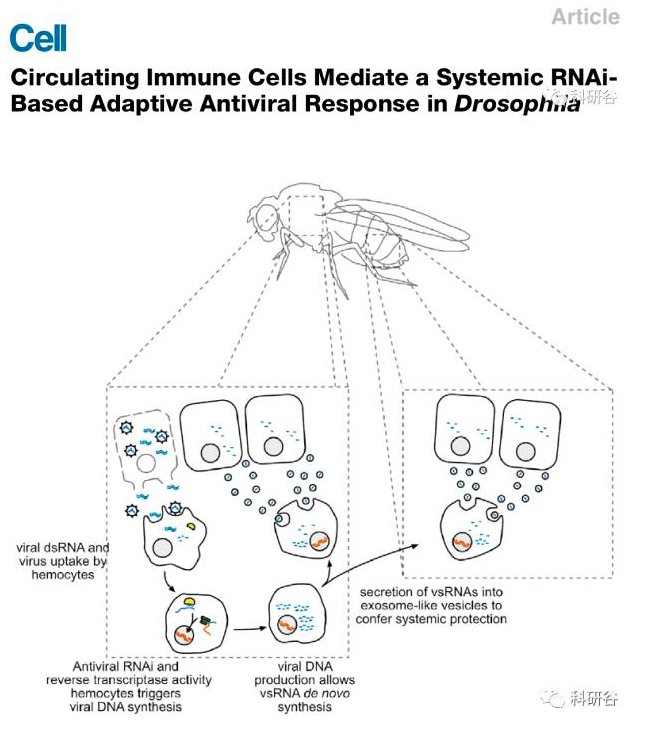
1) Circulating Immune Cells Mediate a Systemic RNAi-Based Adaptive Antiviral Response in Drosophila.Cell
关键词:外泌体;siRNA;系统免疫
综述:有效的抗病毒保护在多细胞生物体中有赖于细胞免疫、系统免疫。系统免疫介导抗病毒信号从侵染部位传递到远距离未被感染组织。在节肢动物中,抗病毒主要是靠RNAi,本文我们展示了果蝇有一个非常精细的由巨噬细胞样的血细胞介导的基于RNAi原理的系统免疫。血细胞从被感染的细胞中汲取双链RNA,通过内源的转座子反转录酶,产生了和病毒RNA互补的DNA链模板。这些DNA片段从头合成siRNA,这种siRNA由外泌体样的小囊泡包裹分泌。从被病毒感染的果蝇的血淋巴结中纯化得到了这种siRNA,而这赋予了机体被动免疫病毒的功能。类似于脊椎动物,昆虫用免疫细胞产生以稳定的互补DNA链形式的免疫记忆,这种免疫受到外泌体分泌siRNA形式的介导。
2) Exosome-Transmitted lncARSR Promotes Sunitinib Resistance in Renal Cancer by Acting as a Competing Endogenous RNA.Cancer Cell
关键词:外泌体;lncRNA;药物耐受
综述:舒尼替尼耐受在肾细胞癌 (renal cell carcinoma,RCC)的治疗中是主要挑战,所以理解这其中的机制以及开发有效的治疗策略令人期待。我们发现了一条lncRNA,lncARSR(有舒尼替尼耐受的肾细胞癌中活动频繁),和临床治疗中舒尼替尼耐受息息相关。lncARSR通过竞争性地结合miR-34/miR-449从而让AXL、c-MET在RCC细胞中表达,导致细胞对舒尼替尼耐受。另外,lncARSR 可以被外泌体所携带并转移到敏感细胞,传播舒尼替尼耐受的效应。理论上用特定的针对lncARSR的核酸序列或者AXL/C-MET抑制剂能够治疗舒尼替尼耐受的RCC细胞,因此lncARSR可以作为舒尼替尼耐受的标记物甚至作为治疗性靶标。
3) MVP-mediated exosomal sorting of miR-193a promotes colon cancer progression.Nature communication.NAT COMMUN
关键词:外泌体;miRNA;colon cancer
综述:外泌体是最近几年发现的作为细胞间交流的新媒介,但是目前外泌体的分泌对于供体细胞、受体细胞分别有何影响未见报道。我们研究了初期小鼠结肠癌、结肠癌肝转移以及正常结肠组织中外泌体miRNA组分,在疾病晚期,肿瘤抑制的miRNA会被包裹入外泌体。MiR-193a和major vault protein(MVP)有相互作用。敲除MVP会导致miR-193a在外泌体受体细胞中堆积,而不是在外泌体中,抑制肿瘤发展。然后miR-193a导致细胞周期停留在G1期,通过打靶Caprin1(可以上调Ccnd2 和c-Myc),细胞增殖也被抑制。患结肠癌晚期的病人,显示在外泌体中miR-193a有更高的水平。总之,我们的数据证明MVP介导了肿瘤抑制miRNA到外泌体中促进肿瘤的扩散。
4) Vps4A functions as a tumor suppressor by regulating the secretion and uptake of exosomal microRNAs in human hepatoma cells.Hepatology
关键词:外泌体;miRNA;结肠癌
综述:外泌体是最近几年发现的作为细胞间交流的新媒介,但是目前外泌体的分泌对于供体细胞、受体细miRNA的下调在人肝癌形成中发挥着重要作用,本文我们重点介绍外泌体参与了调控肝癌细胞中miRNA的表达谱,作为媒介调控肝癌形成。首先,我们对比了肝癌细胞和肝癌细胞外泌体中的miRNA的表达谱;再次共培养实验证明肝癌细胞外泌体能促进肝癌细胞增殖、转移、侵袭,具有向受体细胞传送miRNA的功能;再次,我们数据显示Vps4A,一个外泌体生成的关键调控蛋白,在肝癌组织中的表达是被下调的。在体外实验中显示,Vps4A抑制了肝癌的增殖,细胞团的形成、转移、侵袭。我们再次调查了Vps4A在抑制外泌体活性中的作用,发现它能减弱细胞对外泌体的敏感性。通过RNA测序,我们证明Vps4A有利于促癌miRNA从外泌体中释放,反而使得抑癌miRNA倾向于包裹进外泌体中。一组和Vps4A有关的miRNA被发现,KEGG通路分析表明(PI3K) /Akt 信号通路最有可能被这些miRNA所调控,事实上,当Vps4A过表达时,PI3K/Akt通路被抑制。结论:Vps4A可能发挥着抑癌的功能,它能够使用外泌体作为媒介调控miRNA在肝癌细胞的分泌和吸收。
外泌体资讯网 【综述速递】4篇外泌体相关的小RNA研究