细胞外囊泡起源于不同的亚细胞区间,并释放到细胞外空间。通过将其货物转移到靶细胞和组织中,它们作为邻近细胞和远端细胞间细胞间通讯的新型调节剂。因为囊泡组成和生物学内含物是细胞活化和损伤的特异性特征,因此它们作为诊断和预后生物标志物的潜力已经引起了心血管疾病的极大兴趣。循环囊泡或非泡囊结合的核酸的表征代表了用于诊断和监测心血管疾病的有价值的工具,最近称为液体活检。循环细胞外囊泡在流行病学调查中提供无创和几乎连续的疾病状态信息。最后,细胞外囊泡的基因工程和细胞特异性应用可以显示治疗心血管疾病的新型治疗选择。在这篇综述中,来自德国的研究人员总结了目前关于细胞外囊泡的知识作为诊断和预后生物标志物,以及它们在心血管疾病纵向流行病学研究中的潜在应用。
细胞外囊泡在心血管疾病中的诊断应用
EV可据其大小和释放刺激进行细分。虽然外泌体从细胞中永久地输出,但是由于细胞激活或损伤,微泡也被释放。因此,循环EV的水平在健康受试者的血浆中是可检测的,并且在患有心血管危险因素或已经存在的CVD或心肌衰竭的患者中升高。在它们的形成期间,EV装备有来自其亲本细胞的表面分子,以及选择的胞质内含物。特别地,循环囊泡或非泡囊结合核酸的表征代表了用于诊断和监测肿瘤疾病和CVD的有价值的工具,最近称为液体活检。因此,EV数量和EV成分对于用作CVD的疾病特异性生物标志物具有潜在的应用价值。
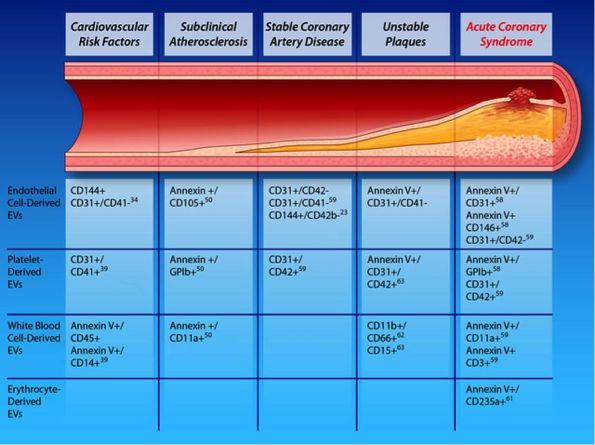
细胞外囊泡作为冠状动脉疾病不同阶段的生物标志物
细胞外囊泡在心血管疾病中的预后应用
已经显示EV将它们的生物学成分转移到受体内皮细胞、血管平滑肌细胞中,或者转移至动脉粥样硬化斑块调节血管功能和CVD进展。鉴于这些发现,可以理解,EV的循环水平已被证明与主要不良心脏事件的发生相关。
在具有高风险CAD的各种心血管危险因素的异质性患者群体中,循环CD144+内皮微泡的水平独立地预测了未来的心血管事件。根据这些发现,证明稳定的CAD和高水平的循环CD31+/annexin V+微泡的患者在6年的随访中冠心病血运重建和心血管死亡的风险更高。此外,在经典风险因子模型中添加CD31+ /annexin+微囊泡水平对预后更佳。在肺动脉高压患者中,CD62e+内皮微泡的循环水平与1年预后相关。在急性中风中,内皮微泡水平与病变体积和临床结果相关。
细胞外囊泡研究的未来方向
如果EV收集和表征方法进一步改进,EVs生物学成分的基因组和蛋白质组学分析将为临床医生提供诊断和监测CVD的整体模式。EV的组成和数量可以提供关于疾病严重程度的额外信息。关于流行病学研究,EV可能代表治疗效果的有价值的指标。通常用于CVD或某些膳食营养素的患者中的几种药物可以针对EV水平、内容物和功能,并显示心血管保护作用。EV在局部和系统地影响受体细胞功能的潜力已经激发了科学家在天然释放或人造囊泡的基础上开发药理学工程改造或转基因小泡。一旦EV吸收和系统清除的基础机制被更深入地了解,EV可以通过修改EV内容物的低表达或过表达分子来作为新疗法的潜在临床递送工具。最后,EV分类、分离和纯化需要标准化,以确保EV分析在临床环境中是可行的。
参考文献:
Jansen, F., et al. (2017)."Extracellular Vesicles in Cardiovascular Disease: Potential Applicationsin Diagnosis, Prognosis, and Epidemiology." Circ Res 120(10):1649-1657. IF=11.551
原文下载:http://www.exosome.com.cn/forum.php?mod=viewthread&tid=1587&extra=&_dsign=13c3fa33
版权所有,未经许可禁止转载。转载请联系本网站获取授权。