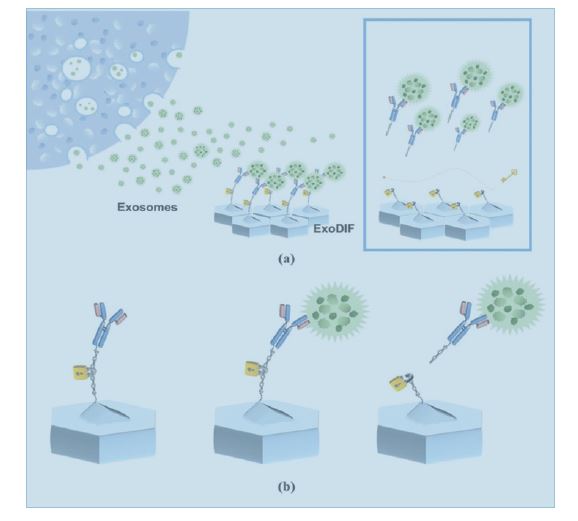
图:利用CD63抗体免疫捕获外泌体的装置原理
外泌体是一种来源于胞吐作用的细胞外囊泡(EV),由大多数细胞分泌,包括造血细胞、树突状细胞、肥大细胞、神经元、血小板、T细胞、上皮细胞、间充质细胞和癌细胞。外泌体由于游离在血液中并且含量丰富,目前受到了人们的极大的关注并被认为是最有希望的生物标志物之一。最近的研究已经阐明了外泌体不仅促进细胞间通讯,而且在癌症进展和转移中起重要作用。此外,有研究已经证明了癌细胞来源的外泌体能够改变其微环境的分子特征并建立适合癌细胞生存和转移的微环境。
与在液体活组织检测中的循环肿瘤细胞(CTC)不同,外泌体能够在不同条件下维持稳定性,这使得循环外泌体在各种领域中都能得到应用,而不会受到样品储存和样品处理的限制。尽管对其临床应用受到广泛关注,但是最好的分离外泌体的金标准方法仍然是超速离心法,其中还包括常规的样品处理和过滤步骤。然而,这个过程太耗时(一般大于10小时)费力。此外,超速离心方法提取外泌体通常得率较低(5%至25%),这有可能会由于外泌体实际量的不同从而使下游分析结果不准确,如miRNA和蛋白质分析等。目前市场上已经可以使用其他方法提取外泌体,例如基于聚合物的外泌体分离试剂盒等。然而,这些试剂盒会非特异性地沉淀下所有外泌体大小的物质,并且需要额外的聚合物去除步骤来降低分子分析过程中的杂质背景。而且试剂盒的昂贵价格也使其难以在临床中去推广。
在这项发表于Nanoscale杂志的研究中,研究人员提出了一种用于从人血液中捕获和释放循环外泌体的微流体装置。外泌体特异双重模块的免疫过滤(ExoDIF)装置由两个不同的免疫模块层组成,并且能够通过机械旋转来增强抗体和外泌体之间结合的机会,从而实现高通量特异性分离外泌体。此外,通过接头处的剪切对免疫亲和分离的外泌体进行恢复,以便于对外泌体进一步的下游分析。研究人员使用MCF-7分泌的外泌体验证了本装置的性能,发现外泌体大小囊泡的浓度和比例均高于常规外泌体分离试剂盒获得的样品。然后研究人员通过该装置从人血液样品中分离了外泌体,并比较了癌症患者和健康志愿者血液中的外泌体差异。使用电子显微镜和纳米粒子跟踪分析验证外泌体大小的囊泡时发现,癌症患者的血液外泌体水平更高,并具有更高的特异性。来自癌症患者的被捕获的外泌体中也表达有丰富的癌相关抗原,即表面上皮细胞粘附分子(EpCAM)。这种简单快速的外泌体捕获技术对阐明癌症患者外泌体的功能具有很大的潜力,因此可以应用于各种基于外泌体的癌症研究。
参考文献: Kang YT, Kim YJ, Bu J, Cho YH, Han SW, Moon BI. High-purity capture and release of circulating exosomes using an exosome-specific dual-patterned immunofiltration (ExoDIF) device. Nanoscale. 2017 Sep 1.
文献下载:http://www.exosome.com.cn/thread-1748-1-1.html?_dsign=3b8c38be