作者:企鹅
在病毒学领域中,裸病毒引起感染细胞裂解释放子代病毒。然而,最近的数据表明,小核糖核酸病毒科和肝炎病毒科的裸病毒类型也可以通过替代途径留下细胞,该途径涉及完全宿主衍生的脂质双分子层。所得到的颗粒与细胞外囊泡(EV)类似,所有细胞释放50nm-1μm囊泡。这些EV包含脂质、蛋白质和RNA,并且通常在各种(病理)生理过程中用作细胞间通讯的载体。EVs可以作为裸体病毒的携带者,并作为躲避免疫攻击的隐形斗篷。然而,病毒颗粒和宿主衍生分子的确切组合决定了这些含有病毒的EVs如何影响感染的传播、以及如何触发抗病毒免疫反应。该领域的研究不足方面是感染细胞可能释放多种类型的病毒诱导和组成性释放的EVs,其具有独特的分子组成和功能。乌得勒支大学的研究人员研究了影响裸病毒感染细胞释放EVs的病毒、细胞和环境特异因素。另外,对目前关于由不同病毒类型诱导的EVs形成和分子组成的研究结果进行比较,并将其置于广泛证实的EV群体异质性和不同EVs分离方法具有差异的背景下。EVs生物学和病毒学领域之间的密切相互作用将有助于进一步描述EVs与裸病毒之间错综复杂的关系及其与病毒生命周期和病毒感染后果的相关性。
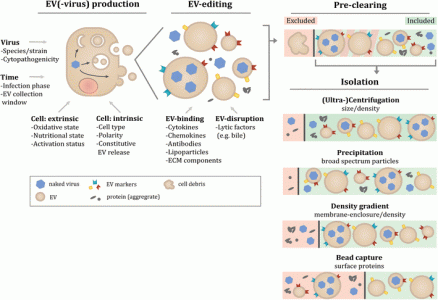
多种因素可影响EV-病毒分离物的组成成分
该图展示了EV和EV病毒领域中影响EV分子组成的因素。首先,EV(-病毒)生产本身可以根据与生产细胞有关的因素而变化,包括细胞的性质(内在因素)和其环境条件(外在因素)。感染后,这些因子以时间敏感的方式与病毒的特性聚合,以控制感染细胞产生和释放病毒粒子、EV-病毒和其他EV。其次,释放EVs的异质类群可以通过参与细胞外环境中遇到的因素进行“EV编辑”。这些因素可以结合或破坏EV膜以修饰现有的粒子。分离和纯化步骤中的差异同样会导致EV分离物组成成分的变化。这与在预清除步骤中用于去除细胞碎片和较大EVs的离心力有关,在该步骤中被去掉了或可以在后续步骤中共分离。应用于分离EV-病毒的不同技术是基于与EV的物理、亲和性或生物化学特性有关的不同原理。因此这些EV分离技术在从裸病毒体和蛋白质聚集体中分离出EV的效率不同,或者可以特定地富集某些EV亚型。
参考文献:
van der Grein SG, Defourny KAY, Slot EFJ, Nolte-‘t Hoen ENM. (2018) Intricate relationships between naked viruses and extracellular vesicles in the crosstalk between pathogen and host. Semin Immunopathol [Epub ahead of print].
外泌体资讯网 细胞外膜泡与裸病毒的复杂关系