11月份国内新出的外泌体和细胞外膜泡领域论文不完全统计有68篇。IF>10的1篇,10>IF>6的12篇,6>IF>3的31篇。本期主要内容包括:外泌体环状RNA、肿瘤相关巨噬细胞、Treg/Th17细胞、卵巢癌、结直肠癌、胃癌、鳞状细胞癌、生物传感器、Wnt、血小板反应蛋白等方面内容。内容十分丰富,不容错过。相关文章的原文都在论坛同名贴下,另有整理好的Endnote文献库,需要的请至论坛(www.exosome.com.cn)下载。
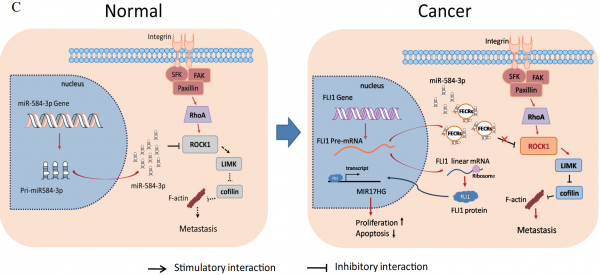
- 吉林大学第一医院肿瘤中心崔久嵬教授等:FLI1外显子环状RNA作为促进小细胞肺癌肿瘤转移的新型致癌驱动因子
Li, L., et al. (2018). "FLI1 exonic circular RNAs as a novel oncogenic driver to promote tumor metastasis in small cell lung cancer." Clin Cancer Res. IF=10.199
原发性肺癌是癌症相关死亡的主要原因之一。 小细胞肺癌(SCLC)约占所有肺癌的15%,是一种快速进展的疾病。尽管其对一线化疗有初始反应,但在大多数情况下迅速复发。SCLC的死亡率很高,特别是当患者被诊断为疾病局限期时,5年生存率仅为10%至26%。 分子疗法尽管在各种实体恶性肿瘤的治疗中取得了成功,但在SCLC中常常失败。此外,缺乏相对特异的生物标志物使得更难以管理治疗策略和评估SCLC患者的预后。因此,迫切需要关注SCLC中涉及的病理因素和特定预后生物标志物的癌症研究,以便为开发新疗法和监测SCLC的进展从而带来突破。
TP53和RB1的双等位基因失活发生在几乎所有的SCLC肿瘤中,并且这两种肿瘤抑制因子的缺失在SCLC的肿瘤发生和发展中是必需的。然而,如小鼠红细胞白血病模型所证明的,仅这些遗传病变不足以引发肿瘤形成。因此,除了TP53和RB1的缺失外,必须有一些分子调节因子在SCLC的肿瘤发生中起重要作用。最近,研究证明了FLI1在TP53和RB1缺陷的SCLC细胞和组织中异常表达,并且与恶性表型密切相关。FLI1是一种ETS转录因子家族成员,最初在F-MuLV诱导的小鼠红细胞白血病中被鉴定为致癌基因。FLI1优先在造血细胞和组织、内皮细胞和成纤维细胞中表达,并且是血液恶性肿瘤的主要驱动因子。最近,人们发现FLI1也在一些实体瘤中高表达,包括SCLC。FLI1在SCLC组织中显著上调。 FLI1癌蛋白的表达与SCLC的广泛期和过表达的Ki67有关。在高侵袭性SCLC细胞系中,FLI1的敲低促进细胞凋亡并抑制细胞增殖、肿瘤集落形成和体内致瘤性。然而,关于SCLC中FLI1异常激活的机制知之甚少。
circRNAs,作为一类新的非编码RNA,是由基因组中数千个基因的mRNA前体剪接产生的。这些circRNA主要是外显子或内含子,由背面剪接或套索内含子产生。一项研究利用Cas9引导的免疫沉淀方法来下调FLI1启动子染色质复合物并鉴定出FLI1外显子环状RNA(FECR1)的存在,其通过FLI1外显子4-2-3的反向剪接得到。值得注意的是,FECR1与顺式FLI1启动子结合并募集TET1(一种积极参与DNA去甲基化的脱甲基酶)。在乳腺癌中,FECR1作为正反馈调节剂起作用,通过协调DNA甲基化来激活FLI1。然而,FLI1环状RNA在SCLC中的作用仍然未知。
该研究发现通过CRISPR Cas9 gRNA敲除FLI1基因抑制了转移,但是FLI1的shRNA敲低不起作用,尽管在SCLC细胞中两种技术同样阻断了FLI1癌蛋白的产生。巧合的是,CRISPR gRNA被设计成靶向形成FLI1外显子环状RNA(FECR)的编码区。因此,研究假设FECR是否可能是SCLC中先前未识别的转移驱动因素。通过监测临床肿瘤组织和血清外泌体中的表达,探讨了与SCLC发病机制的关系。最后,使用SCLC体外和体内模型,研究了FECR作为肿瘤转移驱动因素的分子机制。
- 中科院遗传与发育生物学研究所所长杨维才教授等:高尔基体定位的LOT调节反式高尔基体网络生物发生和花粉管生长
Jia, P. F., et al. (2018). "Golgi-localized LOT regulates trans-Golgi network biogenesis and pollen tube growth." Proc Natl Acad Sci U S A 115(48): 12307-12312. IF=9.504
这是篇关于植物胞内囊泡的研究文章,其中涉及一些多泡小体(MVB)和分泌囊泡的内容。
- 上海交通大学新华医院汪希鹏教授:从肿瘤相关巨噬细胞释放的外泌体miRNAs诱导上皮性卵巢癌中Treg/Th17细胞失衡
Zhou, J., et al. (2018). "Exosomes Released from Tumor-Associated Macrophages Transfer miRNAs That Induce a Treg/Th17 Cell Imbalance in Epithelial Ovarian Cancer." Cancer Immunol Res. IF=9.188
该研究探究了上皮性卵巢癌(EOC)患者中Tregs和Th17细胞之间的不平衡及其临床意义。体外和体内研究均显示Tregs和Th17细胞之间的失衡导致EOC进展和转移。进一步说明了EOC的肿瘤微环境(TME)中肿瘤相关巨噬细胞(TAM)和T淋巴细胞之间的通讯。 此外,研究显示TAM衍生的外泌体转移miRNA,包括miR-29a-3p和miR-21-5p,通过直接靶向CD4+ T细胞中的STAT3协同诱导Treg/Th17细胞失衡。 该研究揭示了TAM在EOC进展中的功能机制。靶向这些外泌体或相关的miRNAs或可作为EOC治疗的治疗策略。
- 华中科技大学同济医院王桂华、胡俊波:M2巨噬细胞衍生的外泌体促进结肠癌中的细胞迁移和侵袭
Lan, J., et al. (2018). "M2 macrophage-derived exosomes promote cell migration and invasion in colon cancer." Cancer Res. IF=9.13
该研究发现M2巨噬细胞通过外泌体对结肠癌细胞的迁移和侵袭产生影响。研究证明了巨噬细胞外泌体(MDE)使BRG1显著下调。MDE包含miR-21-5p和miR-155-5p,即靶向BRG1的微小RNA。研究结果揭示了肿瘤细胞和肿瘤相关巨噬细胞(TAM)之间的新视野:特定的miRNA通过外泌体从M2巨噬细胞直接穿梭到结肠直肠癌(CRC)细胞,靶向下调BRG1表达,从而促进CRC细胞的迁移和侵袭。
- 南开大学胡献刚:来自血液的天然纳米组分抑制肺纤维化
Sun, A., et al. (2018). "Native nanodiscs from blood inhibit pulmonary fibrosis." Biomaterials 192: 51-61. IF=8.806
血液是一个用于理解和控制疾病的宝库,其成分吸引了越来越多的注意力。然而,血液的功能,特别是其在纳米级的组成,仍然在很大程度上是未知的。受外泌体和脂蛋白的启发,该工作使用多种技术分离和表征来自人血液的生物纳米“圆盘”(biotic nanodiscs from human blood, BNHB)。分离的BNHB的直径为10-30 nm,厚度约为2.9 nm。血液中的BNHB浓度达到峰值34.5+/-5.19 mg/mL(比高密度脂蛋白和外泌体高20倍)。BNHB具有高生物相容性,易于细胞内化,具有强大的肺纤维化调控能力。BNHBs是许多金属蛋白和代谢物的杂交体,含有一些类似于脂蛋白或外泌体蛋白的功能蛋白。BNHBs通过抑制α-平滑肌肌动蛋白和胶原-1蛋白的表达来抑制人胚肺成纤维细胞(HELF)中TGF-β1诱导的纤维化损伤。BNHB还强烈结合TGF-β1以抑制纤维发生中的TGF-β1活性。BNHBs成功地减少了小鼠模型中的肺部炎症和胶原沉积,阻止了肺纤维化。应用纳米“圆盘”(nanodiscs)的保护性质可能是肺部和其他疾病的新型治疗方法。
- 【综述】复旦大学上海医学院黄胜林教授等:外泌体在胰腺癌中的功能和临床意义
Qian, L., et al. (2018). "Functions and clinical implications of exosomes in pancreatic cancer." Biochim Biophys Acta Rev Cancer. IF=8.22
胰腺癌是最具侵袭性的人类恶性肿瘤之一,并且预后不良,其具有非典型症状、转移倾向和显著的化学抗性。新出现的证据表明,胰腺癌细胞衍生的外泌体(PEXs)在肿瘤发生和发展中发挥关键作用,因为它们参与抗药性、免疫逃避和代谢重编程以及胰腺癌的远处转移。它们众多差异表达和功能性成分使PEX成为有前途的筛选工具和治疗靶点,需要进一步探索。这篇综述关注PEX的功能及其在胰腺癌中的临床意义。
- 清华大学刘洋教授:Ti3C2 MXenes纳米片催化高效电化学发光生物传感器检测外泌体
Zhang, H., et al. (2019). "Ti3C2 MXenes nanosheets catalyzed highly efficient electrogenerated chemiluminescence biosensor for the detection of exosomes." Biosens Bioelectron 124-125: 184-190. IF=8.173
外泌体在抗肿瘤免疫应答、肿瘤诊断和其他过程中发挥重要作用,并且是早期癌症诊断的有希望的生物标志物。这项工作使用适体修饰的二维材料Ti3C2 MXenes纳米片作为ECL纳米探针,开发了一种灵敏的电生成化学发光(ECL)生物传感器,用于检测外泌体,具有大的表面积,优异的电导率和催化性能。通过在电极表面上修饰的EpCAM蛋白识别的适体,外泌体可以高效地捕获到电极表面上。此外,ECL纳米探针还可识别外泌体,并显著增强鲁米诺的ECL信号。基于该策略,获得了用于MCF-7外泌体检测的高灵敏度ECL生物传感器。检测限为125个颗粒/μL,比传统ELISA方法低100多倍。成功制备ECL生物传感器用于血清中的MCF-7外泌体检测。该策略为外泌体相关临床诊断中的外泌体检测提供了可行、灵敏且可靠的工具。
- 天津医科大学巴一、应国光团队:源自胃癌细胞的外泌体circRNA通过靶向miR-133/PRDM16途径促进白色脂肪褐变
Zhang, H., et al. (2018). "Exosomal circRNA derived from gastric tumor promotes white adipose browning by targeting the miR-133/PRDM16 pathway." Int J Cancer. IF=7.36
前期详细报道:https://www.exosomemed.com/5276.html(公众号插入对应公众号的推文链接)
- 台湾卫生研究院:富含层粘连蛋白γ2的口腔鳞状细胞癌细胞的细胞外囊泡通过淋巴管内皮细胞的整合素α3依赖性摄取增强体外淋巴管生成
Wang, S. H., et al. (2018). "Laminin gamma2-enriched extracellular vesicles of oral squamous cell carcinoma cells enhance in vitro lymphangiogenesis via intergrin alpha3-dependent uptake by lymphatic endothelial cells." Int J Cancer. IF=7.36
口腔鳞状细胞癌(OSCC)LN1-1细胞除了具有增强淋巴管内皮细胞(LECs)的迁移和管形成的能力之外,与其亲本OEC-M1细胞相比,显示出更大的淋巴管生成和淋巴结转移能力。通过一系列差异离心纯化并使用电子显微镜、动态光散射和蛋白质印迹进行表征,LN1-1细胞衍生的细胞外囊泡(LN1-1 EV)促进LEC迁移、管形成和LEC的摄取更多有效地比OEC-M1细胞衍生的EV(OEC-M1 EV)。在基于细胞培养/液相色谱-串联质谱的蛋白质组学平台中使用氨基酸稳定同位素标记,验证出LN1-1 EV中的高表达蛋白有:层粘连蛋白-332蛋白,包括层粘连蛋白α3、β3和γ2。临床上,在患有淋巴结转移的OSCC患者的血浆EV中检测到更高水平的层粘连蛋白-332,表明EV携带的层粘连蛋白-332作为新的和非侵入性的生物标志物检测OSCC淋巴结转移。层粘连蛋白γ2的敲低和抗层粘连蛋白-332中和抗体的抑制损害了LN1-1 EV介导的LEC迁移、管形成和LEC的摄取。重要的是,与对照EV相比,层粘连蛋白γ2缺陷型EV显示出进入淋巴结的能力降低。另外,层粘连蛋白332/γ2介导的EV摄取依赖于整联蛋白α3而不依赖于β1、β4或α6。总的来说,LECs对富含层粘连蛋白γ2的EV的摄取增强了体外淋巴管生成,因此EV携带的层粘连蛋白-332是OSCC的潜在生物标志物。
- 华中科技大学同济医学院覃吉超教授:外泌体Wnt诱导的结肠直肠癌细胞去分化有助于化疗耐药
Hu, Y. B., et al. (2018). "Exosomal Wnt-induced dedifferentiation of colorectal cancer cells contributes to chemotherapy resistance." Oncogene. IF=6.854
癌症干细胞(CSCs)固有地对化疗具有抗性,并且化疗失败的复发性肿瘤中的CSC被富集;然而,化疗诱导的CSC富集的细胞起源仍不清楚。与基质成纤维细胞的通讯可通过分泌因子诱导癌细胞去分化成CSC。最近研究证明,成纤维细胞衍生的外泌体促进结直肠癌(CRC)的化学抗性。该研究报告成纤维细胞通过外泌体诱导的大量CRC细胞重编程(去分化)赋予表型和功能性CSC的CRC化学抗性。在分子水平上,提供了证据表明成纤维细胞外泌体中的主要重编程调节剂是Wnt。发现外泌体Wnt增加分化的CRC细胞中的Wnt活性和药物抗性,并且抑制Wnt释放在体外和体内减弱了这种作用。总之,结果表明,来自成纤维细胞的外泌体Wnt可以诱导癌细胞的去分化以促进CRC中的化学抗性,并且表明干扰外泌体Wnt信号传导可以有助于改善化学敏感性和治疗窗口。
- 高雄医学大学刘博仑教授:色素上皮衍生因子通过上调外泌体血小板反应蛋白1来抑制肺癌的迁移和侵袭
Huang, W. T., et al. (2018). "Pigment epithelium-derived factor inhibits lung cancer migration and invasion by upregulating exosomal thrombospondin 1." Cancer Lett 442: 287-298. IF=6.491
外泌体涉及癌细胞发育、迁移和侵袭。色素上皮衍生因子(PEDF)是一种可以调节肺癌进展的分泌型抗癌蛋白;然而,PEDF在非小细胞肺癌(NSCLC)中的作用,包括转移和癌细胞衍生的外泌体分泌,尚不清楚。这项研究分析了PEDF对外泌体介导的NSCLC细胞的迁移、侵袭和致瘤性的影响。结果显示PEDF过表达显著降低NSCLC侵袭和迁移,同时诱导细胞聚集,而PEDF敲低具有相反的效果。与来自未处理细胞的外泌体相比,用重组PEDF处理的NSCLC细胞的外泌体具有显著降低的促进癌细胞运动性、迁移和侵袭的能力。来自PEDF处理的细胞的外泌体含有血小板反应蛋白1(THBS1),其抑制细胞骨架重塑和外泌体诱导的肺癌细胞运动、迁移和侵袭。此外,与对照肿瘤相比,PEDF过表达的NSCLC细胞形成较小的异种移植肿瘤,具有较高的THBS1表达。研究结果表明,PEDF通过调节癌细胞衍生的外泌体中THBS1释放来降低NSCLC细胞的转移潜力,从而揭示肺癌进展的新机制。
- 首都医科大学宣武医院李非教授:源自人脐带间充质干细胞的外泌体递送miR-145-5p以抑制胰腺导管腺癌进展
Ding, Y., et al. (2018). "Exosomes derived from human umbilical cord mesenchymal stromal cells deliver exogenous miR-145-5p to inhibit pancreatic ductal adenocarcinoma progression." Cancer Lett 442: 351-361. IF=6.491
前期详细报道:https://www.exosomemed.com/5285.html(公众号插入对应公众号的推文链接)
- 南京大学张辰宇、张春妮团队:特发性肾病综合征患儿的尿液外泌体microRNA特征分析
Chen, T., et al. (2018). "Increased urinary exosomal microRNAs in children with idiopathic nephrotic syndrome." EBioMedicine. IF=6.183
前期详细报道:https://www.exosomemed.com/5324.html(公众号插入对应公众号的推文链接)
- 苏州大学:外泌体生物标志物miR-454-3p在神经胶质瘤中起肿瘤抑制剂的作用
Shao, N., et al. (2018). "miR-454-3p is an exosomal biomarker and functions as a tumor suppressor in glioma." Mol Cancer Ther. IF=5.365
- 哈尔滨医科大学:心脏中miR-1的过表达通过外泌体的转运,通过SNAP-25的转录后调节减弱海马突触小泡的胞吐作用
Duan, M. J., et al. (2018). "Overexpression of miR-1 in the heart attenuates hippocampal synaptic vesicle exocytosis by the posttranscriptional regulation of SNAP-25 through the transportation of exosomes." Cell Commun Signal 16(1): 91. IF=5.324
- 兰州大学第二医院:循环外泌体miR-17通过抑制类风湿性关节炎中TGFBR II的表达抑制调节性T细胞的诱导
Wang, L., et al. (2018). "Circulating Exosomal miR-17 Inhibits the Induction of Regulatory T Cells via Suppressing TGFBR II Expression in Rheumatoid Arthritis." Cell Physiol Biochem 50(5): 1754-1763. IF=5.5
前期详细报道:https://www.exosomemed.com/5246.html(公众号插入对应公众号的推文链接)
- 陆军军医大学(第三军医大学):肿瘤分泌的外泌体miR-222通过调节P27表达和胰腺癌的再定位促进肿瘤进展
Li, Z., et al. (2018). "Tumor-Secreted Exosomal miR-222 Promotes Tumor Progression via Regulating P27 Expression and Re-Localization in Pancreatic Cancer." Cell Physiol Biochem 51(2): 610-629. IF=5.5
- 浙江大学:间充质干细胞衍生的细胞外囊泡通过miRNAs的转移影响疾病结果
Qiu, G., et al. (2018). "Mesenchymal stem cell-derived extracellular vesicles affect disease outcomes via transfer of microRNAs." Stem Cell Res Ther 9(1): 320. IF=4.963
- 上海交通大学九院:成熟软骨细胞的外泌体促进软骨祖细胞的皮下稳定异位软骨形成
Chen, Y., et al. (2018). "Exosomes derived from mature chondrocytes facilitate subcutaneous stable ectopic chondrogenesis of cartilage progenitor cells." Stem Cell Res Ther 9(1): 318. IF=4.963
前期详细报道:https://www.exosomemed.com/5336.html(公众号插入对应公众号的推文链接)
- 【综述】南京医科大学金陵医院:外泌体在肝细胞癌中新兴作用的最新进展
Abudoureyimu, M., et al. (2018). "Recent progress in the emerging role of exosome in hepatocellular carcinoma." Cell Prolif: e12541. IF=4.936
- 【综述】山东省医学科学院:肿瘤来源的外泌体蛋白作为非小细胞肺癌的诊断生物标志物
Niu, L., et al. (2018). "Tumor-derived exosomal proteins as diagnostic biomarkers in non-small cell lung cancer." Cancer Sci. IF=4.372
- 中国科学技术大学:以虚假杀死真实——使用细胞外囊泡的膜包裹纳米粒子作为活性靶向药物载体消除细胞内金黄色葡萄球菌
Gao, F., et al. (2018). "Kill the Real with the Fake: Eliminate Intracellular Staphylococcus aureus Using Nanoparticle Coated with Its Extracellular Vesicle Membrane as Active-Targeting Drug Carrier." ACS Infect Dis. IF=4.325
- 山东大学第二医院:评估基于血清外泌体LncRNA的生物标志物组对膀胱癌的诊断和复发预测
Zhang, S., et al. (2018). "Evaluation of serum exosomal LncRNA-based biomarker panel for diagnosis and recurrence prediction of bladder cancer." J Cell Mol Med. IF=4.302
- 复旦大学中山医院:来自表达miR-125b的间充质干细胞的外泌体通过肌球蛋白IE抑制新内膜增生
Wang, D., et al. (2018). "Exosomes from mesenchymal stem cells expressing miR-125b inhibit neointimal hyperplasia via myosin IE." J Cell Mol Med. IF=4.302
- 【综述】上海交通大学六院:细胞外囊泡——昼夜节律同步的潜在参与者
Tao, S. C. and S. C. Guo (2018). "Extracellular Vesicles: Potential Participants in Circadian Rhythm Synchronization." Int J Biol Sci 14(12): 1610-1620. IF=4.057
- 中南大学第二湘雅医院:外泌体传播的LINC00461通过调节microRNA/BCL-2表达促进多发性骨髓瘤细胞增殖并抑制细胞凋亡
Deng, M., et al. (2018). "Exosome-transmitted LINC00461 promotes multiple myeloma cell proliferation and suppresses apoptosis by modulating microRNA/BCL-2 expression." Cytotherapy. IF=3.993
前期详细报道:https://www.exosomemed.com/5298.html(公众号插入对应公众号的推文链接)
- 复旦大学附属浦东医院:hMSC衍生的EVs传递miR-21和miR-19b可调节脊髓损伤患者神经细胞的凋亡和分化
Xu, G., et al. (2018). "miR-21 and miR-19b delivered by hMSC-derived EVs regulate the apoptosis and differentiation of neurons in patients with spinal cord injury." J Cell Physiol. IF=3.923
- 潍坊医科大学:MiRNA-548c-5p通过靶向PTPRO下调先兆子痫中的炎症反应
Wang, Z., et al. (2018). "MiRNA-548c-5p downregulates inflammatory response in preeclampsia via targeting PTPRO." J Cell Physiol. IF=3.923
- 福建医科大学附属协和医院:源自急性髓性白血病细胞的外泌体通过增强糖酵解介导的血管重塑来促进化学抗性
Wang, B., et al. (2018). "Exosomes derived from acute myeloid leukemia cells promote chemoresistance by enhancing glycolysis-mediated vascular remodeling." J Cell Physiol. IF=3.923
- 郑州大学:暴露于粉尘中的工人静脉血中外泌体let-7a-5p的下调有助于肺癌的发展
Zhang, L., et al. (2018). "Downregulation of exosomal let-7a-5p in dust exposed- workers contributes to lung cancer development." Respir Res 19(1): 235. IF=3.751
- 南方医科大学:外泌体miRNA表达谱在人肺癌细胞系上皮间质转化中的变化
Tang, Y. T., et al. (2018). "Alterations in exosomal miRNA profile upon epithelial-mesenchymal transition in human lung cancer cell lines." BMC Genomics 19(1): 802. IF=3.73
- 四川农业大学:泌乳期间'乳'中外泌体microRNA表达谱的探究
Ma, Y., et al. (2018). "Exploration of exosomal microRNA expression profiles in pigeon 'Milk' during the lactation period." BMC Genomics 19(1): 828. IF=3.73
- 福建医科大学肿瘤医院:衍生自rAAV/AFP转染的树突细胞的外泌体引发针对肝细胞癌的特异性T细胞介导的免疫应答
Li, J., et al. (2018). "Exosomes derived from rAAV/AFP-transfected dendritic cells elicit specific T cell-mediated immune responses against hepatocellular carcinoma." Cancer Manag Res 10: 4945-4957. IF=3.702
- 南方医科大学南方医院:LPS诱导的巨噬细胞衍生的外泌体的蛋白质组学分析表明它们参与急性肝损伤
Wang, G., et al. (2018). "Proteomic profiling of LPS-induced macrophage derived exosomes indicates their involvement in acute liver injury." Proteomics: e1800274. IF=3.532
- 中国医科大学第一附属医院:MicroRNA-21过表达促进间充质干细胞治疗脑出血的神经保护作用
Zhang, H., et al. (2018). "MicroRNA-21 Overexpression Promotes the Neuroprotective Efficacy of Mesenchymal Stem Cells for Treatment of Intracerebral Hemorrhage." Front Neurol 9: 931. IF=3.508
- 山东大学齐鲁医院:由子宫内膜异位症外泌体激活的巨噬细胞有助于小鼠病变的发展
Sun, H., et al. (2018). "Macrophages alternatively activated by endometriosis-exosomes contribute to the development of lesions in mice." Mol Hum Reprod. IF=3.449
- 北京协和医科大学:自分泌分泌物在NSCLC细胞中以外泌体依赖性方式增强放射抗性
Wang, S., et al. (2019). "Autocrine secretions enhance radioresistance in an exosomeindependent manner in NSCLC cells." Int J Oncol 54(1): 229-238. IF=3.333
- 福建医科大学漳州附属医院:AHIF通过外泌体促进胶质母细胞瘤进展和放射抗性
Dai, X., et al. (2019). "AHIF promotes glioblastoma progression and radioresistance via exosomes." Int J Oncol 54(1): 261-270. IF=3.333
- 四川大学华西医院:CXCL12通路在结直肠癌肺转移中的作用
Wang, M., et al. (2018). "The Role of CXCL12 Axis in Lung Metastasis of Colorectal Cancer." J Cancer 9(21): 3898-3903. IF=3.249
- 首都医科大学北京友谊医院:VEGFR-2抑制剂阿帕替尼阻碍辐射胃癌细胞外泌体引发的内皮细胞进展
Li, G., et al. (2018). "VEGFR-2 Inhibitor Apatinib Hinders Endothelial Cells Progression Triggered by Irradiated Gastric Cancer Cells-derived Exosomes." J Cancer 9(21): 4049-4057. IF=3.249
- 中南大学第三湘雅医院:间充质干细胞旁分泌作用是糖尿病肾病的一种新型治疗策略
Li, H., et al. (2018). "Paracrine effect of mesenchymal stem cell as a novel therapeutic strategy for diabetic nephropathy." Life Sci 215: 113-118. IF=3.234
- 东南大学中大医院刘必成教授:单核细胞衍生的组织因子阳性微粒的释放有助于特发性膜性肾病中的高凝状态
Wang, G. H., et al. (2018). "The Release of Monocyte-Derived Tissue Factor-Positive Microparticles Contributes to a Hypercoagulable State in Idiopathic Membranous Nephropathy." J Atheroscler Thromb. IF=3.042
- 武汉大学人民医院:乳腺癌释放的外泌体引发癌症相关的恶病质以促进肿瘤进展
Wu, Q., et al. (2018). "Breast cancer-released exosomes trigger cancer-associated cachexia to promote tumour progression." Adipocyte. IF=3.029
- 【综述】中国科学院近代物理研究所:外泌体作为临床应用的药物载体
Di, C., et al. (2018). "Exosomes as drug carriers for clinical application." Artif Cells Nanomed Biotechnol: 1-7. IF=3.026
其余文献可至论坛(www.exosome.com.cn)下载本期文献库
2018年11月份国内外泌体领域的进展整理到此结束。希望大家有所收获。下个月见!
外泌体资讯网 国内外泌体领域进展总结(2018年11月)