作者:企鹅
近期的Nature Biomedical Engineering杂志在线发表了国家纳米科学中心孙佳姝教授团队开发的最新技术平台。该团队开发了一种简单而廉价(成本约为1美元)的基于外泌体的液体活检癌症筛查方法,该方法只需极少量的血清(1微升,是通常采血量的几千分之一)即可检测其中的细胞外囊泡(EVs),可在3小时内对6种癌症进行早期筛查,并区分不同的癌症类型。
癌症诊断和分类需综合考察成像和肿瘤组织的组织病理学检查的结果。尽管是目前的金标准,但这些方法是侵入性的,卵巢和肺等器官的病变风险增加,早期癌症常常难以检测出,在资源有限的环境中难以负担。相比之下,基于血液的液体活组织检查可以提供非侵入性和灵敏性的方法,通过对循环的生物标志物(例如循环的肿瘤DNA、循环蛋白、血小板等)进行取样,在相对早期阶段对癌症类型进行分类。例如,名为CancerSEEK的血液测试利用针对无细胞DNA和循环蛋白的组合测定,使用>7.5 mL血浆检测8种常见阶段I-III癌症类型。基于肿瘤“教育”的血小板(TEP)的液体活检通过对从6 mL全血中分离的TEP进行RNA测序,能够区分六种肿瘤类型。尽管液体活组织检查能够用于多类癌症诊断,但这些方法成本高昂(每个人500美元),并且需要专门的生化实验室来进行复杂的检测。此外,需要高技能人员来解读大量的分析信息。虽然血流中循环肿瘤细胞的分析通常被称为液体活检,但由于其极端罕见和异质的基因型和表型,循环肿瘤细胞尚未用于多类癌症分类。因此,非常需要寻找具有区分早期癌症类型能力的易于操作且具有成本效益的液体活组织检查新循环生物标记物。
细胞外囊泡(EV),如外泌体(直径30-150 nm)和微泡(直径200-1,000 nm),是包裹有来自亲代肿瘤细胞特征分子的脂质双层膜囊泡(包括膜和细胞内蛋白质、核酸和脂质)。肿瘤衍生的EVs已被作为癌症患者中液体活组织检查有希望的生物标志物,其优点归因于它们的高浓度(高达1011/mL)和血液循环中的稳定性。值得注意的是,已经在来自血液样品的EVs中鉴定了许多肿瘤相关蛋白质生物标志物,并且它们的类型和表达水平与某些癌症类别(例如,结肠直肠癌、胰腺癌和卵巢癌)的存在和进展密切相关。然而,目前用于EV分析的方法通常需要耗时的超速离心用于纯化和浓缩、昂贵的抗体和用于标记和检测的广泛程序,以及用于足够灵敏度和可重复性的大样品体积,这阻碍了EVs用于癌症诊断的临床效用。此外,没有基于EV的血液检测用于区分不同的癌症类型。临床上可行和负担得起的EV测定的开发可以显著改善癌症的常规诊断。
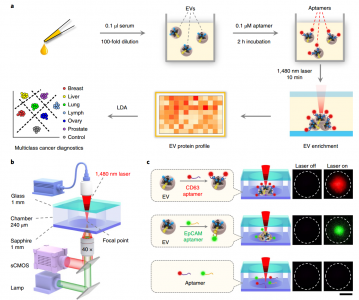
来自国家纳米中心的孙佳姝教授课题组在近期的Nature Biomedical Engineering杂志上发表文章,报道了一个热泳适体传感器(thermophoretic aptasensor, TAS),用于富集与适体共轭的EVs,可从极少量血清中检测肿瘤来源的EVs进行癌症检测。适体结合的EVs在积累时产生放大的荧光信号,其强度与EV的靶表面蛋白的表达水平相关。使用一组7个适体,该研究获得了232个血清样品(包括I-IV期淋巴瘤、乳腺癌、肝癌、肺癌、卵巢癌和前列腺癌的患者以及健康对照)中EVs的表面蛋白质谱。随后将线性判别分析(linear discriminant analysis, LDA)算法应用于六种癌症类型的自动癌症分类。EVs的7个单独标记物的未加权总和(SUM特征)用于区分前列腺癌和良性疾病,并监测根治性前列腺切除术后的生化复发。总的来说,这项工作建立了一个低成本的血液测试,以分析血清中的EV表面蛋白质,这可能潜在地转化为癌症诊断的标准临床实践。
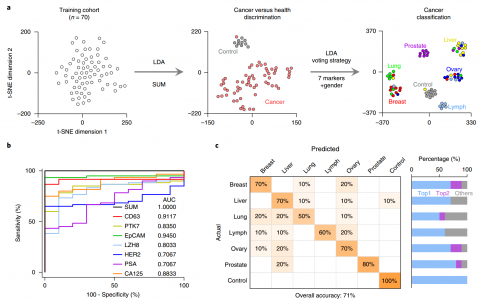
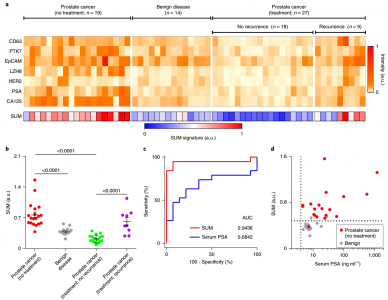
在一组102名患者中,包括I-IV期的6种癌症类型,该检测检测到I期癌症的敏感性为95%(95%置信区间(CI):74-100%)和100%特异性(95% CI:80-100%),并将癌症类型分类,总体准确度为68%(95%CI:59-77%)。对于接受前列腺活检的患者,该检测方法优于前列腺特异性抗原水平分析(曲线下面积:0.94对0.68;33例患者),用于区分前列腺癌和良性前列腺肿大,以及评估根治性前列腺切除术后生化癌症复发。该测定廉价、快速,并且需要少量的血清体积(<1 μL),并且如果在更大的群组中验证可以促进癌症筛查、分类和监测。
用于分析EV表面蛋白质的热泳适体传感器(TAS)示意图
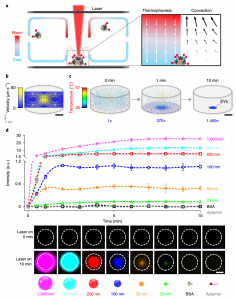
热泳聚集的表征
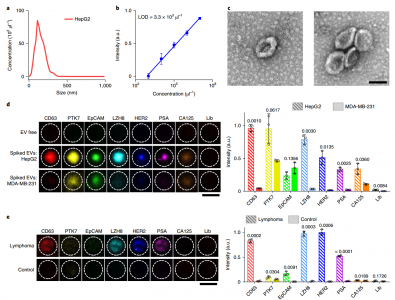
表征TAS以分析EVs的表面蛋白质
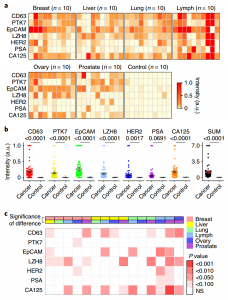
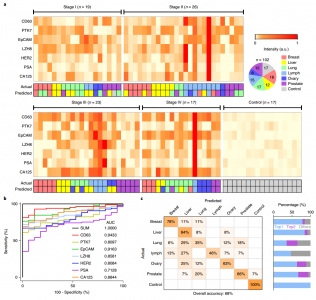
TAS通过TAS测量的癌症患者的EV表面蛋白质谱
通过EV表面蛋白质谱实现的多类癌症诊断
在验证性试验中检测和分类癌症
基于EV的前列腺癌液体活检
该研究展示了一种灵敏且低成本的TAS,用于直接在血清样品中分析EV的表面蛋白质。使用适体识别EV表面蛋白,因为它们具有与抗体相当的特异性和亲和力,合成简单、成本低、小批量可变更和血清中良好稳定性的优点。在用适体标记后,TAS可以以尺寸依赖性方式热力学富集EVs超过103倍,而游离适体和小蛋白质保持随机分布。从而原位获得仅来自适体结合的EVs的扩增荧光信号,而不需要预先分离和纯化EVs。TAS需要不到3小时,在一个血清样品中检测七种EVs蛋白标记物的成本约为1美元,为外泌体临床转化提供了前所未有的潜力。
参考文献:
Chao Liu, Junxiang Zhao, Fei Tian, Lili Cai, Wei Zhang, Qiang Feng, Jianqiao Chang, Fangning Wan, Yunjie Yang, Bo Dai, Yulong Cong, Baoquan Ding, Jiashu Sun & Weihong Tan. Low-cost thermophoretic profiling of extracellular-vesicle surface proteins for the early detection and classification of cancers. Nature Biomedical Engineering (2019) https://doi.org/10.1038/s41551-018-0343-6