土豆
胰岛素抗性是老年人群中发生II型糖尿病的主要病理特征,然而与衰老相关的胰岛素抗性的深层机制仍不清楚。在这项发表于ACS Nano杂志(IF 13.709)上的一项研究中,中南大学湘雅医院内分泌科罗湘杭课题组的研究人员发现骨髓间充质干细胞分泌外泌体中的miR-29b-3p调节着衰老相关胰岛素抗性,可能将会是治疗衰老相关胰岛素抗性的新靶点。
目前,老年人群中II型糖尿病的发病率急剧上升,约25%的老年人符合II型糖尿病的诊断标准。II型糖尿病通常表现为胰岛素抗性现象,其发病与年龄增长之间存在明显的关联性。但是,这里的潜在发生机制尚未得到充分研究。
骨骼具有许多功能,包括支撑躯体、保护我们的内脏免受伤害、参与造血功能等。最近研究表明,骨骼还可以作为一种内分泌器官,系统地调节全身新陈代谢。成纤维细胞生长因子23(fibroblast growth factor 23,FGF23)主要由骨细胞或成骨细胞分泌,是慢性肾病患者胰岛素抗性的预测因子之一。骨钙蛋白是一种由成骨细胞合成的蛋白质,在调节全身葡萄糖和能量稳态中发挥的重要作用。研究显示成骨细胞衍生的脂质运载蛋白-2(lipocalin-2,LCN2)通过与下丘脑中的黑皮质素4受体(melanocortin 4 receptor,MC4R)结合来调节食欲。此外据报道,骨骼中的骨髓间充质干细胞(bone marrow mesenchymal stem cells,BM-MSCs)在肝脏损伤、神经节细胞存活和神经胶质细胞损伤中发挥作用。然而,BM-MSCs是否也参与衰老相关的胰岛素抗性的调节仍然是未知的。
外泌体是由多种细胞或组织释放的小细胞外囊泡,是细胞间通讯的重要介质。外泌体通过递送效应物(如蛋白质、mRNA或microRNA)调节受体细胞或组织的功能。MSCs产生的外泌体数量高于其他细胞类型,比如成肌细胞、急性白血病单核细胞或胚胎肾细胞。另一方面,代谢组织中的miRNA在调节葡萄糖稳态中起着至关重要的作用。因此,研究人员提出设想,BM-MSCs是否参与通过外泌体miRNA调节与衰老相关的胰岛素抗性。
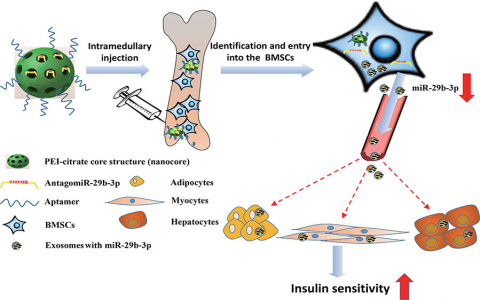
该研究结果表明,BM-MSCs衍生的外泌体可分别被脂肪细胞、肌细胞和肝细胞摄取,从而产生胰岛素抗性。使用miRNA芯片分析发现, miR-29b-3p在老年小鼠BM-MSC释放的外泌体中显著增加。机制上,SIRT1(sirtuin 1)被鉴定是外泌体miR-29b-3p的下游靶标,调节胰岛素抗性。通过纳米复合物递送系统,下调BM-MSC衍生的外泌体中miR-29b-3p的水平后显著改善了老年小鼠的胰岛素抗性。同时,BM-MSCs特异性过表达miR-29b-3p后会诱导年轻小鼠的胰岛素抗性。研究结果表明,BM-MSCs衍生的外泌体miR-29b-3p可以调节与衰老相关的胰岛素抗性,这可能成为衰老相关胰岛素抗性的潜在治疗靶点。
参考文献:Su T, Xiao Y, Xiao Y, Guo Q, Li C, Huang Y, Deng Q, Wen J, Zhou F, Luo XH. Bone Marrow Mesenchymal Stem Cells-Derived Exosomal MiR-29b-3p Regulates Aging-Associated Insulin Resistance. ACS Nano. 2019 Feb 26;13(2):2450-2462.