3月15日,国际学术期刊Journal of Hepatology在线发表了中国科学院上海巴斯德研究所龙钢课题组的研究论文“Syntenin regulates Hepatitis C virus sensitivity to neutralizing antibody by promoting E2 secretion through exosomes”。
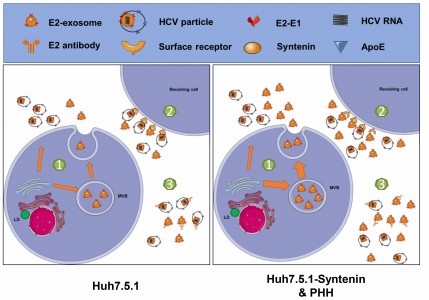
图示:syntenin在E2-外泌体释放中的调控作用。
1.syntenin高表达细胞组装生成更多的E2-外泌体;2.E2-外泌体与病毒粒子吸附于宿主细胞表面过程中有竞争关系;3.病毒中混杂的大量E2-外泌体能有效结合抵消中和抗体。
病毒在于宿主的长期协同进化中,宿主发展出多种识别病毒的机制,而病毒也反过来利用宿主自身原件和识别机制去帮助其入侵和逃逸免疫体系。近年来大量的研究集中在病毒本身如何引起宿主的防御机制以及相应的构建特定的类病毒颗粒作为疫苗刺激免疫系统产生抗体,然而有些病毒在免疫系统已经做出反应并产生抗体的情况下,正是依靠“劫持”宿主囊泡释放途径制造自身的“替身”(类病毒颗粒)以逃逸抗体的识别和杀灭。因此,利用适当的研究模型,研究可能被病原所利用的宿主囊泡释放途径,对于我们更好的理解病毒-宿主互作,以及寻找潜在的病毒感染的防控和治疗手段具有重要的研究意义。
在本项研究中,研究人员以丙型肝炎病毒(HCV)为研究模型,发现病毒膜蛋白可以通过外泌体途径释放到细胞外且该过程受到syntenin蛋白的调控。这种膜蛋白-外泌体存在并独立于HCV感染性病毒颗粒却同样可以被HCV膜蛋白特异性抗体所识别,从而帮助真正的病毒逃逸抗体的中和。进一步的研究发现血清中syntenin含量不同的HCV患者,其体内产生的血清抗体对HCV病毒的中和能力也不同,敲低人原代肝细胞中syntenin的水平后产生的子代病毒逃逸特异性抗体的能力也会降低。该研究结果揭示了syntenin在病毒利用宿主囊泡释放途径帮助自身逃逸抗体中和过程中的调控功能,为研究病毒逃逸宿主免疫系统和外泌体的包装提供了新线索。
邓力宾助理研究员为该论文的第一作者,龙钢研究员为本文通讯作者。感谢吉林大学牛俊奇教授,涂正坤教授,中科院生化细胞所何勇宁研究员和海德堡大学Bartenschlager教授的帮助。
该研究得到了科技部973项目,中科院先导和自然科学基金委等项目的支持。
全文链接:https://doi.org/10.1016/j.jhep.2019.03.006