作者:企鹅
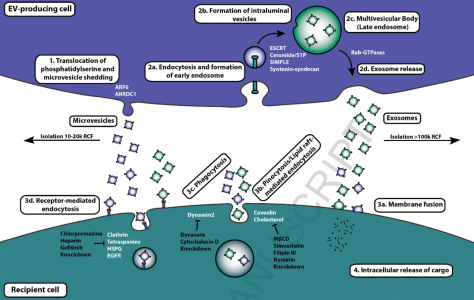
细胞外囊泡(EVs)根据其亚细胞来源的不同而具有大小和组成异质性。目前的分类将EVs分为四个不同的类别:外泌体、微泡、凋亡小体和大的oncosomes。外泌体从被称为多泡体(MVB)的内体结构中产生,是最小的EV,尺寸范围在30-120 nm之间。微泡(也称为脱落微囊泡或ectosomes)通过质膜的向外出芽产生,尺寸范围从200 nm到几微米。凋亡小体通过经历细胞凋亡的整个细胞产生的囊泡,大小在1000-5000 nm之间;而大的oncosome大小在1-10 μm之间。大的oncosomes是新发现的类别,已在癌细胞中观察到,由它们的大小和缺乏核DNA来定义的(它们可能被误认为是细胞)。凋亡小体和大的oncosomes的物理化学特性使得它们不适合作为药物递送载体。
如何使细胞外囊泡具有靶向性(或增强其靶向性)?
使用纳米颗粒进行药物递送是一种流行的策略,治疗更精确且副作用更少。可以设计诸如EV的纳米颗粒以更特异地将其货物运送到疾病部位,因此可以最小化对全身的副作用。已有研究使用了几种方法来实现EV的靶向性,这些方法可以大致分为两大类:被动和主动。
我们将被动靶向定义为EV产生细胞类型和/或EV产生细胞的操纵的策略,而不引入现有转录组的物理改变。主动靶向包括改变EV产生细胞的转录组,例如通过用重组靶向载体转染细胞。这两种方法使用不同的靶向配体和靶标。总体而言,最突出类型的靶向配体是小肽(约38%),跨膜蛋白(34%)和抗体片段(25%)也经常使用。
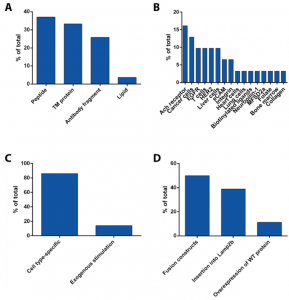
图:EV药物输送研究相关数据总结。A)使用不同类型的靶向配体数量统计:小肽、跨膜蛋白、抗体片段和脂质。B)研究中使用的不同靶标。C)按被动类型分类的研究百分比。D)使用不同的主动靶向策略数量统计。
被动型EV靶向性的策略
EV向某些组织的归巢取决于产生的细胞表型。一些研究显示EV和靶细胞之间的相互作用部分取决于EV表面上存在的特定配体。例如,从U937巨噬细胞分离的EV显示靶向内皮细胞,这是由巨噬细胞衍生的EV上的LFA-1与内皮细胞上的eCAM的相互作用介导的。研究显示这些EV有效靶向肿瘤内皮细胞并递送阿霉素以减小肿瘤大小。另一项研究采用了类似的方法,其中来自原发性胶质母细胞瘤(GBM)细胞的分离的EV显示,通过在脑内皮细胞上靶向Neuropilin-1,EV上的semaphorin 3A的存在降低了体内BBB的完整性,从而导致血管通透性增强独立。
主动型增加EV靶向性的策略
由于感兴趣的靶向蛋白可能不以足够的量表达或者甚至不能在EV中表达,因此过表达或重组表达策略可能是有帮助的。研究报道使用了三种不同的主动定位方法:1)将靶向表位插入野生型蛋白质中;2)构建融合蛋白质;3)野生型蛋白质的过表达。
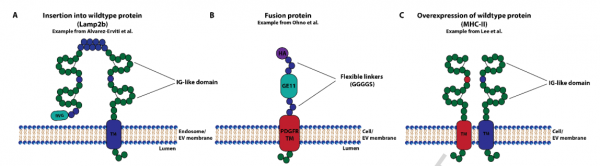
图:不同主动靶向方法的实例。A)将靶向肽插入野生型Lamp2b的N-末端部分。B)通过柔性甘氨酸-丝氨酸接头将靶向肽连接到跨膜结构域。C)未编辑的野生型蛋白质的过表达。
- 主动靶向的通常选择是将靶向表位插入野生型蛋白质中。野生型蛋白Lamp2b已被用于5项研究,这些研究均使用相同的靶向肽(狂犬病病毒糖蛋白或RVG)来靶向脑中的乙酰胆碱受体。Alvarez-Erviti等是第一个提出这种策略的,静脉内给予用抗BACE1的siRNA包装的RVG-Lamp2b EV。他们发现与对照组相比,来自治疗小鼠的脑细胞裂解物中BACE1 mRNA的敲低率高达60%。使用α-突触核蛋白作为靶标的相同靶向系统获得了类似的结果。其他人已经表明RVG与Lamp2b融合时的糖基化状态决定了它是否会在表面表达之前被切割。因此,在N-末端的不同位置引入糖基化基序增加了融合构建体的表达并保护RVG免于剪切和降解。
- 融合蛋白策略是最广泛使用的,其中仅使用表位宿主蛋白的所需结构域而不是将表位插入整个野生型蛋白中。这通常是决定其亚细胞定位的结构域,即跨膜或膜结合结构域。使用该策略,表皮生长因子(EGF)样靶向肽序列GE11与PDGFR的跨膜结构域融合,以获得注射的EV的更高的肿瘤摄取,因为EGFR在上皮肿瘤中上调。将let-7-a miRNA包装到所得的PDGFRTM-GE11 EV中,并且活性靶向和治疗性货物的组合效果在体内产生功能性摄取和体内肿瘤生长抑制。可以使用纳米抗体代替使用跨膜结构域,纳米抗体是衍生自重链抗体的小的单可变结构域。对EGFR特异的纳米抗体附着于糖基磷脂酰肌醇(GPI),从而在体外流动条件下改善所得靶向EV与EGFR表达细胞的细胞结合。梁等人通过用载脂蛋白A1和跨膜蛋白CD63的融合构建体转染HEK293T细胞来使用该策略。载脂蛋白A1是高密度脂蛋白(HDL)中的关键成分,并通过SR-B1受体介导肝细胞中HDL的货物摄取。他们用miR-26a装载外泌体并证明了HepG2细胞中外泌体的摄取,释放了miR-26a,导致细胞迁移和增殖减少。此外,两项研究通过将抗HER2 scFv融合至乳粘素的C1C2结构域并在细胞中表达构建体以产生HER2靶向的EV而使用抗HER2 scFv。然而,仍然存在与scFv的表达水平相关的问题。
- 产生靶向EV的更简单但不太流行的策略是过表达对所需靶标具有亲和力的野生型蛋白质。 从过量表达叶酸受体-α的大鼠脉络膜上皮细胞Z310中收集的EV可以通过脑室内注射后穿过血脑脊液屏障在脑实质中积累。类似地,在鼠黑色素瘤细胞B16F1中过表达MHC-II在EV中产生过表达。通过在荷瘤小鼠中皮内注射这些MHC-II阳性EV,与对照相比,它们可以抑制肿瘤生长并使存活时间延长20%。
细胞外囊泡与脂质体的比较
基于EV的药物递送的未来研究必须回答的一个主要问题是EV策略的功能性和治疗功效是否优于或可与合成的纳米载体相当。目前在基于EV的药物输送研究中选择的脂质体对照很差,因为所选择的脂质体制剂很少具有临床相关性。这意味着与脂质体(如果存在)相比,EV的优越性可能被夸大了。选择临床使用的脂质体制剂可以更好地说明两种策略之间可能存在的差异,并为构建有关EV优势的假设提供有效的基础。例如,在脂质体表面上包含PEG分子将增加系统的循环时间,这可能有益于治疗功效。众所周知,EV静脉注射时循环不良。然而,由于第二剂PEG化脂质体经常观察到抗PEG反应,因此与其合成对应物相比,EV血浆稳定性的性能可能会提高治疗效果。这表明目前可用的信息太少,希望将在不久的将来能解决这个问题。此外,这两个领域可以相互启发,以改善功能和治疗功效。
参考文献:
Gudbergsson JM, Jønsson K, Simonsen JB, Johnsen KB. Targeted extracellular vesicles for drug delivery - Considerations on methodological and biological heterogeneity. J Control Release. 2019 Jun 5. pii: S0168-3659(19)30316-5. doi: 10.1016/j.jconrel.2019.06.006. [Epub ahead of print]
外泌体资讯网 药物递送,如何提高细胞外囊泡的靶向性?