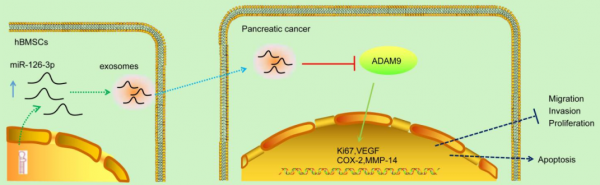
胰腺癌作为一种致命的恶性肿瘤,其有效治疗手段相对较少。近日,来自江苏师范大学郑元林、陆军课题组以及南京大学陈贵泉课题组的研究人员在Molecular Therapy-Nucleic Acids (IF=5.660)杂志上发表文章,揭示了由骨髓间充质干细胞衍生的外泌体传递的miR-126-3p在胰腺癌进展中的作用,确定miR-126-3p可作为胰腺癌治疗的分子靶点。
胰腺癌是威胁人类健康的主要癌症类型之一,目前缺乏有效的治疗和改善预后的方法。胰腺癌是癌症死亡的第四大主要原因,生存率非常低。尽管胰腺癌的治疗方法一直在改进,但在过去几十年中,胰腺癌的死亡率并没有降低,主要原因是缺乏足够的早期筛查方法和早期诊断的生物标志物。骨髓间充质干细胞(BMSC)在骨和软骨中存在,其中包含约0.001%-0.01%的骨髓有核细胞(BMNC)。骨髓间充质干细胞属于与成纤维细胞相似的非造血细胞家族,最初被认为是一种多能祖细胞。研究表明骨髓间充质干细胞可促进癌症的发展,并且有文献显示骨髓间充质干细胞具有安全性和有效性,对肌萎缩侧索硬化患者有治疗潜力。值得注意的是,骨髓间充质干细胞能够迁移到肿瘤组织,推测它们在胰腺癌中可被用作基因治疗的靶点。
外泌体是一种小的膜封闭的囊泡(30-150 nm),可以从来源细胞向受体细胞输送货物(包括蛋白质、脂质和核酸)。从间充质干细胞释放的外泌体可以将功能性RNA转移到受体细胞,这表明外泌体作为细胞疗法的应用前景。据报道,外泌体可携带microRNA(miRNA),参与肿瘤细胞的增殖、分化和凋亡。此外,miRNA可作为肿瘤抑制因子或致癌因子,在转录后层面调节基因表达。例如,miR-126-3p——miRNA的一种亚型——已被证明可作为肿瘤抑制因子,能够抑制肿瘤的进展。此外,miR-126-3p在食管鳞状细胞癌(ESCC)中的水平下调,特别是在预后不良的ESCC中。另外miR-126-3p能够抑制胰腺癌患者血液中的肿瘤细胞转移和侵袭。基于文献的探索,因此miR-126-3p可能可以作为胰腺癌的治疗靶点。先前的报道认为,miR-126-3p对去整合素和金属蛋白酶9(ADAM9)具有负向调节作用。ADAM9是I型膜锚定蛋白,在转移性肿瘤中高表达,因此ADAM9与肿瘤的发展密切相关。研究表明,miR-126对ADAM9的负向调节可以抑制胰腺细胞的恶性进展。
在本研究中,研究人员认为来自BMSCs外泌体中的miR-126-3p可通过下调ADAM9来抑制胰腺癌的进展。首先,作者筛选了一系列候选miRNA以及与胰腺癌相关的基因靶点。作者用miR-126-3p转染PANC-1细胞或者沉默ADAM9,检测了miR-126-3p和ADAM9在胰腺癌细胞中的调节作用。进一步,作者分离源自BMSC的外泌体,并与胰腺癌细胞共培养,阐明外泌体在胰腺癌中的作用。此外,作者通过慢病毒包装miR-126-3p的方式,在体内分析了BMSCs外泌体的过表达miR-126-3p对胰腺癌细胞的增殖、迁移、侵袭、凋亡、肿瘤生长和转移的影响。研究人员发现,miR-126-3p通过下调ADAM9来抑制胰腺癌进展。来自BMSCs的外泌体中的过量miR-126-3p抑制了胰腺癌细胞的增殖、侵袭和转移,并在体外和体内促进胰腺癌细胞的凋亡。因此,研究人员认为, BMSCs外泌体中的过量miR-126-3p通过下调ADAM抑制了胰腺癌的发展,突出了miR-126-3p作为胰腺癌治疗新型生物标志物的潜力。
参考文献:Wu DM, Wen X, Han XR, Wang S, Wang YJ, Shen M, Fan SH, Zhang ZF, Shan Q, Li MQ, Hu B, Lu J, Chen GQ, Zheng YL. Bone Marrow Mesenchymal Stem Cell-Derived Exosomal MicroRNA-126-3p Inhibits Pancreatic Cancer Development by Targeting ADAM9. Mol Ther Nucleic Acids. 2019 Jun 7;16:229-245.