土豆
肝纤维化导致了肝实质细胞的损伤和凋亡以及肝星状细胞的活化,其中缺氧诱导因子和外泌体参与了这些现象的发生。来自华中科技大学同济医学院基础医学院石春薇课题组的研究人员发现,缺氧诱导因子Hif-1介导的活性肝星状细胞分泌外泌体,传递糖酵解相关蛋白GLUT1和PKM2,影响肝脏非实质细胞的活性和代谢状态。这种由肝星状细胞通过外泌体改变非实质细胞的功能的机制可能是肝纤维化发病的新机制。该研究发表于The FASEB Journal杂志上。
外泌体是一类由各种细胞类型分泌的细胞外囊泡,直径约为50-150nm,由细胞内的多泡体与细胞质膜融合后释放到胞外环境中。各类细胞会释放大量的外泌体,作为载体将蛋白质、mRNA和miRNA等功能性物质传递给受体细胞,在细胞间通讯中发挥重要作用。越来越多的研究表明,外泌体参与各种细胞功能的重编程以及各种疾病的发病,包括免疫反应、肿瘤转移、神经变性和传染病等。但是,外泌体在肝纤维化发生发展中的作用研究较少。
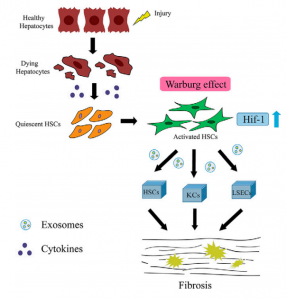
肝纤维化是由很多因素引起的慢性肝损伤的伤口愈合反应,诱发因素包括病毒性肝炎、酒精性和非酒精性脂肪性肝炎、寄生虫感染如血吸虫病以及自身免疫性疾病等。由外界因素引起的肝脏微环境中一系列病理生理变化是导致肝细胞坏死和凋亡的原因,凋亡的肝细胞释放炎症介质和细胞因子,导致肝星状细胞(hepatic stellate cells,HSC)的活化。活化的HSC表现为α-平滑肌肌动蛋白(α-SMA)的高表达、细胞外基质的合成以及脂滴减少,最终引起肝纤维化。肝脏微环境细胞主要由肝实质细胞、肝窦内皮细胞(liver sinusoidal endothelial cells,LSEC)、库普弗细胞(Kupffer cells,KCs)、HSC等细胞成分以及外泌体等非细胞成分组成。
有氧糖酵解对于将静息HSC重编程为活化的HSC至关重要,这与癌细胞中的Warburg效应类似。癌细胞中存在着能量转变的机制,即Warburg效应,它们主要进行有氧糖酵解而不是线粒体氧化磷酸化,即使在含氧量正常的环境中也是如此。在Warburg效应中,葡萄糖转运蛋白1(GLUT1)作为葡萄糖摄取的限速转运蛋白,促进葡萄糖和其他六碳糖向细胞内的扩散和渗透,促进葡萄糖的摄取和利用。M2型丙酮酸激酶(PKM2)催化葡萄糖转化为乳酸,并以更快的速率为细胞提供能量。在机制上,GLUT1和PKM2是重要核转录因子低氧诱导因子1(Hif-1)的靶基因。
Hif-1在受到缺氧或炎症刺激的HSCs的激活中起着至关重要的作用。在这项研究中,研究人员发现外泌体介导了活性HSCs与肝脏非实质细胞之间的通讯。主要研究方法如下:通过电子显微镜、Westernblot和乙酰胆碱酯酶活性检测评估了来自HSC分泌的外泌体的特征;通过共聚焦显微镜检测了静息HSC、KCs、LSEC对外泌体的摄取;通过2-ME或特异性小干扰RNA抑制Hif-1α,检测Hif-1α在HSC来源外泌体中的作用。
研究结果显示,GLUT1和PKM2在肝脏纤维化样本、细胞裂解液和活化HSC外泌体中高表达。HSC释放的外泌体与HSC的活化和葡萄糖摄取相关。活化的HSC分泌的外泌体会诱导静息HSC、KCs和LSEC的糖酵解激活。降低Hif-1表达会抑制外泌体依赖的糖酵解作用。这些结果表明,活化HSC分泌的外泌体通过递送糖酵解相关蛋白(GLUT1和PKM2)影响肝脏非实质细胞之间的代谢转换。该发现揭示了肝纤维化的一种新机制,并对肝病的新诊断和治疗方式具有重要意义。
参考文献:Wan L, Xia T, Du Y, Liu J, Xie Y, Zhang Y, Guan F, Wu J, Wang X, Shi C. Exosomes from activated hepatic stellate cells contain GLUT1 and PKM2: a role for exosomes in metabolic switch of liver nonparenchymal cells. FASEB J. 2019 Jul;33(7):8530-8542.