土豆
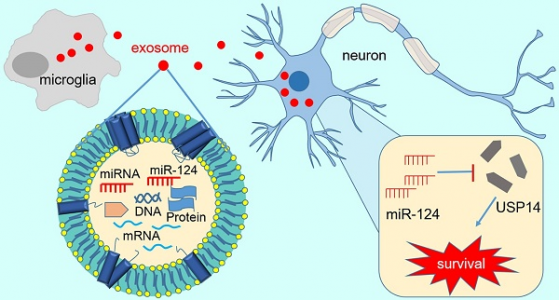
小胶质细胞通过细胞与细胞间的直接相互作用或者营养因子的间接分泌,在调节脑损伤的细胞死亡和神经行为恢复中发挥关键作用。由各类细胞分泌的外泌体被充分证明可将生物活性分子递送至受体细胞以调节细胞功能。作为神经保护作用的细胞类型,M2小胶质细胞是否可以通过外泌体介导的细胞间相互作用在脑缺血后发挥神经保护作用此前并不清楚。
5月4日,来自上海交通大学医学院附属瑞金医院、上海交通大学Med-X研究院、生物医学工程学院杨国源、汤耀辉、张志君课题组的研究人员在Theranostics杂志(IF 8.063)上发表文章,证明M2型小胶质细胞衍生的外泌体通过传递miR-124及其下游靶基因USP14减轻缺血性脑损伤并促进神经元存活。该研究揭示出M2型小胶质细胞衍生的外泌体可能会成为治疗缺血性脑中风的新途径。
小胶质细胞是大脑中固有的免疫效应细胞,在调节中枢神经系统免疫反应和脑功能中起重要作用。脑中风诱导的脑损伤激活小胶质细胞,并使小胶质细胞极化为“经典激活状态”的M1表型或“选择性激活状态”的M2表型。越来越多的证据表明M1型小胶质细胞产生高水平的促炎细胞因子并加剧急性脑损伤。相比之下,M2表型一直被认为是一种“愈合性”表型,通过神经元碎片的吞噬作用和多种营养因子(如BDNF、CXCL12、galectin-3等)的分泌,在脑卒中后发挥神经保护作用并改善长期神经学预后结果。M2型小胶质细胞的条件培养基也被充分证明具有神经保护作用,然而M2型小胶质细胞介导的神经保护的潜在机制仍然很大程度上是未知的。
外泌体是由不同细胞类型分泌的膜囊泡,并且能够穿过血脑屏障(BBB)。越来越多的证据表明外泌体在介导细胞与细胞间通讯中起重要作用。细胞衍生的外泌体货物含有多种microRNA(miRNA)、蛋白质、mRNA和DNA,可以在局部起作用或稳定地转移到受体细胞中。其中,miRNA研究最多,并且已被证明参与许多生理和病理过程。在过去十年中,外泌体已被用作缺血性中风的治疗策略。间充质干细胞(MSC)衍生外泌体富含的miR-17-92簇和miR-133b能够帮助缺血性中风后神经突触重塑和功能恢复。据报道,神经元外泌体miR-132介导神经血管通讯的细胞间信号。小胶质细胞衍生的微泡也可调节神经元兴奋性。最近的一项研究表明,在创伤性脑损伤后,来自小胶质细胞外泌体的miR-124增加会抑制神经元炎症,并通过将这些外泌体转移到神经元中而促进神经突触向外生长。然而,M2型小胶质细胞对中风后神经元功能的影响尚不清楚。
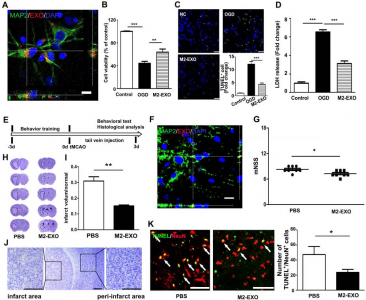
在这项研究里,研究人员将M2型小胶质细胞衍生的外泌体在大脑动脉闭塞后立即通过静脉注射到小鼠脑内。在脑缺血后3天检查梗塞体积、神经学评分和神经元凋亡情况,并测定神经元和脑组织中的外泌体RNA和靶蛋白表达水平。
结果显示, M2小胶质细胞衍生的外泌体在体外和体内均可以被神经元摄取。M2小胶质细胞衍生的外泌体能够减弱氧和葡萄糖缺乏后引起的神经元凋亡(p <0.05)。体内结果显示M2小胶质细胞衍生的外泌体处理在短暂脑缺血后3天显著减少梗塞体积,并降低动物行为缺陷(p <0.05),而miR-124敲低(miR-124 k/d)的M2小胶质细胞衍生的外泌体部分逆转了这种神经保护作用。在机制研究中,研究人员进一步证明蛋白酶USP14是miR-124的直接下游靶标。注射miR-124 k/d M2外泌体同时与USP14抑制剂联用,能够实现与单独注射M2外泌体同样的神经保护作用。
因此,研究人员得出结论,M2型小胶质细胞衍生的外泌体(M2-EXO)通过将miR-124转移到神经元中,并通过调节下游基因USP14在缺血性小鼠大脑中发挥神经保护作用。该研究突出了外泌体在脑中风后的治疗价值和潜力。
图:M2-EXO可减轻脑中风后神经元凋亡,促进神经行为恢复。
参考文献:Song Y, Li Z, He T, Qu M, Jiang L, Li W, Shi X, Pan J, Zhang L, Wang Y, Zhang Z, Tang Y, Yang GY. M2 microglia-derived exosomes protect the mouse brain from ischemia-reperfusion injury via exosomal miR-124. Theranostics. 2019 May 4;9(10):2910-2923.
外泌体资讯网 【Theranostics】上海交通大学:M2型小胶质细胞衍生的外泌体通过传递miR-124保护小鼠大脑免受缺血再灌注损伤