作者:企鹅
近日,东南大学先进光子学中心主任崔一平教授团队在Small杂志(影响因子10.856)上发表文章,开发了一种定量分析平台,用于在单外泌体水平上实现多个外泌体表面生物标志物的连续定量分析,其利用DNA-PAINT和机器学习算法自动分析结果。作为概念证明,开发了四种外泌体表面生物标志物(HER2、GPC-1、EpCAM、EGFR)的分析以鉴定来自癌症来源的血液样品的外泌体。该技术进一步应用于以100%的准确度检测来自未知样品的胰腺癌和乳腺癌。
外泌体是一种小膜囊泡(30-100 nm),含有蛋白质、脂质和核酸,可以反映其原始组织或细胞的状态。研究表明,外泌体可以参与细胞间通讯,是转移物质和信息(即蛋白质、mRNA和miRNA)的优良候选者,而不需要直接的细胞间接触。此外,由于它们富含在体液中,如尿液、血液和唾液,因此外泌体已被公认为用于非侵入性检测和监测癌症阶段的潜在生物标志物,具有改善的便利性和更快的速度,并且成本低。到目前为止,基于免疫电子显微镜(EM)表征、蛋白质印迹分析和酶联免疫吸附测定(ELISA)的方法已经揭示了外泌体上常见的以及细胞类型特异性蛋白的存在。然而,传统的基于体积的分析方法提供的灵敏度不令人满意,通常对于蛋白质印迹分析检测限为107,对于ELISA检测限为105,这使得无创性早期癌症检测无法实现。此外,目前的方法不能代表外泌体内容的异质性。解析单个外泌体内容物的能力可以更好地解决外泌体群体的固有异质性。基于珠子的流式细胞仪是一种广泛使用的方法,用于大量水平的外泌体的定量和定性,但它缺乏多参数信息。这种多参数信息可以提供更多信息的生物分子对疾病发作和进展的理解。另一方面,由于外泌体的不纯收集和不确定的浓度,在基于批量的分析方法中也出现了人工制品。从生物流体(例如,商业提取试剂盒)中大量提取外泌体很容易引入杂质,如蛋白质和长链RNA。此外,不同样品之间外泌体的浓度变化使外泌体的预定量对于整体分析是必需的。然而,对于基于单外泌体的分析,这种预先定量是不必要的。结果,基于单个外泌体的稳健的多重分析方法要求减少假阳性并提高疾病(例如,癌症)的检测准确度。
到目前为止,已经提出了几种策略用于在亚细胞水平上多重原位分析蛋白质。然而,由于外泌体的尺寸小和仪器灵敏度低,基于单外泌体的分析仍然具有挑战性。荧光超分辨率显微镜的最新进展使它们有资格观察尺寸低至10-20 nm的纳米结构。例如,单分子定位显微镜(SMLM)可以通过随机切换荧光和使用点扩散函数(PSF)的图像来解析纳米级结构。此外,还进一步探索了在此程序中获得的大量信息,以进行定量分析。然而,由于荧光团的广泛激发和发射光谱,荧光显微镜的“色彩上限”极大地限制了成像通道。为了解决这个问题,基于循环标记的连续成像方法引起了广泛关注。用于纳米级拓扑(DNA-PAINT)成像的DNA点积累提供了易于实施的方法,通过两条互补DNA链(即对接链和成像链)之间的瞬时相互作用实现多个靶的连续检测。在DNA-PAINT中,短染料标记的成像链(8-10nt)由于热波动而瞬时结合到对接链上。成像链和对接链之间的瞬时杂交和解离分别代表荧光开和关状态。通过全内反射荧光(TIRF)显微镜可以检测焦平面上的连续荧光,从而产生“眨眼状”事件。与SMLM类似,暗态和亮态之间明显的“切换”事件可用于≈25 nm空间分辨率的随机超分辨重建。通过顺序引入正交成像链,可以使用相同的激发激光进行多重成像,而不需要光谱上不同的染料。此外,对于感兴趣的区域,正交DNA探针之间的结合率与靶分子的浓度成比例。这种可编程的结合动力学(即闪烁频率和持续时间)可以进一步调整,以定量分析分布在衍射极限以下区域内的密集堆积的目标,这被称为定量PAINT(或qPAINT)。例如,Albertazzi研究组组利用DNA-PAINT来绘制和量化纳米材料表面的活性位点。
哈佛大学尹鹏研究组展示了qPAINT在蛋白质原位定量中的应用,并表明它可以在不同的实验条件下稳定而准确地工作,甚至对于一些密集的分子复合物(例如蛋白质簇)也是如此。该研究应用DNA-PAINT方法实现外泌体表面生物标志物的定量分析/分析。DNA-PAINT前所未有的灵敏度使得能够在单外泌体水平上分析表面生物标记物。该实验中,单个外泌体稀疏地固定在成像室中,因此使得分析成为相对独立的单外泌体分析并且对浓度变化不敏感。此外,由于其他污染物(例如,蛋白质和RNA)不能被特异性抗体识别,基于单外泌体的方法也可以避免不纯的提取问题。作为概念验证实验,结合机器学习算法,基于DNAPAINT的四种外泌体表面生物标志物(HER2、GPC-1、EpCAM、EGFR)的定量分析能够鉴定来自癌症血液样品的外泌体。另一方面,可以进一步探索这种集成平台,以高精度检测胰腺癌和乳腺癌。
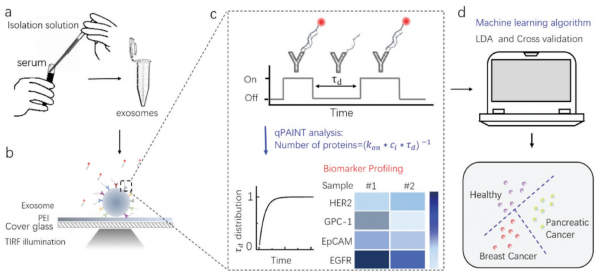
使用基于外泌体的DNA-PAINT方法检测癌症的示意图
总之,该研究开发了基于DNA-PAINT的定量平台,以实现单外泌体水平的外泌体生物标志物的综合评估。使用该平台,可以准确区分来自不同样品的外泌体。这是DNA-PAINT的第一次用于量化单个外泌体的多种生物标记物用于癌症检测。DNA-PAINT具有前所未有的灵敏度,可以在单外泌体水平上对表面生物标记进行分析,使其具有早期疾病诊断的潜力。与基于批量的分析相比,该基于单体的分析排除了蛋白质污染和浓度变化的影响,确保更准确的检测结果。基于DNA-PAINT的多重成像易于操作,没有任何特定的洗涤缓冲液,避免了在一定程度上破坏外泌体的结构。此外,对接和成像链之间的可编程和可调节的结合时间允许在更宽的检测范围内对目标进行准确的定量分析。四种生物标志物的多重定量和机器学习分析的组合使得能够准确诊断特定癌症,这使用单一生物标志物难以实现。因此,该平台为疾病(例如癌症)的无创早期诊断提供了途径。此外,该技术可以进一步开发用于单外泌体分析,以揭示外泌体异质性和功能,这将对基础研究和诊断应用具有重要影响。
参考文献:
Chen C, Zong S, Liu Y, Wang Z, Zhang Y, Chen B, Cui Y. Profiling of Exosomal Biomarkers for Accurate Cancer Identification: Combining DNA-PAINT with Machine- Learning-Based Classification. Small. 2019 Sep 3:e1901014. doi: 10.1002/smll.201901014. [Epub ahead of print]