作者:企鹅
非酒精性脂肪肝疾病(NAFLD)已成为全球主要的公共健康问题。该疾病目前影响西方国家总人口的20-35%,并且10%的患者可以从良性脂肪变性发展为更严重的疾病,包括脂肪性肝炎、肝硬化和肝衰竭。此外,有多种证据显示NAFLD与亚临床动脉粥样硬化的几种标志物之间有很强的联系,而与传统的危险因素无关。因此,NAFLD的不利影响不仅包括恶化的肝损伤,而且还包括动脉粥样硬化和其他相关心血管疾病(CVD)发生的风险。
动脉粥样硬化被认为是由脂质异常积累和血管内皮内炎性细胞浸润引起的慢性炎性代谢疾病。人们认为,启动动脉粥样硬化的第一步是内皮损伤和功能障碍。临床证据和实验数据表明,NAFLD、内皮功能障碍与CVD之间存在密切的联系,而其潜在机制尚待阐明。
NAFLD和CVD之间的联系表明细胞间通讯在疾病的致病过程中的重要性。现在已经众所周知,细胞不仅通过直接接触和可溶性因子进行通信,而且通过膜衍生的纳米大小的囊泡(即细胞外囊泡EVs)进行通信。EV携带着许多供体细胞衍生的分子,包括蛋白质、脂质和核酸。 通过将这些生物活性成分转移到靶细胞中,EV在细胞间通讯中起着至关重要的作用。EV在生理或病理条件(包括肝脏疾病)下释放,并对靶细胞产生广泛影响。各种分子货物中,microRNA被认为对EV的功能至关重要。
高度保守的miRNA,由19-26个核苷酸组成,是多种生物体基因表达的关键调节者。它们通常包含6至8个核苷酸的种子序列,对应于3'-靶mRNA的非翻译区(3′-UTR)。因此,miRNA可以通过翻译阻滞或mRNA降解来抑制靶mRNA的蛋白表达。作为EV的重要货物,miRNA最近已成为涉及多种疾病(包括NAFLD和CVD )的发病机理的关键调节因子。
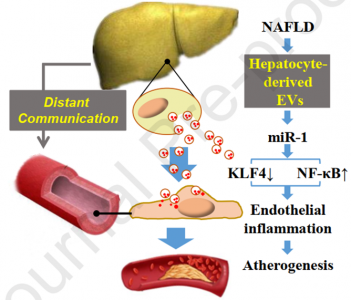
复旦大学附属中山医院内分泌科夏朴课题组在最新发表于Journal of Hepatology(影响因子18.946)的研究中,首次证明从脂肪肝细胞释放的EV是内皮炎症的有效诱因。确定了miR-1是通过下调KLF4和激活内皮细胞中NF-κB途径介导EV促炎作用的关键分子。此外,用特定的antagomir抑制miR-1会大大减弱ApoE缺陷小鼠的动脉粥样硬化。因此,该发现揭示了肝细胞源性EV在内皮炎症中的重要作用,以及与NAFLD相关的CVD发生的新的致病机制。
要点:
- 源自脂肪肝细胞的细胞外囊泡(EVs)是内皮炎症的有效诱导剂;
- MicroRNA-1(miR-1)是EV的重要分子载体,负责脂肪肝细胞的促炎作用;
- miR-1对内皮细胞的作用是通过抑制KLF4和激活NF-κB介导的;
- 抑制miR-1可以显著减少内皮炎症并减弱动脉粥样硬化;
- 肝细胞衍生的EV在肝脏与脉管系统之间的远距离通讯中起关键作用。
方法与结果:
通过使用内皮细胞特异性PCR芯片,研究发现脂肪肝的肝细胞衍生EV是内皮炎症的有效诱导剂。通过对EV中总体microRNA的分析和功能分析,发现microRNA-1是的EV关键成分,通过下调KLF4和激活内皮细胞中的NF-κB通路介导EV的促炎作用。此外,miR-1的抑制作用不仅在体外减少了内皮细胞的炎症,而且在ApoE缺陷小鼠中减弱了动脉粥样硬化的形成。
热图显示了从正常对照(NCEV)和DIO(DIOEV)小鼠分离的肝细胞源性EV之间miRNA的差异表达。
结论:
脂肪肝细胞衍生的EV通过miR-1传递、KLF4抑制和NF-κB途径激活,促进内皮炎症、动脉粥样硬化的形成。这些发现说明了肝细胞衍生的EV在肝脏与脉管系统之间的远距离通讯中的重要作用,表明了NAFLD与CVD之间联系的新机制。
总结:
非酒精性脂肪肝疾病(NAFLD)是肥胖或糖尿病患者中高度流行的疾病,对心血管疾病(CVD)发展也是一种高风险因素。该研究中确定了一种“有毒颗粒”,即在NAFLD条件下由肝细胞释放的细胞外囊泡,引起血管内皮炎症并促进动脉粥样硬化。此外,在“有毒颗粒”中鉴定出一个小分子货物,它是内皮炎症的有效诱因。通过抑制这种成分,一种特定的基于基因的抑制剂,可大大减轻小鼠的动脉粥样硬化。因此,该研究揭示了肝脏与血管之间远距离通讯的新机制,并提出了预防和治疗CVD的新方法,尤其是对于NAFLD患者。
模式图
参考文献:
Jiang F, Chen Q, Wang W, Ling Y, Yan Y, Xia P. Hepatocyte-Derived Extracellular Vesicles Promote Endothelial Inflammation and Atherogenesis via microRNA-1. Journal of Hepatology. 2019 Sep 27. pii: S0168-8278(19)30552-5. doi: 10.1016/j.jhep.2019.09.014. [Epub ahead of print]