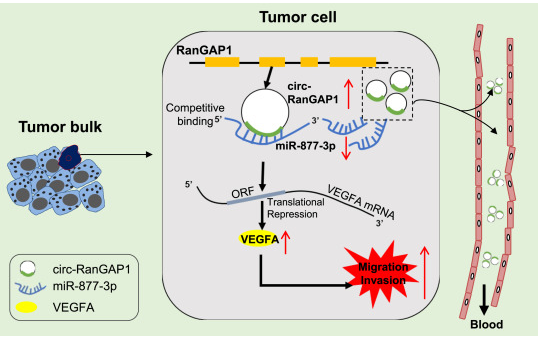
胃癌中的环状RNA(circRNA)的生物学功能研究是当前的热点。来自福建医科大学附属协和医院黄昌明、李平课题组的研究人员在Cancer Letters杂志发表文章,发现circ-RanGAP1在胃癌组织和血浆外泌体中表达增加,并作为miR-877-3p的竞争内源性RNA(ceRNA)促进了胃癌侵袭和转移,揭示了胃癌进展的一种新机制。
胃癌(GC)是一种主要的恶性肿瘤类型,是癌症死亡的第二大主要原因,也是世界第五大最常见的癌症。影响胃癌预后并导致治疗失败的重要因素是肿瘤的侵袭和转移,因此对于胃癌的治疗,探索胃癌的侵袭和转移机制具有重要意义。
环状RNA(circRNA)以共价闭环形式存在于真核细胞中,没有5’-3’极性或多聚腺苷酸尾巴,与线性RNA相比,具有更好的稳定性和保守性。越来越多的证据表明,circRNA参与了各种恶性肿瘤的各种病理过程,例如增殖、侵袭和转移,涉及的肿瘤类型包括食道癌、膀胱癌、乳腺癌、胰腺癌等等。在胃癌中,已经表明有几种circRNA可以调节肿瘤的进展。然而,circRNA在胃癌中的作用尚不清楚。
外泌体是细胞内吞起源的膜囊泡,直径在30-100 nm之间,可以将特定的蛋白质或核酸转移到局部肿瘤微环境或远处转移部位的受体细胞中。最近,许多研究报道外泌体参与肿瘤发生、肿瘤侵袭和转移。已发现外泌体中的不同蛋白质、miRNA、lncRNAs和circRNAs与肿瘤的进展相关。然而,尚未明确阐明circRNA在胃癌患者的组织和血浆外泌体中的作用模式和潜在作用。
在这项研究中,研究人员首次揭示了一种此前在肿瘤中未被发现的circRNA——circ-RanGAP1,并在GC患者术前血浆外泌体和胃癌组织中通过微阵列分析鉴定出来。研究人员发现,胃癌病人血浆中外泌体和胃癌组织中circ-RanGAP1均显著上调。 circ-RanGAP1高表达与晚期TNM分期、淋巴结转移和不良生存密切相关。抑制circ-RanGAP1降低了体外胃癌细胞的侵袭和迁移,circ-RanGAP1的过表达则出现相反的作用。此外,沉默circ-RanGAP1显著抑制了体内肿瘤的生长和胃癌的转移。在机制上,circ-RanGAP1促进miR-877-3p上调VEGFA的表达。miR-877-3p的过表达逆转了circ-RanGAP1在胃癌细胞中介导的生物学功能。有趣的是,circ-RanGAP1在术前胃癌患者的血浆外泌体中被上调,这些患者的血浆外泌体增强了胃癌细胞的迁移和侵袭能力。总体而言,circ-RanGAP1介导的miR-877-3p / VEGFA可促进胃癌进展。circ-RanGAP1可能作为潜在的预后生物标志物和胃癌治疗靶点。
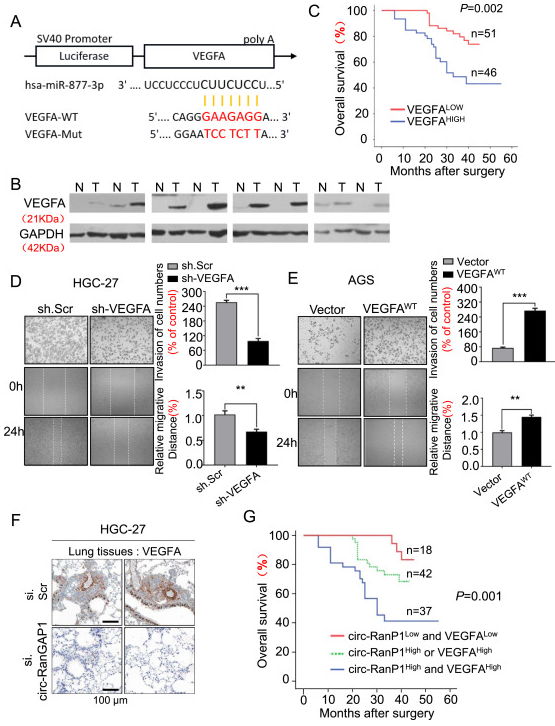 图:circ-RanGAP1通过靶向miR-877-3p / VEGFA轴促进胃癌的进展
图:circ-RanGAP1通过靶向miR-877-3p / VEGFA轴促进胃癌的进展
参考文献:Lu J, Wang YH, Yoon C, Huang XY, Xu Y, Xie JW, Wang JB, Lin JX, Chen QY, Cao LL, Zheng CH, Li P, Huang CM. Circular RNA circ-RanGAP1 regulates VEGFA expression by targeting miR-877-3p to facilitate gastric cancer invasion and metastasis. Cancer Lett. 2019. doi: 10.1016/j.canlet.2019.11.038.




