肝细胞癌是世界上最致命的癌症之一,预后极差。近年来,外泌体被认为是肝癌的潜在治疗靶标并在肝癌的发展进展中起着关键作用。来自中国医科大学附属盛京医院赵相轩课题组的研究人员在Journal of Hematology & Oncology杂志(IF=8.731)上发表综述,系统地阐述了外泌体在肝癌恶性进展中的确切分子机制和作用。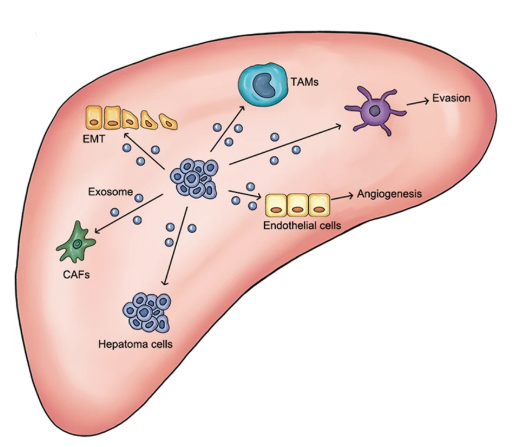 图: HCC细胞通过释放外泌体影响许多细胞类型的生物学行为变化
图: HCC细胞通过释放外泌体影响许多细胞类型的生物学行为变化
肝细胞癌(HCC,也称为原发性肝癌)是世界上最常见的癌症之一。每年大约有84万新发的HCC病例,并且至少有78万人死于HCC。肝癌的主要治疗方案是手术切除、肝移植、放疗或化学药物局部给药以及联合治疗。然而,由于HCC起病的隐匿性和缺乏特定的早期标志物,大多数患者通常被诊断时已经是晚期,不再适合手术治疗,生存时间通常只有6个月。射频消融(RFA)目前是较小的HCC的一线治疗,具有与外科手术切除相似的功效,并且损伤小、恢复快。然而,由于消融能量在肿瘤中的分布不均,杀死远端或末梢癌细胞的效率不高,可能导致残留肿瘤的存在。经导管动脉化疗栓塞(TACE)是晚期肝癌的另一种一线治疗方法。然而,由于缺氧后肿瘤中的代偿性血管增生,治疗效果也不能令人满意。索拉非尼是晚期肝癌的主流靶向治疗药物,可以显着延长患者的中位生存期,但在治疗后期逐渐会出现耐药性。因此,鉴定HCC的早期特异性诊断标志物并解决耐药性和疾病复发的问题是临床实践中的紧迫问题。
肝癌的发生和发展是一个极其复杂的病理过程,其潜在的分子机制仍不清楚。大量的基础和临床研究表明,病毒感染、酒精和非酒精性肝毒性是HCC的主要原因,而其发病机理尚不清楚。近年来,体内和体外实验都证明外泌体可能在肝癌的发生、发展、诊断和治疗中起关键作用。在肝脏中产生外泌体的细胞类型主要是肝实质细胞(例如肝细胞)、非实质肝内免疫细胞(例如巨噬细胞、树突状细胞、T / B细胞和自然杀伤细胞)、以及各种非实质性肝基质细胞(如星状细胞)。外泌体被包括乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)在内的各种病毒所利用,将病毒RNA复合物传递至相邻的正常肝细胞,并通过浆细胞样树突状细胞(PDC)诱导非特异性免疫反应,以及引起T细胞抑制的特异性免疫反应。肝星状细胞产生的外泌体含有miR-335-5p,可以通过降低HCC细胞中ROCK1的表达来诱导增殖并抑制肿瘤侵袭。然而,HCC细胞产生的外泌体中携带的miR-21可以将肝星状细胞转化为癌症相关的成纤维细胞(CAF),从而促进癌症进展。最近的研究还发现,HCC患者脂肪细胞产生的外泌体circRNA可以促进HCC细胞的生长和存活。HCC细胞还可以通过产生抑制免疫应答的外泌体来逃避肿瘤的免疫监视。临床研究发现循环外泌体中的非编码RNA(例如miR-21、miR-122和lncRNA-ATB等)或蛋白质(例如G3BP、HMGB1、LOXL4和HSP等)可用作HCC分期以及疗效和预后评估的独立肿瘤标志物。因此,外泌体在肝癌的发展、诊断和治疗中起着关键作用,并具有广泛的临床应用。
在该综述中,研究人员阐明了肝癌相关外泌体的调控机制及其信号传导途径,并分析其在肝癌的诊断和治疗中的临床应用,为今后的肝癌治疗方案提供有用的线索。该综述还讨论并总结了肝癌相关外泌体的研究进展及其潜在的临床应用。最后,研究人员得出结论,HCC相关外泌体的分离、纯化、成分鉴定和功能分析将有助于以下几个方面:第一,外泌体将有助于阐明HCC发生和发展的机制,并确定用于干预治疗的特定信号靶点;第二,可以在体外合成具有相似结构的抑癌功能的微囊泡,然后重新引入体内以达到治疗目的;第三,可以将抗癌药封装在外泌体小泡中,通过静脉内注射或肿瘤内注射直接杀伤癌细胞,避免了药物自由扩散所引起的正常细胞或器官毒性;第四,可以在外泌体的外膜上标记特异性抗原,以诱导特异性免疫反应,从而达到抗肿瘤作用;第五,外泌体可以用作新型肿瘤标志物,在基于液体活检的无创肝癌早期诊断中发挥作用。
参考文献:Wang H, Lu Z, Zhao X. Tumorigenesis, diagnosis, and therapeutic potential of exosomes in liver cancer. J Hematol Oncol. 2019 Dec 9;12(1):133.
外泌体资讯网 中国医科大学综述:外泌体在肝癌发生中的作用和诊断治疗潜力




