炎症性肠病(IBD)的常规治疗有很多副作用,迫切需要替代疗法的开发。来自中山大学附属第六医院兰平、吴现瑞课题组的研究人员在JCI Insight 杂志上发表文章,发现人骨髓来源的间充质干细胞分泌外泌体对结肠炎具有保护作用,提出了一种潜在的新型治疗IBD的治疗工具。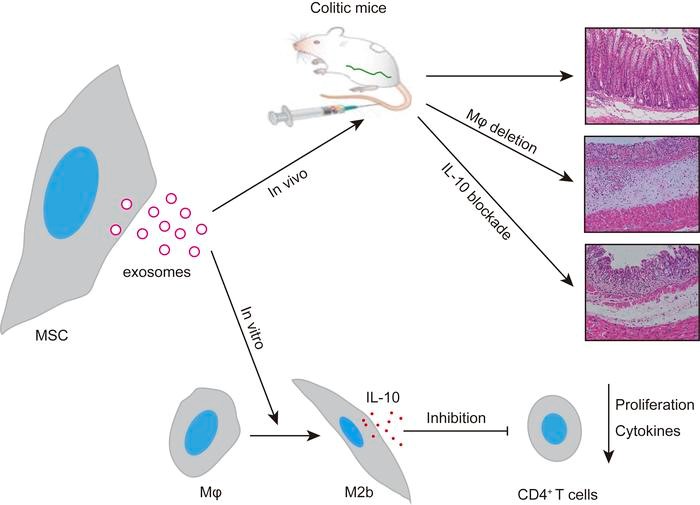 炎症性肠病(IBD)是一系列慢性、特发性、复发性和组织破坏性疾病,包括克罗恩病和溃疡性结肠炎,已成为全球范围内的一个巨大的公共卫生挑战。IBD的特征在于遗传易感人群中对肠道菌群的异常免疫反应。尽管抗肿瘤坏死因子疗法对IBD治疗取得了进展,但在当前的临床实践中,IBD有效治疗仍然是一项艰巨的挑战。传统的IBD疗法经常会导致多种严重的副作用和治疗耐药性,这就要求更多能满足需求的IBD替代疗法。
炎症性肠病(IBD)是一系列慢性、特发性、复发性和组织破坏性疾病,包括克罗恩病和溃疡性结肠炎,已成为全球范围内的一个巨大的公共卫生挑战。IBD的特征在于遗传易感人群中对肠道菌群的异常免疫反应。尽管抗肿瘤坏死因子疗法对IBD治疗取得了进展,但在当前的临床实践中,IBD有效治疗仍然是一项艰巨的挑战。传统的IBD疗法经常会导致多种严重的副作用和治疗耐药性,这就要求更多能满足需求的IBD替代疗法。
间充质干细胞(MSCs)作为一种可行且有效的IBD生物治疗方法,表现出巨大潜力。 MSC的抗炎和免疫调节活性为IBD患者的MSC移植提供了理论依据,并为IBD提供了潜在的新型细胞疗法。多项临床前研究表明,植入的MSC可以归巢于受损的组织,并可以在原位分化为功能性细胞以替代受损的细胞。但是,只有非常低的比例的植入MSC能够在体内存活并移植到受伤的组织中。这强烈表明,MSC介导的治疗作用可能归因于它们的分泌途径,而不是其组织归巢能力。的确,MSC的无细胞条件培养基和MSC的分泌物(包含细胞外囊泡和外泌体)在各种疾病中均具有有益作用。尽管MSC分泌物中具有抗炎和免疫抑制特性的治疗载体众多,但尚未鉴定出特定的介质是基于MSC治疗的有益物质。而且,尽管尚未明确证实,但在受试者体内发生恶性转化的风险仍然是阻碍MSC临床转化的关键问题。
相反,来自MSC的外泌体(MSC-Exos)具有像MSC一样的免疫调节和组织修复特性,最近已成为MSC“分泌途径”的重要组成部分,并引起了极大的研究热潮。实际上,MSC-Exos在很多疾病中都具有类似MSC的保护作用。在机制上,有研究发现,来自脂肪干细胞的外泌体通过极化M2巨噬细胞来减轻脂肪的炎症和肥胖。此外,有研究证明MSC-Exos通过调节肺巨噬细胞表型来减弱高氧血症引起的炎症。基于MSC-Exos的无细胞治疗不仅仅是MSC的治疗的补偿,MSC-Exos具有很多其他理想的功能,包括免疫沉默、非致癌性、高稳定性、细胞和组织特异性归巢,并且无血管阻塞风险。因此,与基于MSC的治疗相比,MSC-Exos具有治疗优势,探索MSC-Exos在IBD及其相关机制中的潜在作用越来越引起人们的兴趣。
在这项工作中,研究人员利用人骨髓源性间充质干细胞分泌的外泌体(MSC-Exos)可在各种IBD模型中缓解结肠炎的进展。 MSC-Exos的治疗可下调炎症反应,维持肠屏障完整性,并使M2b巨噬细胞极化,同时抑制肠纤维化。在机制上,注入的MSC-Exos主要作用于结肠巨噬细胞,与未处理的小鼠相比,用MSC-Exos处理的小鼠结肠的巨噬细胞对炎症再刺激具有明显的抵抗力。巨噬细胞的耗竭阻止了MSC-Exos的有益作用。诱导巨噬细胞产生IL-10也部分参与了MSC-Exos的抗炎作用。 MSC-Exos富含蛋白质,这些蛋白质参与调节与MSC-Exos的抗结肠炎作用有关的多种生物过程。另外,MSC-Exos中的金属硫蛋白-2是抑制炎症反应过程中的关键分子。综上所述,MSC-Exos是炎症反应的关键调节剂,可能是有希望的IBD治疗候选药物。
参考文献:Liu H, Liang Z, Wang F, Zhou C, Zheng X, Hu T, He X, Wu X, Lan P. Exosomes from mesenchymal stromal cells reduce murine colonic inflammation via a macrophage-dependent mechanism. JCI Insight. 2019 Dec 19;4(24).




