乳腺癌根据其细胞表达雌激素受体(Estrogen receptor, ER)、孕激素受体(Progesterone receptor, PR) 的情况以及表皮生长因子受体2(Epidermal growth factor receptor 2, Her-2) 基因的扩增水平可以分为luminal A/B型,Her-2扩增型(Her-2-amplified)以及三阴性 (Triple-negative)乳腺癌。曲妥珠单抗(赫赛汀)作为Her-2阳性乳腺癌治疗的常用药物,给Her-2乳腺癌患者带来了很大的生存获益,但是只有一小部分转移性乳腺癌患者对曲妥珠单抗治疗有效,并且起初治疗有效的患者中大约60%随后产生治疗抗性。所以,研究曲妥珠单抗耐药的相关机制和应对策略具有非常重要的意义。
2020年1月22日,来自郑州大学第一附属医院的韩明利博士(第一作者)、谷元廷教授(通讯作者)和海南省人民医院的董华英主任医师(通讯作者)的研究人员在Cell death&disease杂志发表文章证实,MCF10A细胞分泌的外泌体miR-567可以被曲妥珠单抗耐药细胞摄取,通过靶向ATG5逆转乳腺癌细胞的曲妥珠单抗耐药性。
外泌体是细胞分泌的细胞外囊泡,其大小在30至150 nm之间。研究表明,这些囊泡可以介导细胞间的通讯,已被用作将各种有效生物活性物质(例如蛋白质、脂质和核酸)输送至受体细胞的传递介质。在这项研究中,研究人员认为外泌体传递的miR-567可以在逆转曲妥珠单抗耐药中发挥重要作用,miR-567可作为HER-2+乳腺癌患者的治疗靶点和预后指标。为了验证这一假设,研究人员首先通过已经公开的乳腺癌表达谱数据和生物信息学分析筛选曲妥珠单抗耐药相关的潜在miRNAs。然后,通过一系列体内实验和体外实验,证实 miR-567和 ATG5在曲妥珠单抗耐药过程中的作用。研究结果显示:与对照组患者相比,对曲妥珠单抗耐药患者miR-567的表达显著降低;与亲本细胞相比,曲妥珠单抗耐药细胞的miR-567也显著下调;无论在体内还是体外,miR-567的过表达均能够逆转曲妥珠单抗的耐药性,并且miR-567的沉默还可以诱导曲妥珠单抗的耐药性;此外,miR-567可以被外泌体装载运输,靶向曲妥珠单抗耐药细胞,通过下调ATG5抑制细胞自噬,进而逆转曲妥珠单抗耐药。 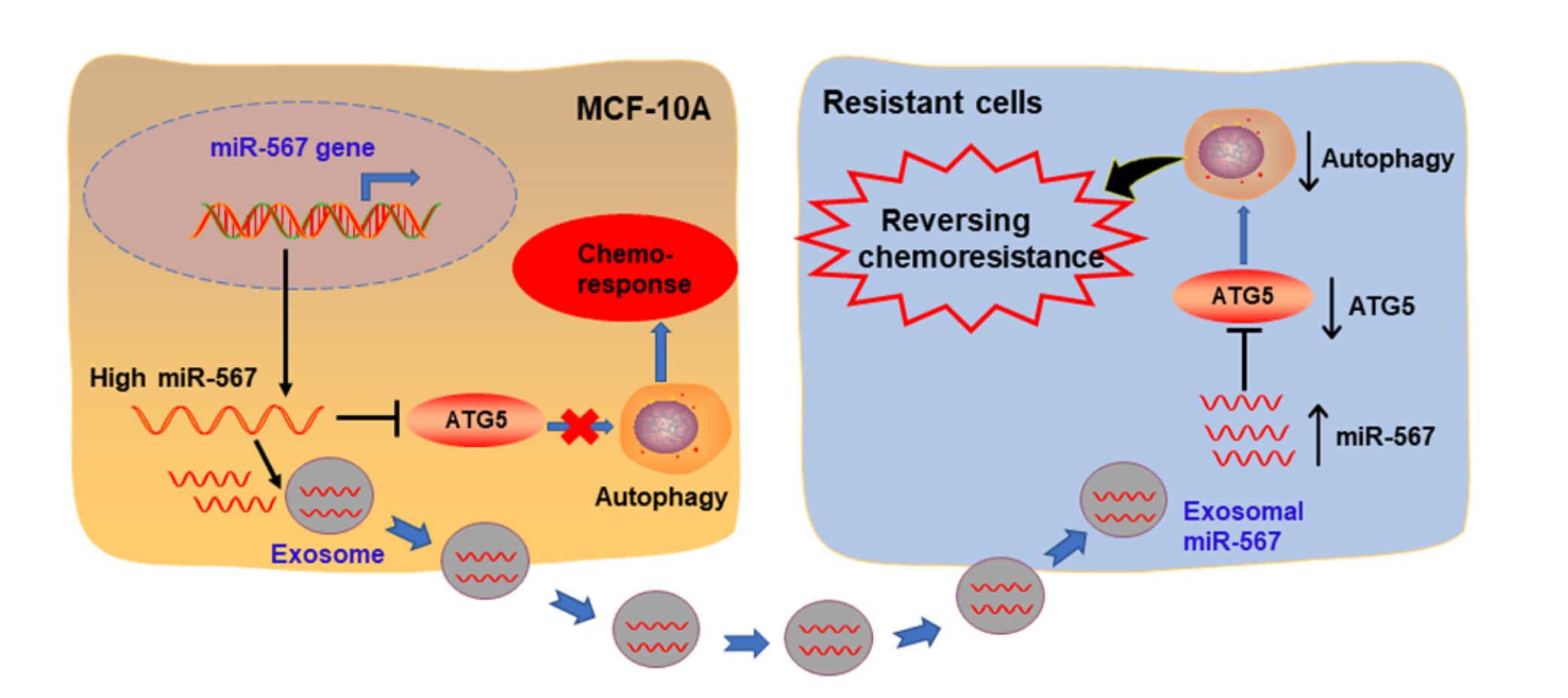
图1:该研究的机制示意图
总之,外泌体装载的miR-567通过调节细胞自噬,在逆转曲妥珠单抗耐药的过程中发挥着关键作用,该研究不仅会增加我们对非编码RNA调节癌症治疗效果的认识,而且有助于寻求更有效的逆转化疗耐药的策略。
参考文献:Mingli Han, Jianguo Hu, Pengwei Lu, Hui Cao, Chao Yu, Xiangke Li, Xueke Qian, Xue Yang, Yunqing Yang, Na Han, Dongwei Dou, Fan Zhang, Mulin Ye, Changcheng Yang, Yuanting Gu,Huaying Dong. Exosome-transmitted miR-567 reverses trastuzumab resistance by inhibiting ATG5 in breast cancer. Cell Death and Disease (2020) 11:43.




