流行病研究表明,肥胖与结肠炎发病之间存在着密切的联系。近日,来自第四军医大学杨国栋、张健课题组的研究人员在ACS Nano杂志上发表文章,利用高脂饮食喂养的肥胖小鼠模型揭示了内脏脂肪组织衍生的外泌体通过转移促炎性miRNA加剧了结肠炎进程。炎症性肠病(Inflammatory boweldisease,IBD)主要包括溃疡性结肠炎和克罗恩氏病,特征是肠道的慢性炎症。在西方国家,据估计每1000个人中就有一个患有炎症性肠病。尽管炎症性肠病与遗传易感性相关,但也发现该疾病受环境因素的影响。流行病学研究已将西方高脂饮食与炎症性肠病联系起来。此外,在过去的几十年中,该疾病在全世界的发病率都在增加,这可能部分归因于发展中国家饮食习惯的改变。由于高脂饮食与脂肪库的增加、肥胖有关,因此肥胖可能会增加炎症性肠病的风险。在临床上,高体重指数(BMI)的患者表现出更严重的症状,在确诊后的住院治疗表现中尤为明显。因此,有必要探索脂肪库与炎症性肠病之间的分子联系。事实上,脂肪组织可以通过脂肪分泌因子进行主动分泌,被认为是一种内分泌器官。这些脂肪因子起到了促炎或抗炎作用,并可能参与肥胖相关疾病的发作和进展。在脂肪因子中,科研人员近来对外泌体进行了深入研究。外泌体是胞内来源的纳米囊泡,直径范围为40至160 nm。外泌体已被认为是通过转移封装的货物(如生物活性脂质、非编码RNA、mRNA和蛋白质)来进行细胞间通讯的重要介质。这些生物活性分子由于有生物膜的包被能够避免被降解,因此具有持久的稳定性。由于表面具有蛋白特征,外泌体对受体细胞也显示出相对高的靶特异性。所有这些特征使外泌体成为细胞间通讯的重要介质,尤其是器官之间的通讯。此外,外泌体也被认为是合理的药物输送载体,为疾病诊疗提供了希望。在这项研究里,研究人员通过揭示源自内脏脂肪库的外泌体的作用来探讨高脂饮食如何影响炎症性肠病的发生,并描述了该机制在炎症性肠病预防和治疗中的价值。研究结果显示,高脂饮食显著加重了硫酸葡聚糖(DSS)引起的结肠炎表型。同时,高脂饮食改变了内脏脂肪外泌体的miRNA谱,使外泌体从抗炎表型转变为促炎表型。令人惊讶的是,这些炎性外泌体有效地循环到肠道固有层,这些外泌体则通过促进巨噬细胞M1极化使肠道发生炎症。在机制上,外泌体可以部分地通过转移促炎性miRNA(例如miR-155)促进了巨噬细胞M1型分化。此外,外泌体介导的miR-155抑制剂的递送显著阻止了DSS诱导的结肠炎。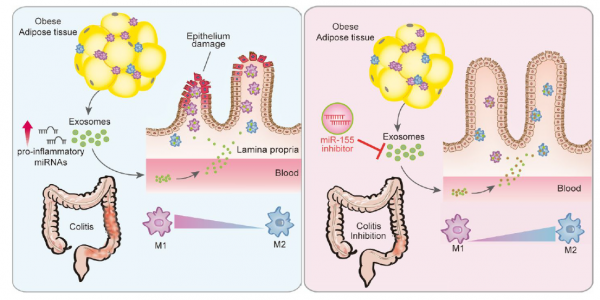 图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。总而言之,研究人员揭示了肥胖如何加剧结肠炎的外泌体途径,并提出了基于外泌体的结肠炎干预策略。通过在高脂饮食和高脂饮食喂养的小鼠中与DSS相关的结肠炎模型,研究人员探索了外泌体在结肠炎中的可能作用(如图所示)。这项研究的主要发现包括:1)脂肪组织中存在外泌体的活跃生物发生,并且来自脂肪组织的外泌体优先循环到肠道固有层中,作为重要的脂肪因子。 2)高脂饮食和肥胖改变了脂肪外泌体的miRNA谱,使外泌体从抗炎表型转变为促炎表型。炎性外泌体从肥胖脂肪到结肠组织的循环过程主要是通过促炎性货物进行的,促进巨噬细胞M1极化而促进肠道炎症。 3)脂肪组织和固有层之间的外泌体途径可用于临床干预。作为概念验证,研究表明,包裹有miR-155抑制剂的内脏脂肪来源的外泌体有效地将miRNA药物递送至固有层,从而缓解了结肠炎表型。参考文献:Wei M, Gao X, Liu L, Li Z, Wan Z, Dong Y, Chen X, Niu Y, Zhang J,Yang G. Visceral Adipose Tissue Derived Exosomes Exacerbate Colitis Severityvia Pro-inflammatory MiRNAs in High Fat Diet Fed Mice. ACS Nano. 2020 Apr 16.[Epub ahead of print]
图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。总而言之,研究人员揭示了肥胖如何加剧结肠炎的外泌体途径,并提出了基于外泌体的结肠炎干预策略。通过在高脂饮食和高脂饮食喂养的小鼠中与DSS相关的结肠炎模型,研究人员探索了外泌体在结肠炎中的可能作用(如图所示)。这项研究的主要发现包括:1)脂肪组织中存在外泌体的活跃生物发生,并且来自脂肪组织的外泌体优先循环到肠道固有层中,作为重要的脂肪因子。 2)高脂饮食和肥胖改变了脂肪外泌体的miRNA谱,使外泌体从抗炎表型转变为促炎表型。炎性外泌体从肥胖脂肪到结肠组织的循环过程主要是通过促炎性货物进行的,促进巨噬细胞M1极化而促进肠道炎症。 3)脂肪组织和固有层之间的外泌体途径可用于临床干预。作为概念验证,研究表明,包裹有miR-155抑制剂的内脏脂肪来源的外泌体有效地将miRNA药物递送至固有层,从而缓解了结肠炎表型。参考文献:Wei M, Gao X, Liu L, Li Z, Wan Z, Dong Y, Chen X, Niu Y, Zhang J,Yang G. Visceral Adipose Tissue Derived Exosomes Exacerbate Colitis Severityvia Pro-inflammatory MiRNAs in High Fat Diet Fed Mice. ACS Nano. 2020 Apr 16.[Epub ahead of print]外泌体资讯网 第四军医大学:内脏脂肪组织来源的外泌体在炎症性肠病中的促炎作用
 图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。
图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。 图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。
图:该研究的示意图。在高脂饮食诱导的肥胖中,外泌体转变为促炎症表型。此外,外泌体有效地进入结肠固有层,促进巨噬细胞M1与包裹的miR-155和其他可能的促炎性miRNAs的极化。相反,携带miR-155抑制剂的外泌体可通过诱导受体巨噬细胞M2极化而减轻结肠炎。



