肿瘤来源外泌体是生物标记物的潜在丰富来源,但是尚无有效的分离或检测方法。来自复旦大学余绍宁课题组和宁波大学丁传凡课题组的研究人员开发了一种微流控拉曼生物芯片用于分离和分析外泌体,成功应用于临床血清样品中外泌体的测定,可能会成为前列腺癌诊断的有前途的工具。该研究发表于LAB ON A CHIP杂志上。
前列腺癌(PCa)是全世界男性中最常见的癌症之一。前列腺特异性抗原(PSA)是PCa筛查和诊断中使用最广泛的生物标志物,但也有一些缺点, PSA不是疾病特异性的,PSA水平升高在非癌疾病(例如良性前列腺增生和前列腺炎)的患者中很常见。因此,迫切需要生物标志物来提高PCa诊断的特异性和敏感性。
直径在30-200 nm之间的外泌体可通过大多数细胞类型释放,并存在于不同的生物体液中,包括血液、唾液和尿液。外泌体的分子含量反映了其亲代细胞的特定生理条件和功能。近年来,由于肿瘤外泌体的高浓度(高达1011 /mL)和循环的稳定性,被作为癌症患者活检的有前途的生物标志物。分离外泌体的常用方法主要取决于非特异性的理化特性,例如粒度/密度和溶解度。超速离心是分离外泌体的最常用方法,但需要多步离心,结果产量和纯度低。此外,还已经开发了免疫捕获外泌体方法。来自多种细胞类型的所有外泌体均携带一些常见的蛋白质,例如CD9、CD63、CD81和MHCI。由于其高表达,通常选择抗CD63抗体来捕获外泌体。最近的研究报告说,EpCAM在PCa细胞和非PCa细胞的外泌体之间具有巨大的差异。
拉曼光谱已成为免疫测定的有力技术。目前,拉曼光谱法的直接应用受到其低信号强度的限制。当分析物吸附在粗糙的金属表面上,尤其是金属纳米颗粒的聚集体时,拉曼信号的强度显示出极大的增强。但是,诸如脂质、蛋白质和核酸之类的生物分子也具有拉曼活性,在400-1800 cm-1和2800-3100 cm-1区域表现出强烈的拉曼信号,这可能会影响样品检测。此前的研究曾开发了一种基于磁性富集和表面增强拉曼散射(SERS)探针的夹心免疫测定法,以检测捕获的外泌体。但是,该测定法受到金属底物的限制。为了能够有效消除复杂的细胞起源成分的干扰,又有研究报道了新型的拉曼活性聚合物纳米材料(拉曼珠),具有高密度的炔烃、腈和叠氮基,可用于细胞中的多色拉曼生物成像。拉曼珠在生物拉曼无声区(1800-2800 cm-1)具有强烈且独特的拉曼振动(高达104),极大地扩展了拉曼珠的使用范围。
由于高通量、低材料消耗、低污染以及分析所需的样品量少等优点,微流体技术被认为是一种有前途的技术。拉曼与微流体技术的结合为系统的小型化和集成化创造了新的机遇。一方面拉曼测量得到了很大的改进,另一方面微流体平台需要能够小体积感应的检测方法。因此,拉曼微流体技术非常适合此任务。幸运的是,在过去的十年中,微流控拉曼分析提高了重现性和特异性,已广泛用于生物学、化学和医学领域。
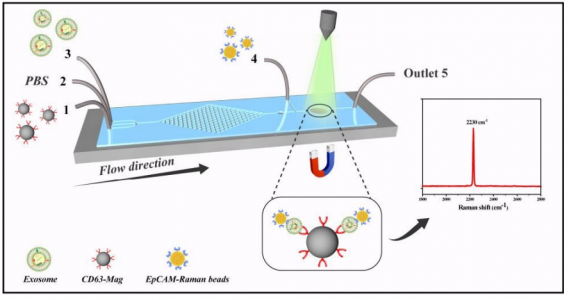
在这项研究里,研究人员开发了一种微流控拉曼生物芯片,旨在原位分离和分析外泌体。研究人员使用抗CD63磁性纳米粒子用于通过交错的三角柱阵列的混合通道富集外泌体。 他们将富集的外泌体磁性固定在拉曼检测区域和具有高密度腈的EpCAM功能化拉曼珠上,用作探针,通过简单地监测强度即可定量检测PCa细胞(LNCaP)和正常前列腺细胞(PrEC)外泌体的2230 cm-1 SERS峰的峰值,并在来自PCa患者和健康个体的临床血清样品的进一步证实了癌症诊断在临床应用中的可行性。因此,这种新颖的装置可能具有作为前列腺癌临床外泌体分析工具的潜力。
参考文献:Wang Y, Li Q, Shi H, Tang K, Qiao L,Yu G, Ding C, Yu S. Microfluidic Raman biochip detection of exosomes: apromising tool for prostate cancer diagnosis. Lab Chip. 2020 Nov 10.