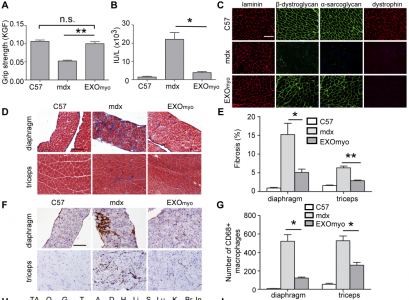
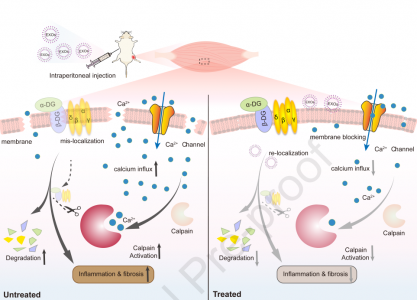
近日,天津医科大学尹海芳教授在Molecular Therapy杂志上发表文章,报道了外泌体在肌营养不良小鼠中介导膜完整性和肌肉功能的改善。杜氏肌营养不良症(DMD)是一种危及生命的肌肉疾病,由于功能性膜相关肌营养不良蛋白(一种维持肌细胞膜结构完整性所必需的蛋白质)的缺乏而导致肌肉逐渐恶化。尽管已经对许多不同的治疗方法进行了深入研究,包括恢复部分功能性肌营养不良蛋白表达的策略,例如基因替代、外显子跳跃、终止密码子通读和基因组编辑治疗,或通过针对DMD涉及的不同病理方面改善肌肉功能,但目前临床上没有一种通用的万能疗法。肌营养不良蛋白的缺乏会导致肌营养不良蛋白相关蛋白复合物(DAPC,这是确保膜稳定性的大分子复合物)的失稳和错误定位,从而严重损害膜的完整性。肌膜屏障功能的丧失会引发一系列有害事件,包括异常升高的细胞内钙内流和蛋白酶体信号通路的激活,从而导致细胞内稳态破坏和进行性肌细胞死亡。因此,膜完整性的破坏是由缺乏功能性肌营养不良蛋白引起的主要缺陷,也是DMD的潜在治疗靶标。人们一直在认真地研究改善肌肉膜完整性和稳定性的方法;目前膜稳定共聚物走在前列,如poloxamer 188(P188)。P188已在具有肌肉营养不良的mdx小鼠和金毛寻回犬中进行了全面研究,但稳定骨骼肌和心肌膜的结果各不相同,并引起争议。因此,需要探索其他可以改善肌肉膜完整性的策略。外泌体是膜结合的纳米大小的囊泡,在生理和病理条件下充当细胞间信使。最近,外泌体已被用于再生医学、在包括DMD在内的不同疾病模型中用作药物递送载体,因为外泌体本质上具有良好的品质,例如功能部分的富集、免疫原性低或无、生物相容性以及与脂质体相比更长的循环时间。值得注意的是,作为膜状囊泡的外泌体很容易通过膜融合或内吞作用被受体细胞吸收。研究表明,人间质基质细胞(MSC)衍生的外泌体可通过局部肌肉内注射缓解mdx小鼠的四头肌纤维化。然而,外泌体治疗DMD的全身治疗潜力仍有待确定。该研究证明了对来自不同来源,特别是来自鼠肌管的外泌体(EXOmyo)的反复全身性给药,可引起功能性抢救并减轻了mdx小鼠的肌肉病理进展,而没有可检测的毒性。进一步的研究表明,外泌体通过改善膜完整性并导致细胞内钙内流和钙依赖性蛋白酶活化的部分阻断以及防止DAPC降解而发挥其保护作用。该发现证明了外泌体作为DMD可行的补充治疗方法的可行性。小鼠分化肌管的外泌体(EXOmyo)改善mdx小鼠的肌肉功能和病理描述营养不良性肌肉中外泌体功能的可能作用机制的示意图LengL, Dong X, Gao X, Ran N, Geng M, Zuo B, Wu Y, Li W, Yan H, Han G, Yin H.Exosome-mediated improvement in membrane integrity and muscle function indystrophic mice. Molecular Therapy. 2020 Dec14:S1525-0016(20)30675-4. doi: 10.1016/j.ymthe.2020.12.018. Epub ahead ofprint. PMID: 33333294.外泌体资讯网 【Molecular Therapy】天津医科尹海芳教授组:外泌体介导DMD小鼠模型的肌肉功能改善