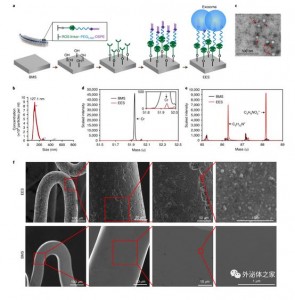
来自美国北卡罗莱纳州立大学的研究人员开发了一种具有“智能释放”触发器的外泌体支架,该支架既可以防止重新扩张的血管变窄,又可以将干细胞再生疗法用于供血不足或缺血的组织。 血管成形术是一种打开阻塞的动脉的手术,通过放置金属支架以加固动脉壁,并在去除阻塞后防止其塌陷。但是,支架的放置通常会对血管壁造成一定程度的损伤,刺激平滑肌细胞增殖并迁移到损伤处,从而修复损伤。结果是会出现再狭窄:即通过血管成形术打开的血管又发生了狭窄。该研究的通讯作者程柯教授说:“支架引起的炎症反应会降低其治疗益处。” “理想情况下,如果我们能够阻止平滑肌细胞过度反应和增殖,募集内皮细胞覆盖支架,那么将减轻炎症反应并防止再狭窄。” 程柯是北卡罗莱纳州立大学著名的再生医学特聘教授,也是北卡罗莱纳州立大学生物医学工程学联合系的教授。目前临床使用的药物涂层支架涂有抑制细胞增殖的药物,但是这些抗增殖药物也会延迟内皮细胞对支架的覆盖,而内皮细胞是临床医师希望涂覆支架的细胞类型。为了解决这个问题,程柯教授和他的团队开发了一种支架涂层,该支架涂层由间充质干细胞衍生的外泌体组成。外泌体是大多数细胞类型分泌的微小纳米囊泡。开发这种涂层背后的思路有两个方面:首先,由于外泌体与细胞膜成分类似,它们“伪装”了支架以欺骗平滑肌细胞和人体的免疫系统。其次,外泌体促进内皮细胞对支架的覆盖,在受伤的情况下,促进内皮细胞移动至靶部位以促进组织修复。为防止治疗时外泌体过早耗尽,当支架遇到活性氧(ROS)时,支架才会释放出外泌体,而活性氧在炎症反应期间更为普遍的出现。 “我们将其视为外泌体的智能释放功能,” 程柯教授说,“缺血再灌注损伤是在血流减少然后重新建立时发生的,产生了大量的ROS。假设心脏因局部缺血而受损,增强的ROS将触发支架上外泌体的释放,通过血管到达损伤部位。”图:外泌体涂层支架(EES)的制备与表征。a,EES制备过程的示意图。简而言之,从BMS到EES,制备过程包括羟基化、硅烷化、添加ROS反应性连接子、DSPE层和外泌体层。b,使用NanoSight检测MSC-XO的尺寸分布。c,MSC-XO的代表性TEM图像。 d,e,ToF-SIMS光谱显示来自BMS的Cr的表面信号和来自EES的C5H12N +和C3H6NO2 +信号。f,EES和BMS在不同放大倍数下的代表性SEM图像。 该研究团队进行了体外试验,确保生物相容性并测试释放机理。他们发现,在存在ROS的情况下,外泌体在损伤后48小时内释放了高达60%的分泌物。在大鼠缺血性损伤模型中,研究人员将外泌体涂层支架(EES)与裸金属支架(BMS)和药物涂层支架(DES)进行了比较。他们发现,与BMS相比,EES支架在减少狭窄和促进内皮覆盖方面都表现更好。尽管DES在预防再狭窄方面的表现与EES相似,但EES对血管壁的伤害较小,并且总体上具有更好的内皮覆盖率。此外,从EES释放的外泌体还促进了后肢缺血大鼠的肌肉再生。研究人员计划在大型动物模型中测试支架,并着眼于最终的临床试验。程柯教授说:“这种具有生物活性的支架可以促进血管愈合和缺血修复,并且患者在支架安装到位后就不需要其他程序进行再生治疗。” “支架是外泌体的理想载体,外泌体使支架在组织修复中更安全、更有效。”参考文献:Hu S, Li Z, Shen D et al. (2021)Exosome-eluting stents for vascular healing after ischaemic injury. Nat BiomedEng [Epub ahead of print].外泌体资讯网 Nat Biomed Eng:外泌体涂层支架用于缺血性损伤后的血管组织修复