近日,来自意大利和德国的研究人员在European Heart Journal杂志(影响因子22.673)上发表文章,报道了CD172a可用于识别来自心脏心肌的细胞外囊泡(EVs)。心脏的应激促进循环中CD172a+ EV的增加;应激产生的EVs可促进未受应激的 CMs 的正性肌力效应。在临床上,循环心脏源性CD172a+ EVs水平较高的主动脉瓣狭窄患者的生存率高于那些较低水平的患者,是一种很有前景的心肌疾病预后生物标志物。
细胞外囊泡 (EVs) 是由脂质双层分隔的、从不同亚细胞区室释放的非复制颗粒。它们可以根据物理特征进行分类,密度或大小——例如,小的EVs表示颗粒<100–200nm、中等/大EVs 表示那些>200 nm的EVs;或细胞/起源条件——例如,血小板 EVs、缺氧 EVs 或凋亡小体(ABs)。此外,因为 EVs 来自各种细胞类型,它们获得特定的原细胞表达的抗原,除了带负电荷的磷脂和膜相关糖蛋白,主要是磷脂酰丝氨酸 (PS) 和乳粘素。因此,它们也可以根据其生化成分进行分类。EVs在相同细胞和不同细胞类型之间发生的细胞间通讯途径中发挥作用。EV 与蛋白质、肽、脂质和非编码 RNA 一起,是细胞分泌组的一部分。一旦被释放,EV 就会通过其活性生物分子的货物影响周围环境,例如蛋白质、mRNA、miRNA、和脂质。特别是鞘脂在EV 生物发生、释放和活性中的作用已被确定。值得注意的是,两种鞘脂,神经酰胺 (Cer) 和 1-磷酸鞘氨醇,作为信号分子,可以改变细胞活化、生长和死亡等过程。据报道,EV 脱落会在炎症、缺氧和机械压力下增加。EVs已被描述为各种疾病环境中有趣的新生物标志物,包括炎症疾病、代谢综合征、癌症和心血管疾病 (CVD)。事实上,据报道,在动脉粥样硬化中,EVs会在斑块中积聚并影响炎症、增殖、血栓形成、钙化和血管活性反应等生物学途径;来自不同细胞类型的 EV 循环水平增加被认为在各种 CVD 中具有潜在的诊断和/或预后价值。然而,由于它们的多样性,它们的识别、表征和量化具有挑战性。因此,心肌细胞(CM) 特异性表面抗原的缺失或非选择性阻碍了对心脏源性 EV 作为心脏病诊断和预后生物标志物的特定分析。信号调节蛋白α(SIRPα;CD172a)——由白细胞亚群(即单核细胞和淋巴细胞)表达——最近据报道也是一种独特的表面标志物,可识别从人类诱导的多能干细胞(hiPSCs)分化而来的CM谱系的祖细胞。因此,该研究试图建立一种基于SIRPα表面表达来识别 CM EV 的方法。使用这种方法证明,缺氧会导致体外和体内 CM 的 CD172a+ EV 脱落增加。值得注意的是,在缺氧条件下释放的 CD172a+ EV 在功能上与无压力 CM 中的正性肌力反应相关,将这种效应归因于这些 EV 表面上的 Cer(在缺氧期间会增加的鞘脂)的富集。具有潜在临床重要性的证据表明,循环心脏 CD172a+ EV 的评估可用于主动脉瓣狭窄患者的经导管主动脉瓣置换术 (TAVR)的预后,主动脉瓣狭窄是继发于主动脉硬化的年龄相关疾病,可引起心肌肥厚和压力。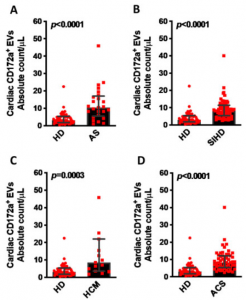
方法和结果:使用表面抗原 CD172a 作为心肌细胞 (CM) 衍生的 EV 的特异性标志物;CD172a+ EVs 的 CM 起源由它们的心脏特异性蛋白质和心脏富含的 microRNAs 的含量支持。研究发现主动脉瓣狭窄、缺血性心脏病或心肌病患者的循环CD172a+ 心脏 EV 计数高于健康受试者。细胞应激是CM 释放 EV 的主要决定因素,在体外和体内实验中,缺氧会增加EV释放。在功能水平上,从人诱导多能干细胞衍生的 CM 上清液中分离出的 EV 并在缺氧环境中培养,在未受压的 CM 中引发了正性肌力反应,研究发现这种效果依赖于表面表达神经酰胺的EV 数量的增加。具有潜在临床相关性的是,循环心脏 CD172a+ EV 计数最高的主动脉瓣狭窄患者与计数较低的患者相比,经导管主动脉瓣置换术的预后更好。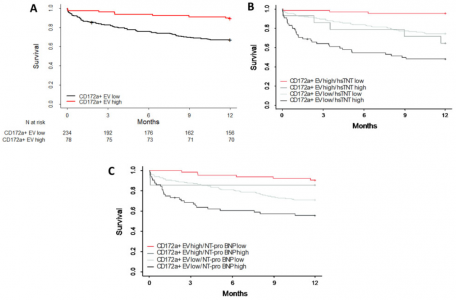
心脏 CD172a+ 细胞外囊泡在经导管主动脉瓣置换术患者中的预后相关性(Kaplan-Meier曲线)开发用于心血管疾病预后的改进方法是一项持续的挑战。该研究将 CD172a+细胞外囊泡 (EVs) 鉴定为心肌起源,并发现在缺氧应激下,心肌细胞 (CMs) 会脱落更多的 EVs,从而促进未受应激的 CMs 的正性肌力效应。在临床上,在接受经导管主动脉瓣置换术时,循环心脏源性 CD172a+ EVs水平较高的主动脉瓣狭窄患者的生存率高于那些较低水平的患者。总之,循环心脏衍生的 CD172a+ EVs是一种很有前景的心肌疾病预后生物标志物。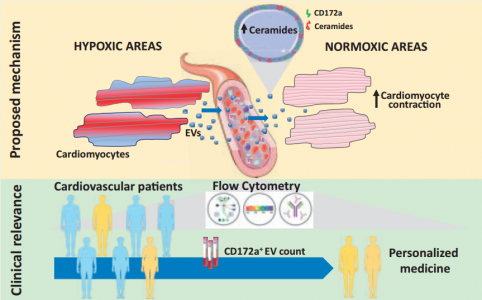
心肌细胞在缺氧应激时释放的 CD172+ 细胞外囊泡中含有的 Cermaides 可能对心脏的未受压区域产生正性肌力作用(顶部),这些囊泡数量较多的主动脉瓣狭窄患者瓣膜置换术的预后更好(底部)。AnselmoA, et al. Myocardial hypoxic stress mediates functional cardiacextracellular vesicle release. Eur Heart J. 2021 Jun9:ehab247. PMID: 34104945.外泌体资讯网 Eur Heart J:心肌缺氧应激介导功能性心脏细胞外囊泡释放