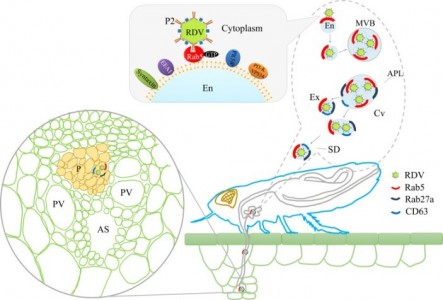
借助外泌体等细胞外囊泡进行跨物种的遗传信息或病毒分子的水平传递是近年的新研究发现。包括动物界、植物界和微生物界中不同物种间外泌体介导的生物活性分子传递都已经有所报道。但是目前对于病毒劫持外泌体释放途径进行跨物种传播的机制还存在一些缺失的环节和机制。近日,来自加拿大皇后大学的研究者们解析了病毒通过外泌体穿越昆虫唾液腺腔质膜屏障的过程,这对于我们理解外泌体接到的跨物种横向传递具有积极意义。相关研究成果有“Exosomesmediate horizontal transmission of viral pathogens from insect vectors to plantphloem”为题,发表在eLife上。 许多具有破坏性的植物、动物和人类病毒病原体通过节肢动物昆虫进行水平传播。例如,飞虱传播的水稻条纹病毒对整个亚洲的水稻种植国构成严重的农业威胁,蚊子传播的寨卡病毒(ZIKV)最近已成为美洲的公共卫生威胁。一般来说,节肢动物传播的病毒(虫媒病毒)在昆虫肠道中建立它们的初始感染,然后传播到血淋巴并最终扩散到唾液腺中,从唾液腺中病毒粒子与唾液一起被引入易感宿主体内。昆虫唾液腺细胞充满了丰富的顶端质膜内衬腔,其中储存唾液。虫媒病毒必须通过顶端质膜进入昆虫唾液腔,从而随着唾液流移动以在宿主中建立初始感染。粉虱唾液腺中央区域的分泌细胞已被证明可以协助 begomo病毒的传播性。然而,虫媒病毒如何克服腔质膜障碍以成功传播病毒仍知之甚少。通常,虫媒病毒在细胞中会被隔离在昆虫唾液腺细胞的多泡体 (MVB) 中。MVB 是球形内体细胞器,包含由膜向内体腔内出芽形成的小囊泡。 MVB 与质膜融合,以胞吐方式将内部囊泡释放到细胞外空间。这些释放的囊泡被称为外泌体,它可以将各种细胞调节 RNA 从供体细胞转运到受体细胞,因此MVB来源的外泌体受到广泛的研究关注。外泌体生物发生始于从早期内体到晚期内体的成熟,几种蛋白质与外泌体生物发生有关,包括 Rab GTPases 和四跨膜蛋白 CD63。内体 Rab GTP 酶,例如 Rab27a、Rab5 和 Rab11,可以调节外泌体的生物发生、运输和/或从培养的动物细胞中释放。值得注意的是,在 MVB 和外泌体中也检测到早期内体 Rab5。例如,来自丙型肝炎病毒感染和未感染肝癌细胞的纯化外泌体含有 Rab5。在拟南芥(一种模型植物系统)中,从叶质体中纯化的外泌体同样含有 Rab5 GTPase 同源物 ARA7。事实上,Rab5 的消耗强烈抑制外泌体的形成和分泌。此外,Rab27a 在质膜中 MVB 的对接中起作用,从而调节外泌体的分泌。例如,单纯疱疹病毒 1 糖蛋白可以与 Rab27a 相互作用以介导外泌体释放途径。正如在培养的蚊子细胞中观察到的那样,登革热病毒 (DENV) 和 ZIKV 等几种虫媒病毒劫持外泌体以释放病毒粒子。此外,虫媒病毒感染的蚊子细胞分泌的外泌体可以将病毒传播给培养的哺乳动物细胞。然而,外泌体介导的病毒传播是否发生在体内受感染的宿主组织或器官中仍然未知。通过昆虫载体进行病毒感染的最后一个瓶颈,即唾液腺的腔质膜,是昆虫物种传播病毒能力的主要决定因素。因此,作者们合理地将昆虫唾液腺的腔质膜视为培养的感染细胞的质膜。虫媒病毒利用外泌体克服昆虫唾液腺的腔质膜屏障是我们更轻松地理解体内外泌体途径释放病毒过程的良好系统.许多具有农业重要性的植物病毒病原体通过刺吸昆虫载体(例如叶蝉、飞虱和粉虱)持续传播到植物韧皮部。水稻矮缩病毒 (RDV) 是 1895 年第一个记录到的由叶蝉载体传播的植物虫媒病毒,在亚洲引起了严重的水稻病害。作者之前的研究表明,培养的叶蝉细胞可以通过感染性外泌体分泌植物呼肠孤病毒 RDV。 在这项工作中,作者们报告了 RDV 劫持外泌体释放途径以穿过顶端质膜进入唾液储存的唾液腔,最终与外泌体一起进入水稻植株的韧皮部,建立初始病毒感染。外泌体资讯网 外泌体介导病毒从昆虫到植物韧皮部的水平传播