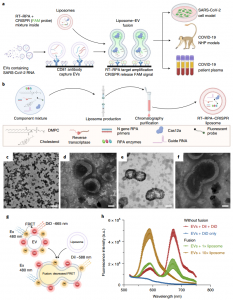
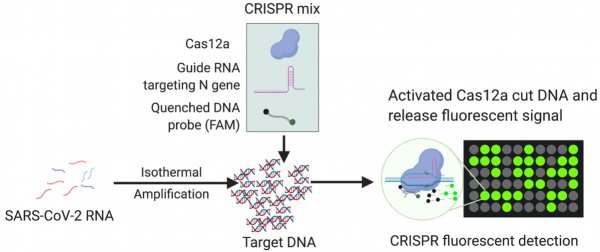
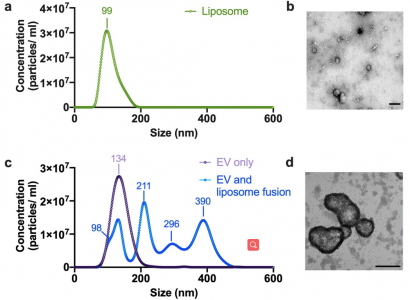
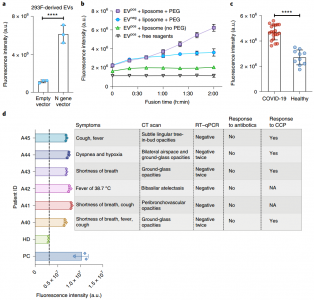
血浆SARS-CoV-2 RNA可能代表呼吸道RNA水平的可行诊断替代方案,呼吸道RNA水平在感染后迅速下降。定量RT-qPCR对血浆表现出较差的性能,这可能反映了释放到循环中的病毒RNA的稀释和降解,但这些问题可以通过分析包装到细胞外囊泡中的病毒RNA来解决。近日,美国杜兰大学(Tulane University)胡晔(Tony Ye HU)教授团队在Nature Nanotechnology杂志上发表文章,描述了一种测定方法,将直接从血浆中捕获的细胞外囊泡与载有试剂的脂质体融合,以灵敏地放大和检测SARS-CoV-2基因靶标。这种方法准确地识别了COVID-19患者,包括RT-qPCR遗漏的具有挑战性的病例。在感染后第1天检测到SARS-CoV-2阳性细胞外囊泡,并在非人类灵长类动物模型中从第6天到第28天趋于稳定,而在幼儿中观察到信号持续时间为20-60天。这种纳米技术方法使用非传染性样本并扩展病毒检测窗口,提供了一种工具来支持对呼吸道中检测不到SARS-CoV-2 RNA的患者进行COVID-19诊断。 呼吸道样本的RT-qPCR分析是COVID-19诊断的金标准,但它有局限性。感染后上呼吸道中的SARS-CoV-2 RNA水平迅速下降,而下呼吸道水平保持高位。因此,在早期SARS-CoV-2感染后进行的RT-qPCR检测可能会产生假阴性,但感染事件通常不清楚,使解释复杂化。鼻咽组织高度表达血管紧张素转换酶 2,这是SARS-CoV-2的主要受体,但该蛋白也在其他组织(例如心脏和小肠)中表达。因此,鼻咽RT-qPCR检测结果可能无法准确反映下呼吸道或肺外感染的状态。在轻度至重度COVID-19中可检测到的循环SARS-CoV-2 RNA与疾病严重程度相关并可以预测,并且似乎是导致肺外感染的原因。然而,RT-qPCR对血浆中的SARS-CoV-2 RNA的总体敏感性较差(≤41%)。因此,与常规临床测试兼容的更灵敏、更强大的基于血液的SARS-CoV-2RNA检测可以改善COVID-19的诊断和预后评估。然而,只有两项不适合临床使用的液滴数字RT-PCR研究使用超灵敏方法检测血清或血浆中的SARS-CoV-2 RNA。受感染的细胞可以分泌含有病原体衍生因子的细胞外囊泡 (EVs),保护这些因子免受水解酶的影响,并允许它们在循环中积累。甲型和丙型肝炎可以通过EV介导的病毒基因组转移来感染细胞,这表明SARS-CoV-2可能使用类似的机制。因此,这种载有病毒的EV可能作为全身病毒载量和疾病严重程度的指标,但大多数EV分离和分析方法在临床应用中不可行。RT-RPA-CRISPR脂质体的设计、表征和功能评价该报道描述了一种检测方法的开发,通过抗体与EV表面蛋白CD81的相互作用直接从血浆中捕获EV,然后与含有逆转录酶 (RT)、重组酶聚合酶扩增 (RPA) 试剂的脂质体融合,并使用类似于用于临床诊断的酶联免疫吸附测定(ELISA)的工作流程将CRISPR-Cas12a反应聚集在一起。在该测定中,向导RNA 指导CRISPR-Cas12a与RT-RPA扩增子结合,诱导淬灭寡核苷酸探针的浓度依赖性裂解,用于超灵敏检测SARS-CoV-2 RNA。这种方法采用两种成熟的技术:抗体介导的捕获和脂质体介导的试剂递送,文献中有大量报道描述了临床应用的脂质体合成和稳定方法。该方法直接检测血浆EV中的SARS-CoV-2RNANingB, Huang Z, Youngquist BM, Scott JW, Niu A, Bojanowski CM, Zwezdaryk KJ, SabaNS, Fan J, Yin XM, Cao J, Lyon CJ, Li CZ, Roy CJ, Hu TY. Liposome-mediateddetection of SARS-CoV-2 RNA-positive extracellular vesicles in plasma. NatureNanotechnology. 2021 Jul 22. dPMID: 34294909.
呼吸道样本的RT-qPCR分析是COVID-19诊断的金标准,但它有局限性。感染后上呼吸道中的SARS-CoV-2 RNA水平迅速下降,而下呼吸道水平保持高位。因此,在早期SARS-CoV-2感染后进行的RT-qPCR检测可能会产生假阴性,但感染事件通常不清楚,使解释复杂化。鼻咽组织高度表达血管紧张素转换酶 2,这是SARS-CoV-2的主要受体,但该蛋白也在其他组织(例如心脏和小肠)中表达。因此,鼻咽RT-qPCR检测结果可能无法准确反映下呼吸道或肺外感染的状态。在轻度至重度COVID-19中可检测到的循环SARS-CoV-2 RNA与疾病严重程度相关并可以预测,并且似乎是导致肺外感染的原因。然而,RT-qPCR对血浆中的SARS-CoV-2 RNA的总体敏感性较差(≤41%)。因此,与常规临床测试兼容的更灵敏、更强大的基于血液的SARS-CoV-2RNA检测可以改善COVID-19的诊断和预后评估。然而,只有两项不适合临床使用的液滴数字RT-PCR研究使用超灵敏方法检测血清或血浆中的SARS-CoV-2 RNA。受感染的细胞可以分泌含有病原体衍生因子的细胞外囊泡 (EVs),保护这些因子免受水解酶的影响,并允许它们在循环中积累。甲型和丙型肝炎可以通过EV介导的病毒基因组转移来感染细胞,这表明SARS-CoV-2可能使用类似的机制。因此,这种载有病毒的EV可能作为全身病毒载量和疾病严重程度的指标,但大多数EV分离和分析方法在临床应用中不可行。RT-RPA-CRISPR脂质体的设计、表征和功能评价该报道描述了一种检测方法的开发,通过抗体与EV表面蛋白CD81的相互作用直接从血浆中捕获EV,然后与含有逆转录酶 (RT)、重组酶聚合酶扩增 (RPA) 试剂的脂质体融合,并使用类似于用于临床诊断的酶联免疫吸附测定(ELISA)的工作流程将CRISPR-Cas12a反应聚集在一起。在该测定中,向导RNA 指导CRISPR-Cas12a与RT-RPA扩增子结合,诱导淬灭寡核苷酸探针的浓度依赖性裂解,用于超灵敏检测SARS-CoV-2 RNA。这种方法采用两种成熟的技术:抗体介导的捕获和脂质体介导的试剂递送,文献中有大量报道描述了临床应用的脂质体合成和稳定方法。该方法直接检测血浆EV中的SARS-CoV-2RNANingB, Huang Z, Youngquist BM, Scott JW, Niu A, Bojanowski CM, Zwezdaryk KJ, SabaNS, Fan J, Yin XM, Cao J, Lyon CJ, Li CZ, Roy CJ, Hu TY. Liposome-mediateddetection of SARS-CoV-2 RNA-positive extracellular vesicles in plasma. NatureNanotechnology. 2021 Jul 22. dPMID: 34294909.外泌体资讯网 Nat Nanotechnol:脂质体介导检测血浆中SARS-CoV-2RNA阳性的细胞外囊泡