外泌体是细胞分泌和吸收的内源性纳米颗粒,已被用作癌症治疗的诊断和治疗平台。将基于外泌体的递送与多种治疗方式相结合,可以带来更好的临床结果并减少副作用。近日,来自华中科技大学刘笔锋课题组研究人员将外泌体的靶向性、生物相容性与化学/基因/光热疗法相结合,设计了装载有阿霉素并涂有磁性纳米颗粒的外泌体,该纳米颗粒与能够靶向miR-21的分子信标结合,用于响应分子成像,并通过外部磁场引导外泌体富集到肿瘤部位,释放阿霉素并进行光热治疗。这种外泌体介导的多模式疗法将成为下一代精准癌症纳米药物的有前途的平台。该研究发表于Biomaterials杂志上。 癌症是最致命的人类疾病之一,在全世界夺走了数百万人的生命。癌症的治疗方法,如化学疗法、免疫疗法、放射疗法、基因疗法和热疗法在患者的临床结果方面取得了巨大进步。近年来,两种或多种癌症治疗方式间的不同疗法的组合已表现出癌细胞的治疗效力的提高,同时减少了副作用。这些组合疗法的推进需要依赖于将不同的治疗方式集成到一个单一的可调节纳米递送系统中。在这个领域里,外泌体,由各种细胞分泌并被受体细胞吸收的内源性纳米颗粒(50-150 nm),由于其独特的结构和组成,已被用作癌症诊断和治疗的多功能治疗天然载体,并具有低细胞毒性、克服生物障碍和逃避免疫监视的特性。特别是外泌体由于与人体其他细胞成分相似,具有稳定的脂双层膜结构,在血液中循环稳定,因此可以稳定包封的核酸或蛋白质,提高疏水性药物的溶解度。
癌症是最致命的人类疾病之一,在全世界夺走了数百万人的生命。癌症的治疗方法,如化学疗法、免疫疗法、放射疗法、基因疗法和热疗法在患者的临床结果方面取得了巨大进步。近年来,两种或多种癌症治疗方式间的不同疗法的组合已表现出癌细胞的治疗效力的提高,同时减少了副作用。这些组合疗法的推进需要依赖于将不同的治疗方式集成到一个单一的可调节纳米递送系统中。在这个领域里,外泌体,由各种细胞分泌并被受体细胞吸收的内源性纳米颗粒(50-150 nm),由于其独特的结构和组成,已被用作癌症诊断和治疗的多功能治疗天然载体,并具有低细胞毒性、克服生物障碍和逃避免疫监视的特性。特别是外泌体由于与人体其他细胞成分相似,具有稳定的脂双层膜结构,在血液中循环稳定,因此可以稳定包封的核酸或蛋白质,提高疏水性药物的溶解度。 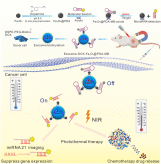 在这项研究里,研究人员提出了一种通过整合生物外泌体和合成成分来实现化学/基因/光热癌症治疗的组合治疗平台。该系统由生物素标记的供体细胞通过细胞代谢途径分泌的生物素功能化外泌体组成。通过电穿孔将阿霉素(DOX)封装到分离的外泌体中,然后用聚多巴胺(PDA)包被的磁性 Fe3O4 纳米粒子(Fe3O4@PDA)进而功能化外泌体表面。Fe3O4@PDA 表面在碱性条件下通过自聚合用亲和素和分子信标(MB)进行改性。Fe3O4@PDA 会使得外泌体在磁场下靶向聚集在肿瘤部位。同时,涂覆在 Fe3O4 上的 PDA 可以强烈淬灭 MB 的荧光。进入肿瘤细胞后,释放的分子信标可以针对 miR-21 进行成像和基因沉默。由于对细胞内 microRNA-21(miR-21) 的特异性识别,这是一种众所周知的肿瘤诊断和预后标志物,然后MB 的荧光被打开,同时 miR-21 响应荧光成像,并通过形成双链体结构抑制 miR-21 功能,进行抗肿瘤治疗。近红外辐射 (NIR) 的应用会引起局部高热并触发外泌体内装载的货物的释放,同时释放的阿霉素用于杀死癌细胞。在近红外下用 Exo-DOX-Fe3O4@PDA-MB 处理后,约 91.04% 的癌细胞被杀死。动物模型也证明了基于外泌体的癌症治疗方法的能力,其中使用磁场引导的肿瘤靶向化学/基因/光热方法使肿瘤大小显著减小了97.57%。这是由于聚合在磁珠表面的PDA可以将近红外光转化为热能,从而杀死靶标癌细胞,造成外泌体不稳定性,从而促进封装化学药物DOX的触发释放。因此,这项工作为设计具有多种功能的外泌体以实现精确的癌症诊断铺平了道路。参考文献:Designer exosomes enabling tumor targeted efficientchemo/gene/photothermal therapy. Biomaterials. 2021 Jul 31;276:121056.
在这项研究里,研究人员提出了一种通过整合生物外泌体和合成成分来实现化学/基因/光热癌症治疗的组合治疗平台。该系统由生物素标记的供体细胞通过细胞代谢途径分泌的生物素功能化外泌体组成。通过电穿孔将阿霉素(DOX)封装到分离的外泌体中,然后用聚多巴胺(PDA)包被的磁性 Fe3O4 纳米粒子(Fe3O4@PDA)进而功能化外泌体表面。Fe3O4@PDA 表面在碱性条件下通过自聚合用亲和素和分子信标(MB)进行改性。Fe3O4@PDA 会使得外泌体在磁场下靶向聚集在肿瘤部位。同时,涂覆在 Fe3O4 上的 PDA 可以强烈淬灭 MB 的荧光。进入肿瘤细胞后,释放的分子信标可以针对 miR-21 进行成像和基因沉默。由于对细胞内 microRNA-21(miR-21) 的特异性识别,这是一种众所周知的肿瘤诊断和预后标志物,然后MB 的荧光被打开,同时 miR-21 响应荧光成像,并通过形成双链体结构抑制 miR-21 功能,进行抗肿瘤治疗。近红外辐射 (NIR) 的应用会引起局部高热并触发外泌体内装载的货物的释放,同时释放的阿霉素用于杀死癌细胞。在近红外下用 Exo-DOX-Fe3O4@PDA-MB 处理后,约 91.04% 的癌细胞被杀死。动物模型也证明了基于外泌体的癌症治疗方法的能力,其中使用磁场引导的肿瘤靶向化学/基因/光热方法使肿瘤大小显著减小了97.57%。这是由于聚合在磁珠表面的PDA可以将近红外光转化为热能,从而杀死靶标癌细胞,造成外泌体不稳定性,从而促进封装化学药物DOX的触发释放。因此,这项工作为设计具有多种功能的外泌体以实现精确的癌症诊断铺平了道路。参考文献:Designer exosomes enabling tumor targeted efficientchemo/gene/photothermal therapy. Biomaterials. 2021 Jul 31;276:121056.外泌体资讯网 华中科技大学研究人员开发了基于外泌体的化学/基因/光热联合疗法,实现高效肿瘤治疗



