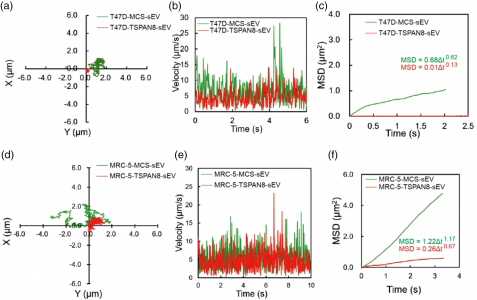
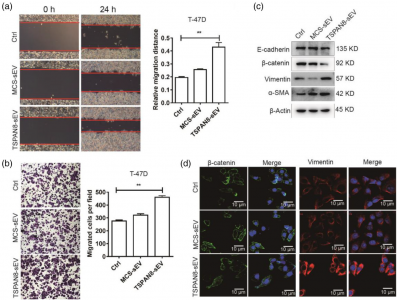
近年来,微小细胞外囊泡(smallextracellular vesicles, sEVs)由于其特异优势而被广泛的应用于疾病的诊断与治疗。sEVs包装大量的生物活性分子可以通过血流输送至机体多种器官组织。有研究表明sEVs荷载分子可以调控生理或病理微环境中靶细胞的表型。然而,有关sEVs与受体细胞结合的相关分子机制还不明确。近日,来自南开大学医学院岳世静副教授团队及南开大学化学院肖乐辉教授团队的合作研究首次证明TSPAN8分子可以促进sEVs在受体细胞中的限制性扩散,进而提高靶细胞的摄取并促进肿瘤细胞的迁移和上皮间充质样转化(epithelial-mesenchymal transition, EMT),诱导肿瘤转移。该研究有利于明确TSPAN8分子修饰在提高sEVs药物递送系统效率中的作用。相关内容以“High TSPAN8expression in epithelial cancer cell-derived small extracellular vesiclespromote confined diffusion and pronounced uptake”为题发表在国际细胞外囊泡学会会刊JExtracell Vesicles上(2021;10:e12167)。本文的第一作者为南开大学医学院硕士研究生王腾、南开大学化学院博士研究生王鑫、成都第三人民医院的王浩斌副主任医师;通讯作者为南开大学化学院肖乐辉教授和南开大学医学院岳世静副教授。sEVs在细胞间通讯中具有关键调节作用,sEVs装载大量生物活性分子可能会影响受体细胞的表型和功能。上皮样癌细胞来源的sEVs富集CD151或TSPAN8与整合素Integrins分子相互作用形成复合物,可促进肿瘤进展。而sEVs与受体细胞的结合过程及调节机制仍然缺乏研究。这项研究通过基因工程手段调节乳腺癌细胞表达TSPAN8,通过检测表达TSPAN8乳腺癌细胞来源的sEVs与靶细胞的相互作用,研究 TSPAN8分子对sEVs在靶细胞膜表面的扩散和转运特性的影响。运用单粒子追踪技术证明TSPAN8分子可通过对sEVs的限制性扩散显著促进其与受体细胞的结合。进一步功能分析表明,表达TSPAN8的sEVs显著促进了癌细胞的运动性和上皮间充质样转化(EMT)。体内研究表明,表达TSPAN8的sEVs显著促进了其在肝脏、肺和脾脏中的结合和滞留。该研究得出结论,TSPAN8通过加强限制性扩散促进sEVs与靶细胞间的相互作用,并显著促进细胞的运动。因此,表达TSPAN8的sEVs可作为重要的直接或间接肿瘤治疗靶点。图1. TSPAN8改变sEVs在靶细胞表面的扩散模式图2. 富集TSPAN8的sEVs促进受体细胞的迁移和EMT转变HighTSPAN8 expression in epithelial cancer cell-derived small extracellularvesicles promote confined diffusion and pronounced uptake. J ExtracellVesicles. 2021 Nov;10(13):e12167. doi: 10.1002/jev2.12167.外泌体资讯网 J Extracell Vesicles:高表达TSPAN8促进上皮癌细胞来源微小细胞外囊泡的限制性扩散和摄取