使用免疫检查点阻断(immune checkpoint blockade, ICB)在癌症治疗方面取得了前所未有的进展。然而,反应仅限于一部分患者,并且可能存在免疫相关不良事件(immune-related adverse events, irAE)问题而需要停止治疗。迫切需要深入了解影响ICB反应和毒性的宿主内在和外在因素。在过去的十年中,我们对宿主内在因素(例如宿主基因组、表观基因组和免疫)的影响的理解有了很大的发展,对这些因素以及肿瘤和免疫共同进化有了更深入的了解。此外,我们开始了解宿主内部和外部(如exposome)的急性和累积暴露对宿主生理和治疗反应的影响。这些共同代表了对ICB的反应、抗性和毒性的标志。在癌症的发展和进展过程中,肿瘤会进化并可能表现出多种机制来逃避肿瘤免疫监视和抑制抗肿瘤免疫反应。肿瘤免疫逃避的一个主要机制涉及免疫检查点通路的参与。在生理条件下,免疫检查点分子调节免疫系统,在成功缓解感染或其他威胁后抑制免疫反应。然而,这些免疫检查点相互作用也可能与癌症的发生有关,越来越多的努力以这些免疫检查点为目标以增强抗肿瘤免疫。该综述总结了过去十年对免疫检查点阻断(immune checkpoint blockade, ICB)的反应和抵抗机制方面取得的进展;描述了不同的免疫检查点和ICB策略,并讨论了各种宿主内在和宿主外在因素在对ICB产生抗性中的作用,并提供了对ICB毒性的潜在决定因素的见解;最后,探索了不断增长的诊断和治疗策略,以增强对ICB的反应并消除毒性。
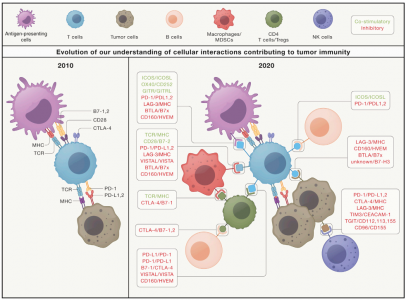
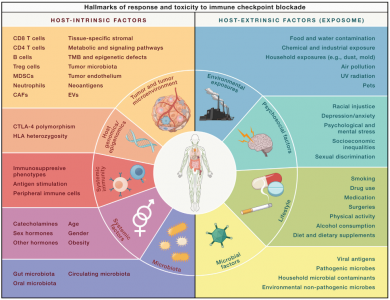 影响抗肿瘤免疫和免疫治疗反应的因素癌症免疫疗法领域的范式转变发现及其对治疗策略的成功转化,使原本只有有限治疗选择的癌症患者获得了长期生存。尽管如此,由于对ICB的原发性或获得性耐药以及相关的毒性,从这些治疗中获得临床益处的患者数量仍然有限。已经做出了广泛的努力来开发诊断方法,以识别将从ICB中受益的患者,以及增强反应和消除毒性的治疗策略。然而,将ICB的益处扩展到更多的癌症患者需要深入了解耐药性和毒性的潜在机制。宿主内在因素在响应ICB中的作用,包括肿瘤遗传学和肿瘤微环境的免疫和非免疫成分已被广泛研究,并且仍在积极研究中。然而,为了充分阐明这些机制,重要的是要认识到包括微生物组、宿主系统因素以及环境暴露(exposome)在内的各种因素在对ICB的反应和毒性方面可能发挥重要作用。未来的研究需要了解这些因素的个体和集体作用,并将促进新的诊断、预后和治疗策略的开发,以解决当前与ICB相关的局限性并改善癌症患者的预后。文献:Morad G, HelminkBA, Sharma P, Wargo JA. Hallmarks of response, resistance, and toxicity toimmune checkpoint blockade. Cell. 2021 Oct14;184(21):5309-5337. doi: 10.1016/j.cell.2021.09.020. Epub 2021 Oct 7. PMID:34624224.
影响抗肿瘤免疫和免疫治疗反应的因素癌症免疫疗法领域的范式转变发现及其对治疗策略的成功转化,使原本只有有限治疗选择的癌症患者获得了长期生存。尽管如此,由于对ICB的原发性或获得性耐药以及相关的毒性,从这些治疗中获得临床益处的患者数量仍然有限。已经做出了广泛的努力来开发诊断方法,以识别将从ICB中受益的患者,以及增强反应和消除毒性的治疗策略。然而,将ICB的益处扩展到更多的癌症患者需要深入了解耐药性和毒性的潜在机制。宿主内在因素在响应ICB中的作用,包括肿瘤遗传学和肿瘤微环境的免疫和非免疫成分已被广泛研究,并且仍在积极研究中。然而,为了充分阐明这些机制,重要的是要认识到包括微生物组、宿主系统因素以及环境暴露(exposome)在内的各种因素在对ICB的反应和毒性方面可能发挥重要作用。未来的研究需要了解这些因素的个体和集体作用,并将促进新的诊断、预后和治疗策略的开发,以解决当前与ICB相关的局限性并改善癌症患者的预后。文献:Morad G, HelminkBA, Sharma P, Wargo JA. Hallmarks of response, resistance, and toxicity toimmune checkpoint blockade. Cell. 2021 Oct14;184(21):5309-5337. doi: 10.1016/j.cell.2021.09.020. Epub 2021 Oct 7. PMID:34624224.外泌体资讯网 Cell综述介绍了细胞外囊泡在免疫检查点阻断疗法中的功能作用

 影响抗肿瘤免疫和免疫治疗反应的因素
影响抗肿瘤免疫和免疫治疗反应的因素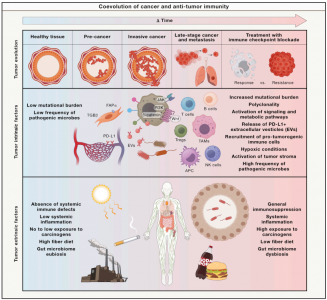
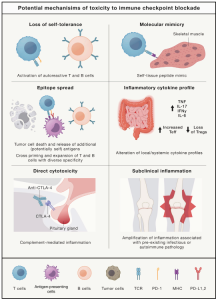

 影响抗肿瘤免疫和免疫治疗反应的因素
影响抗肿瘤免疫和免疫治疗反应的因素
