外泌体是细胞内的多囊泡体与细胞质膜融合后分泌至胞外的纳米级囊泡,广泛分布于血液、唾液、尿液、母乳等多种体液中。它不仅是细胞间信号传递载体,也是相关疾病潜在的生物标志物,对疾病诊断及预后监测具有重要价值。目前基于外泌体的液体活检大多利用血液中的外泌体进行分析,具有一定的侵入性。相对而言,尿液携带了丰富的组分信息,收集方便,且无侵入性。由于泌尿系统相关疾病的发生发展与尿液组分变化的相关性,对尿液来源外泌体表面蛋白标志物进行分析,有望为泌尿系统疾病的无创早期诊断提供可能。
近日,东北大学理学院王建华教授团队开发了一种基于3D DNA机器联合机器学习算法的新策略,通过分析尿液外泌体来源的蛋白标志物,构建了3种泌尿疾病早期诊断模型,结果显示,相对于传统的统计分析,机器学习能够通过对已知生物信号进行学习,构建决策系统,进而显著提高疾病的诊断效能。该研究以“Ratiometric 3D DNA Machine Combined with Machine Learning Algorithmfor Ultrasensitive and High-Precision Screening of Early Urinary Diseases”为题,发表在国际著名学术期刊 ACS Nano上(doi.org/10.1021/acsnano.1c06429),博士研究生武娜为论文第一作者,杨婷教授为论文通讯作者。
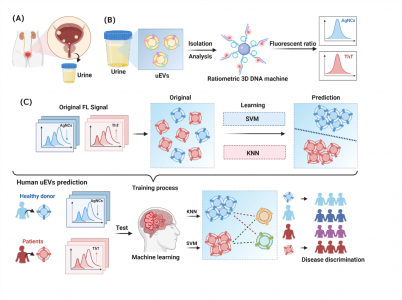
该研究利用适配体与外泌体表面蛋白的特异性结合,设计了一种基于3D DNA walker结合RCA级联放大策略的3D DNA机器。具体而言,轨道分子与挂锁探针 (包含G-4链的互补链)以及信号探针1 (AgNCs-DNA) 经过预杂交形成一个复合探针,随后复合探针被负载到一个磁性纳米粒子上,可通过与目标外泌体特异性竞争吸附适配体释放DNA walker。在核酸外切酶 III (Exo III) 的作用下,DNA walker可以沿着三维表面上的轨道分子高速行走并切割及释放大量信号分子1。此时,轨道分子的双链结构被破环,挂锁探针与轨道分子杂交体由“封闭”转变为“灵活”结构,在phi29聚合酶的作用下进行RCA扩增,产生大量的G-4链的重复单元用于输出信号分子2。由此可实现对外泌体的稳定、高灵敏检测。多种适配体的引入可实现对外泌体多种表面蛋白的分析。
通过分析临床样本来源外泌体,获取比率荧光数据,将数据随机分成70%和30%。70%的数据用于两种ML算法 (K-最邻近(KNN)和支持向量机(SVM))的训练以构建诊断模型,然后将30%的数据用于三种泌尿疾病的预测和分类。借助ML辅助诊断模型,可通过将预测与病理诊断患者的实际情况进行比较,进一步评估不同来源外泌体标志物组合的诊断性能。该方法为泌尿系统基本早期诊断提供了新的思路
图1 比率3D DNA机器结合机器学习-早期泌尿疾病来源外泌体的诊断系统的构建示意图;
参考文献:
Ratiometric 3D DNA Machine Combinedwith Machine Learning Algorithm for Ultrasensitive and High-Precision Screeningof Early Urinary Diseases. ACS Nano, 2021 Nov 23.