外泌体作为当前液体活检领域的研究热点之一,可以参与肿瘤的形成和演化过程,在肿瘤的早期筛查及精准诊疗过程中蕴含巨大潜力和价值。因此,通过高效灵敏检测手段监测外泌体对了解肿瘤的发生发展情况意义重大。
近日,来自重庆医科大学检验医学院丁世家教授课题组的研究人员在国际知名杂志Journal of Nanobiotechnology上发表了题为“Surface plasmon resonance biosensor for exosome detectionbased on reformative tyramine signal amplification activated by molecularaptamer beacon”的文章(2021 Dec 24;19(1):450)。在这篇文章中,作者提出了一种基于分子适体信标(MAB, molecular aptamer beacon)和酪胺信号放大(TSA, tyramine signal amplification)技术的新型表面等离子体共振(SPR, surface plasmon resonance)传感方法用于高灵敏检测人表皮生长因子受体2(HER2)阳性外泌体(HER2+外泌体),并完成了对临床样本的检测,具有一定的临床应用价值。HER2+外泌体在乳腺癌的早期诊断和治疗监测中发挥着极其重要的作用。该课题组基于分子适体信标 (MAB) 转换激活的改良酪胺信号放大 (TSA)技术,提出了一种免标记表面等离子共振 (SPR) 生物传感器,用于高灵敏和特异性检测 HER2+外泌体。通过适体和HER2蛋白的相互作用,外泌体被修饰于芯片表面的 MAB捕获,这使得其G4序列暴露,从而形成具有类过氧化物酶活性的 G4-hemin催化酶。继而,在 H2O2存在时,G4-hemin催化大量酪胺包被的金纳米颗粒在外泌体膜上沉积,产生显著放大的SPR信号。在该工作中,作为TSA主要成分的辣根过氧化物酶被仿生酶 G4-hemin取代,创新性的构建了改良的TSA,规避了传统TSA中采用天然酶所导致的弊端。同时,得益于改良TSA有效的信号增强能力,这种新型SPR生物传感器具有较高的灵敏度,线性检测范围为1.0 × 104 到 1.0 × 107 颗粒/mL。此外,对外泌体表面HER2蛋白和脂质膜的双重识别赋予了该传感策略高度的特异性,避免了游离蛋白的干扰。该方法能够准确地区分HER2+乳腺癌患者和健康个体,具有巨大的临床应用潜力。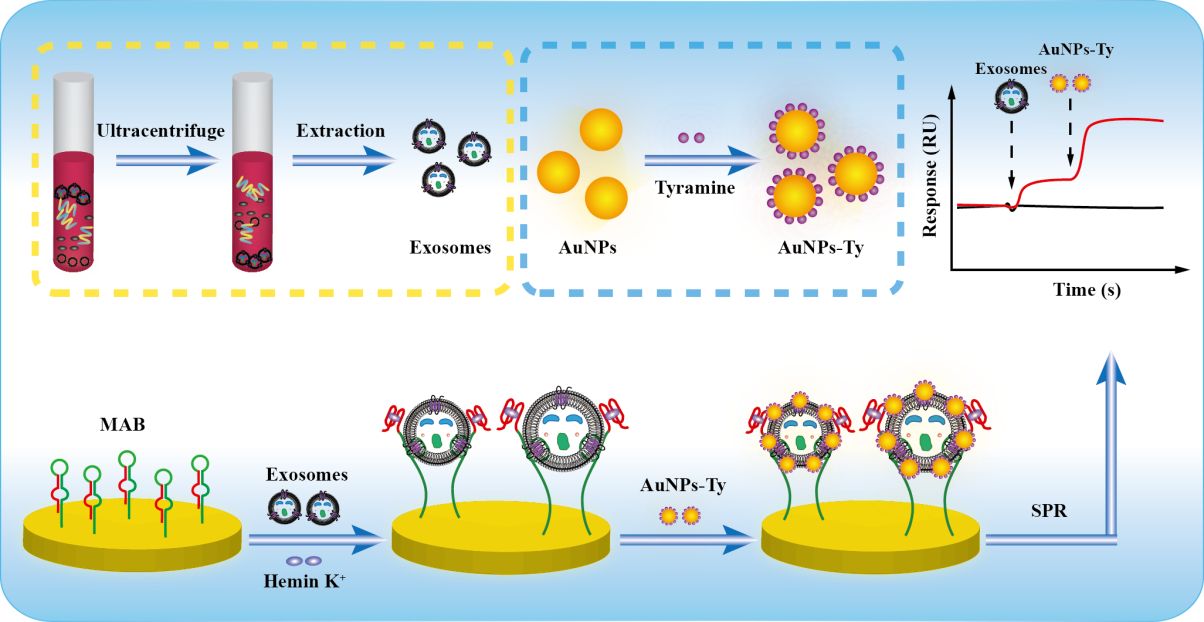
基于MAB框架转换激活改良酪胺信号放大(TSA)用于HER2 +外泌体的高灵敏检测Surface plasmon resonance biosensor for exosomedetection based on reformative tyramine signal amplification activated bymolecular aptamer beacon. J Nanobiotechnology. 2021 Dec 24; 19 (1):450. 外泌体资讯网 J Nanobiotechnology:基于分子适体信标激活改良酪胺信号放大技术的表面等离子共振生物传感器用于外泌体检测

