质母细胞瘤(GBM)是成人最常见的原发性颅内恶行肿瘤,其标准治疗方案包括手术切除联合放疗和化疗。替莫唑胺(TMZ)是GBM的常规治疗用药,尽管TMZ在治疗的早期阶段可以抑制GBM的生长,但超过40%的GBM患者逐渐发展为TMZ耐药,从而导致患者病情的恶化。目前,克服TMZ耐药仍然是治疗GBM面临的重大挑战。因此,寻找可靠的生物标志物来预测TMZ的疗效并进一步探索导致GBM患者TMZ耐药的潜在机制迫在眉睫。近日,天津医科大学总医院康春生教授团队在Theranostics上发表了题为“PTRF/Cavin-1 enhances chemo-resistance and promotes temozolomide efflux through extracellular vesicles in glioblastoma”的研究论文(2022 May 16;12(9):4330-4347), 揭示了胶母细胞瘤中,PTRF/cavin1通过细胞外囊泡促进替莫唑胺外排和增加化学药物抗药性的作用机制。天津医科大学总医院康春生教授,河北大学附属医院方川教授及天津市环湖医院刘晓民教授为该文的共同通讯作者,天津医科大学总医院研究生杨二艳,王琳,武烨为文章的共同一作。

聚合酶I和转录释放因子(PTRF),也称为cavin-1,是与细胞膜穴样内陷(caveolae)相关的蛋白。PTRF直接参与了细胞来源的外泌体(EXO)的形成和分泌,以维持神经胶质瘤细胞之间的联系。该团队前期研究表明PTRF可以触发细胞质磷脂酶A2(cPLA2)介导的磷脂重塑,从而促进GBM细胞增殖。并且PTRF可能在GBM患者的多重耐药(MDR)中充当阳性调节剂。因此,作者假设PTRF介导的外泌体(EXO)形成和分泌可能在GBM患者TMZ耐药中起关键作用。氯喹(CQ)是一种传统的抗疟药,可改变溶酶体pH值抑制内吞作用和EXO的释放。之前研究表明,CQ可以通过减少抗癌药物的向外运输来有效地逆转癌细胞的多重耐药。因此,作者提出探究CQ是否可以增加GBM治疗中TMZ的敏感性。 通过对TCGA数据库的GBM基因表达谱进行分析,作者发现GBM患者的预后与PTRF表达水平负相关。进一步分析发现TMZ治疗的GBM患者的预后与PTRF表达水平呈负相关。使用多元因素回归分析结果表明,PTRF表达与GBM患者整体生存预后相关。因此,证明PTRF可以作为一种新的生物标志物,独立于MGMT甲基化来预测GBM患者给予TMZ治疗的预后。随后,体外实验发现PTRF通过增加细胞外囊泡介导的TMZ外排减少细胞内TMZ浓度来降低TMZ的疗效。为了更好地促进临床转化,作者进行了一系列体外和体内实验,证明了TMZ联合CQ的序贯疗法可通过增加细胞内TMZ浓度从而抑制神经胶质母细胞瘤的生长。该研究为临床胶质母细胞瘤患者的治疗提供了新的方向。
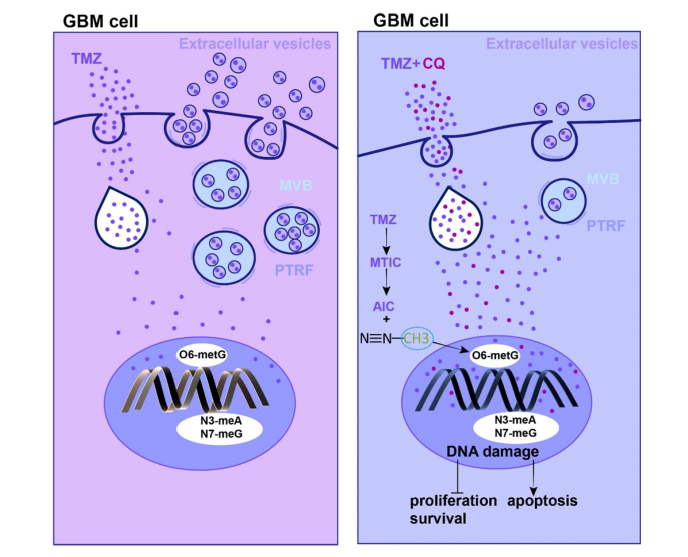
胶质母细胞瘤TMZ耐药性机制及TMZ联合CQ序贯治疗降低TMZ耐药性 参考文献:PTRF/Cavin-1 enhances chemo-resistance and promotes temozolomide efflux through extracellular vesicles in glioblastoma, Theranostics. 2022 May 16;12(9):4330-4347. doi: 10.7150/thno.71763.
外泌体资讯网 Theranostics | PTRF/cavin1通过细胞外囊泡释放促进胶母细胞瘤外排替莫唑胺和增加化学药物抗药性




