细胞外囊泡和外泌体通过运输蛋白质和RNA等大分子介导细胞间通讯。而想要识别外泌体内的货物分子,需要预先进行外泌体的分离才能进行。来自美国奥古斯塔大学的研究人报告了一种用于外泌体货物识别的原位标记方法,绕过了外泌体分离步骤。在该方法中,工程化的抗坏血酸过氧化物酶APEX的变体与外泌体货物蛋白(如CD63)融合,在细胞内囊泡或条件培养基中分泌出来的外泌体中特异性表达,诱导蛋白质的生物素化并激发信号,并通过蛋白质质谱证明氧化应激导致的蛋白质货物的积累。该研究发表于J Extracell Vesicles杂志上。
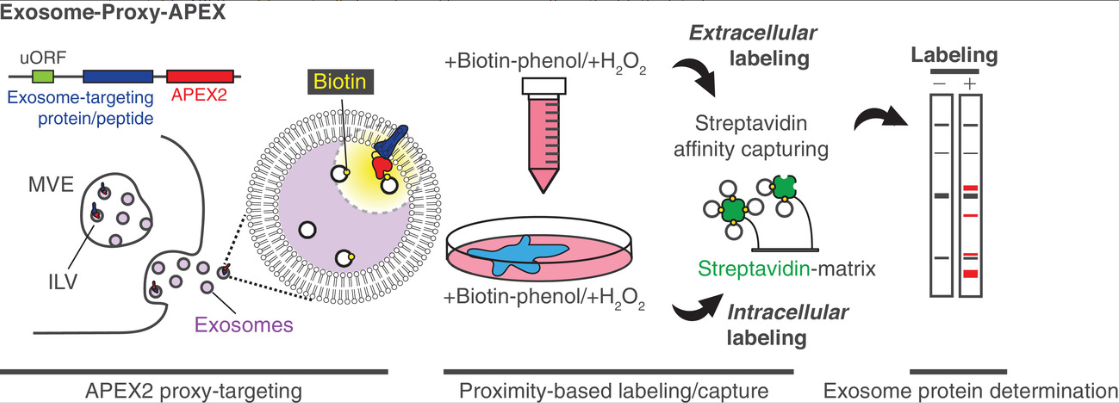
血液和尿液等生物体液携带多种细胞外囊泡,包括外泌体,这是一种直径40-150 nm的球形囊泡。目前的研究揭示了外泌体在各种正常和疾病过程中发挥的细胞间通讯作用,从机体功能和免疫反应到组织修复和肿瘤发展。作为货物包装在外泌体中,蛋白质和RNA被认为可以将供体细胞信息传递给受体细胞。不同货物分子组成造就了不同的外泌体介导的生物反应。因此,更好地理解外泌体的生物学作用需要对外泌体内容物进行精确检测。外泌体似乎是通过细胞中的囊泡运输来发展的。晚期内体成熟为多泡内体(MVE,也称为多泡体MVB)是外泌体生物发生的核心。在囊泡运输过程中,货物蛋白和RNA被装载到MVE 内的腔内囊泡(ILV) 中。当 MVE 膜与质膜融合时,ILV 将作为带有一组特定蛋白质和 RNA 的外泌体分泌到细胞外环境中。几种生化方法,如差速和密度梯度离心、尺寸排阻色谱和聚合物介导的沉淀已被用于分离外泌体。然而,生物流体的不同粘度、外泌体表面的粘附性和外泌体的可变大分子组成可能会阻碍我们制备具有一致质量的外泌体。通过这些方法制备外泌体通常需要较长的处理时间,并且还需要特殊设备。值得注意的是,与现有外泌体分离方法相关的这些困难也可能导致外泌体货物的识别变得复杂,也无法充分区分外泌体与其他类型的细胞外囊泡。在这项研究里,研究人员采用一种替代方法来识别外泌体货物分子。他们认为,在原位特异性地进行外泌体货物分子的基因工程的化学标记可以在ILV或分泌的外泌体中完成,并可以绕过外泌体分离步骤。随后将通过相容的亲和捕获来收获所得的化学修饰分子。最近开发的使用工程化的抗坏血酸过氧化物酶 APEX 的邻近依赖性蛋白质生物素化方法可以达到目的。 APEX 的催化活性在过氧化氢存在下将外源添加的生物素-苯酚(也称为生物素酪酰胺)转化为高反应性、不稳定的生物素-苯酚自由基,进而与附近的蛋白质混杂地结合。在表达与指导特定亚细胞定位的肽或蛋白质融合的APEX变体后,可以在短时间内诱导生物素化反应,通常为1-2分钟左右,然后淬灭,从而对亚细胞位置的蛋白质产生高度可信的快速信号反应。在APEX 生物素化后使用链霉亲和素基质进行高效、严格的亲和力捕获已证明其在定义几种亚细胞水平蛋白质组中的实用性。
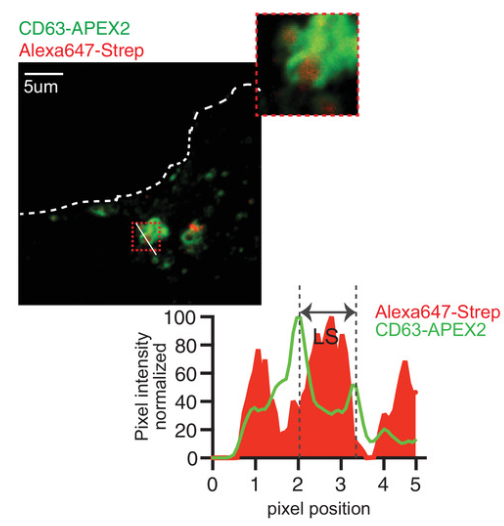
图:在 APEX生物素化诱导后表达CD63-APEX2的细胞的共聚焦免疫荧光显微照片。在生物素化诱导和淬灭后30分钟固定细胞,使生物素化蛋白质扩散。CD63-APEX2,绿色 (Alexa 488)。生物素化蛋白质,红色(Alexa 647-Strep)。因此,研究人员试图通过在外泌体生物发生囊泡运输中表达APEX变体,将其特异性递送至外泌体。最近的研究类似地设计了APEX或另一种混杂的生物素连接酶BirA,证明了细胞内细胞外囊泡相关蛋白的生物素化。因此,研究人员首先检查了APEX变体特异性定位到产生外泌体的ILV的能力,诱导在外泌体中释放的蛋白质的生物素化(细胞内标记)。然后,研究人员探讨了新建立的可靶向外泌体的APEX是否可以在无细胞条件下诱导邻近的蛋白质生物素化,特别是在条件培养基中存在的分泌外泌体中(细胞外标记)。结合细胞外标记和对分泌的外泌体中捕获的生物素化蛋白的质谱分析,研究人员进一步展示了氧化应激如何通过使用肾近端小管衍生的培养细胞模型改变外泌体货物蛋白的含量。参考文献:Ascorbate peroxidase-mediated in situ labelling of proteins in secreted exosomes. J Extracell Vesicles. 2022 Jun;11(6):e12239.
外泌体资讯网 JEV丨抗坏血酸过氧化物酶介导的外泌体蛋白质的原位标记




