10月份国内新出的细胞外囊泡/外泌体领域论文不完全统计有287篇。IF>10的有33篇;IF>15的有12篇;IF>20的有4篇。本期主要内容包括:活化STING通过细胞外囊泡转移可促进抗肿瘤免疫、外泌体lncRNA LINC01614与肺腺癌、肿瘤细胞EV介导抗PD-L1治疗的机制、糖尿病牙周组织的重塑、外泌体CircATG4B编码的新型蛋白质诱导结直肠癌的奥沙利铂耐药、干细胞EV改善炎症性骨溶解、从大肠杆菌中大量收集细胞外膜囊泡、基于CRISPR/Cas系统的外泌体检测等方面内容。内容十分丰富,不容错过。全部文献列表及部分文章原文可在外泌体之家论坛同名贴下下载。
1.中山大学康铁邦教授等:由RAB22A介导的非经典自噬触发的活化STING的细胞间转移可促进抗肿瘤免疫
Gao, Y., et al. (2022). "Intercellular transfer of activated STING triggered by RAB22A-mediated non-canonical autophagy promotes antitumor immunity."
Cell Res. IF= 46.297
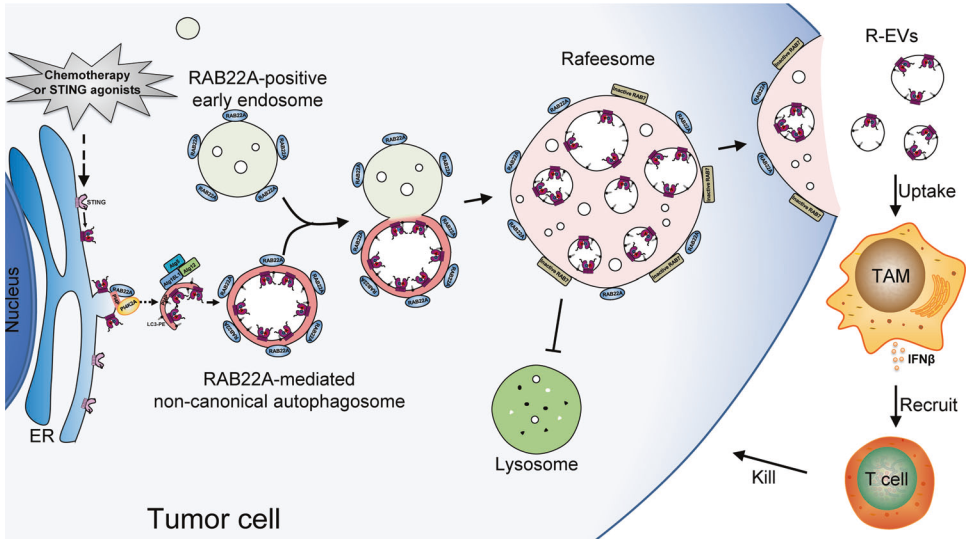
STING是一种内质网(ER)跨膜蛋白,在cGAMP刺激后介导先天免疫激活,并通过自噬降解。该研究报告激活的STING可以在细胞之间转移以促进抗肿瘤免疫,这是由RAB22A介导的非经典自噬触发的过程。从机制上讲,RAB22A与PI4K2A结合生成PI4P,该PI4P募集Atg12-Atg5-Atg16L1复合物,诱导ER衍生的RAB22A介导的非经典自噬体的形成,其中包装了由激动剂或放化疗激活的STING。这种RAB22A诱导的自噬体与RAB22A阳性的早期内体融合,产生一个新的细胞器,我们将其命名为Rafeesome(RAB22A介导的非经典自噬体与早期内体融合)。同时,RAB22A使RAB7失活以抑制Rafeesome与溶酶体的融合,从而使带有活化STING的自噬体的内囊泡分泌成为一种新型的细胞外囊泡,我们将其定义为R-EV(RAB22A诱导的细胞外囊泡)。活化的含有STING的R-EV诱导受体细胞向肿瘤微环境释放IFNβ,从而促进抗肿瘤免疫。一致地,RAB22A增强了STING激动剂diABZI在小鼠中的抗肿瘤作用,并且高水平的RAB22A预测接受放化疗的鼻咽癌患者的良好生存率。研究结果表明,Rafeesome调节活化STING的细胞间转移以触发和传播抗肿瘤免疫,并且源自ER的非经典自噬体的内囊泡以R-EV的形式分泌,为理解细胞器膜蛋白的细胞间通讯提供了新的视角。
2.【综述】浙江大学梁廷波教授等:胰腺癌个体化治疗——mRNA疫苗
Huang, X., et al. (2022). "Personalized pancreatic cancer therapy: from the perspective of mRNA vaccine."
Mil Med Res 9(1): 53. IF= 34.915
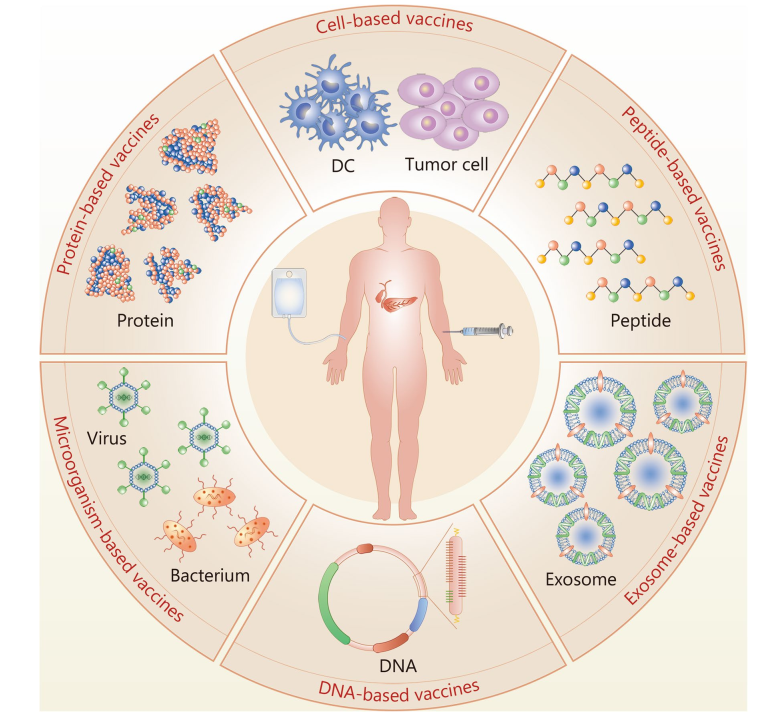
胰腺癌的特点是肿瘤间和肿瘤内异质性,特别是在基因改变和微环境方面。胰腺癌的常规治疗策略通常会遇到耐药性,这凸显了个性化精准治疗的必要性。癌症疫苗已成为胰腺癌治疗的有希望的替代品,因为它们具有多方面的优势,包括多靶向、最小的非特异性作用、宽的治疗窗口、低毒性和诱导持久的免疫记忆。已经开发出多种基于细胞、微生物、外泌体、蛋白质、肽或DNA的针对胰腺癌的常规疫苗;然而,它们的整体功效仍然不能令人满意。与这些疫苗模式相比,基于信使RNA(mRNA)的疫苗在个性化精准治疗方面提供了技术和概念上的进步,因此代表了胰腺癌新治疗方法的潜在前沿选择。这篇综述总结了胰腺癌疫苗的最新进展,强调了mRNA疫苗相对于其他常规疫苗的优势,并提出了设计和应用个性化mRNA疫苗来精准治疗胰腺癌的可行策略。
3.南京医科大学尹荣教授等:癌症相关成纤维细胞特异性lncRNA LINC01614增强肺腺癌中谷氨酰胺的摄取
Liu, T., et al. (2022). "Cancer-associated fibroblast-specific lncRNA LINC01614 enhances glutamine uptake in lung adenocarcinoma."
J Hematol Oncol 15(1): 141. IF= 23.168
背景:除了特征性的葡萄糖消耗外,最近的研究表明,癌细胞可能更喜欢“上瘾”来自肿瘤微环境(TME)的特定能量底物。然而,潜在的机制仍不清楚。方法:使用NJLCC队列、TCGA和CCLE数据集的RNA-seq数据筛选成纤维细胞特异性长非编码RNA。使用流式细胞仪分选、荧光原位杂交(FISH)和定量逆转录聚合酶链反应(RT-PCR)鉴定LINC01614在外泌体中的表达和包装。LINC01614在肺腺癌(LUAD)和CAF中的转移和功能作用使用4-硫氧嘧啶标记的RNA转移和获得和丧失功能的方法进行了研究。进行了RNA下拉、RNA免疫沉淀、双荧光素酶测定、基因表达微阵列和生物信息学分析,以研究所涉及的潜在机制。结果:证明LUAD中的癌症相关成纤维细胞(CAF)主要增强癌细胞的谷氨酰胺代谢。由CAF衍生的外泌体包装的CAF特异性长非编码RNALINC01614介导LUAD细胞中谷氨酰胺摄取的增强。在机制上,LINC01614直接与ANXA2和p65相互作用以促进NF-κB的激活,从而导致谷氨酰胺转运蛋白SLC38A2和SLC7A5的上调,并最终增强癌细胞的谷氨酰胺内流。相反,肿瘤衍生的促炎细胞因子上调CAF中的LINC01614,构成CAF和癌细胞之间的前馈循环。阻断外泌体传播的LINC01614可抑制体内谷氨酰胺成瘾和LUAD生长。临床上,CAFs中LINC01614的表达与LUAD患者的谷氨酰胺流入和预后不良有关。结论:该研究强调了靶向CAF特异性lncRNA抑制LUAD中谷氨酰胺利用和癌症进展的治疗潜力。
4.浙江大学蔡志坚团队:肿瘤细胞来源的胞外囊泡介导抗PD-L1治疗的机制
Chen, J., et al. (2022). "Tumor extracellular vesicles mediate anti-PD-L1 therapy resistance by decoying anti-PD-L1."
Cell Mol Immunol. IF= 22.096
该研究首次揭示了TEVs通过PD-L1“诱捕”并大量消耗抗PD-L1,导致抗PD-L1的治疗抵抗,从而为临床上有效提高抗PD-L1治疗的响应率提供有效的策略。
前期报道:https://www.exosomemed.com/12412.html
5.重庆医科大学宋锦璘教授等:二甲双胍的纳米载体辅助递送通过细胞胞吐作用介导的内质网稳态调节促进糖尿病牙周组织的重塑
Zhong, W., et al. (2022). "Nanocarrier-Assisted Delivery of Metformin Boosts Remodeling of Diabetic Periodontal Tissue via Cellular Exocytosis-Mediated Regulation of Endoplasmic Reticulum Homeostasis."
ACS Nano. IF=18.027
内质网(ER)功能障碍是糖尿病(DM)患者牙周组织修复能力受损的潜在原因。因此,恢复ER稳态对于糖尿病牙周组织的成功再生治疗至关重要。最近的研究表明,二甲双胍可以调节DM诱导的ER功能障碍,但其机制尚不清楚。该研究表明,在牙周膜干细胞(PDLSCs)中,由于胞吐作用介导的释放失败,高葡萄糖会提高细胞内miR-129-3p的水平,并随后通过下调跨膜和卷曲螺旋结构域1(TMCO1)来扰乱ER钙稳态,这是一种ERCa(2+)泄漏通道。这导致RUNX2通过泛素化依赖性途径降解,进而导致PDLSCs成骨受损。有趣的是,二甲双胍可以上调P2X7R介导的外泌体释放并减少细胞内miR-129-3p的积累,从而恢复ER稳态,从而挽救受损的PDLSC。为了进一步证明二甲双胍的体内作用,开发了一种用于在牙周组织中持续局部递送二甲双胍(Met@HALL)的纳米载体。研究结果表明,与对照组相比,具有增强的细胞相容性和促成骨活性的Met@HALL可以促进大鼠糖尿病牙周组织的重塑。总的来说,该研究结果揭示了二甲双胍在恢复细胞ER稳态中的机制,从而能够开发一种纳米载体介导的ER靶向策略来重塑糖尿病牙周组织。
6.【综述】江苏大学张徐教授等:癌症耐药性中的细胞外囊泡——作用、机制和意义
Yang, Q., et al. (2022). "Extracellular Vesicles in Cancer Drug Resistance: Roles, Mechanisms, and Implications."
Adv Sci (Weinh): e2201609.IF= 17.521
细胞外囊泡(EVs)是细胞衍生的纳米级囊泡,通过转运生物活性分子介导细胞间通讯,因此与各种生理和病理状况密切相关。EV有助于癌症进展的不同方面,例如癌症生长、血管生成、转移、免疫逃避和耐药性。EV通过转移影响药物流出的特定货物并调节与上皮-间质转化、自噬、代谢和癌症干性相关的信号通路来诱导癌细胞对化学疗法、放射疗法、靶向疗法、抗血管生成疗法和免疫疗法的抵抗力。此外,EVs调节肿瘤微环境(TME)中癌细胞和非癌细胞之间的相互作用以产生治疗抗性。在癌症患者的许多生物体液中都可以检测到EV,因此被认为是监测治疗反应和预测预后的新型生物标志物。此外,EV被认为是有前途的目标,并被设计为纳米载体,以提供药物以克服癌症治疗中的耐药性。在这篇综述中,总结了EV的生物学作用及其在癌症耐药性中的作用机制。还讨论了使用EV监测和克服癌症耐药性的临床前研究。
7.广东省人民医院李勇教授等:一种由外泌体CircATG4B编码的新型蛋白质通过促进自噬诱导结直肠癌的奥沙利铂耐药
Pan, Z., et al. (2022). "A Novel Protein Encoded by Exosomal CircATG4B Induces Oxaliplatin Resistance in Colorectal Cancer by Promoting Autophagy."
Adv Sci (Weinh): e2204513. IF= 17.521
奥沙利铂常用于结直肠癌(CRC)手术切除后的化疗方案。但获得性化疗耐药严重影响结直肠癌患者的疗效,其机制尚不清楚。该研究发现了一种环状RNA,circATG4B,它在CRC的奥沙利铂耐药中起重要作用。发现circATG4B表达在奥沙利铂耐药CRC细胞分泌的外泌体中增加。此外,结果表明circATG4B通过促进自噬诱导奥沙利铂耐药。进一步的体内和体外研究表明,circATG4B的作用归因于其编码新型蛋白质circATG4B-222aa的潜力。接下来,发现circATG4B-222aa作为诱饵与TMED10竞争性相互作用并阻止TMED10与ATG4B结合,从而导致自噬增加,随后诱导化学抗性。因此,本研究揭示了外泌体circATG4B参与降低了CRC细胞的化学敏感性,为CRC中奥沙利铂耐药的潜在治疗靶点提供了新的理论基础。
8.中山大学韦曦教授等:源自低氧预处理牙髓干细胞的小细胞外囊泡通过调节巨噬细胞极化和破骨细胞生成来改善炎症性骨溶解
Tian, J., et al. (2023). "Small extracellular vesicles derived from hypoxic preconditioned dental pulp stem cells ameliorate inflammatory osteolysis by modulating macrophage polarization and osteoclastogenesis."
Bioact Mater 22: 326-342. IF= 16.874
在炎症性或感染性溶骨过程中,广泛的巨噬细胞炎症反应和破骨细胞形成占主导地位。间充质干细胞(MSC)衍生的小细胞外囊泡(MSC-sEV)已被证明对骨缺损具有治疗作用。然而,培养的MSCs通常在体外暴露于常氧(21%O(2)),这与缺氧条件下体内的氧气浓度有很大不同。目前尚不清楚在缺氧条件下培养的牙髓干细胞(DPSCs)(Hypo-sEV)是否比在常氧条件下培养的(Nor-sEV)对脂多糖(LPS)诱导的炎症性骨溶解具有更好的治疗效果。抑制巨噬细胞炎症反应和破骨细胞生成。该研究表明缺氧显著诱导sEV从DPSC中释放。此外,与Nor-sEV相比,Hypo-sEV在促进M2巨噬细胞极化和抑制破骨细胞形成以减轻LPS诱导的炎症性颅骨骨丢失方面表现出显著提高的功效。从机制上讲,缺氧预处理显著改变了DPSC-sEV的miRNA谱。MiR-210-3p富含Hypo-sEV,可同时通过靶向NF-κB1p105诱导M2巨噬细胞生成和抑制破骨细胞生成,从而减弱骨质溶解。该研究表明,缺氧诱导的DPSC-sEV具有治疗炎症性或感染性骨溶解的潜力,并确定了miR-210-3p通过抑制NF-kB1表达同时阻碍破骨细胞生成和巨噬细胞炎症反应的新作用。
9.【综述】上海交通大学附属九院林开利教授等:细胞外囊泡在骨关节炎发病机制、诊断和治疗方面的突破
Liu, Z., et al. (2023). "Breakthrough of extracellular vesicles in pathogenesis, diagnosis and treatment of osteoarthritis."
Bioact Mater 22: 423-452. IF= 16.874
骨关节炎(OA)是一种高度流行的全关节疾病,会导致残疾和疼痛,并影响患者的生活质量。然而,目前缺乏有效的早期诊断和治疗。尽管干细胞可以促进软骨修复和治疗OA,但免疫排斥和致瘤性等问题仍然存在。细胞外囊泡(EVs)可以传递来自供体细胞的遗传信息并介导细胞间通讯,这被认为是干细胞的功能性旁分泌因子。越来越多的证据表明,EVs可能在OA的发病机制、诊断和治疗中发挥重要而复杂的作用。该研究通过影响炎症、新陈代谢和衰老来介绍EV在OA进展中的作用。接下来,作者讨论了来自血液、滑液和关节相关细胞的EV用于诊断。此外,概述了修饰和未修饰的EV及其与生物材料组合用于OA治疗的潜力。最后,我们讨论了EV在OA领域应用的不足,并提出了相关的前景和挑战。
10.中国科学院物理研究所陈佳宁研究员等:用于无创恶性肿瘤诊断的单囊泡红外纳米镜检查
Xue, M., et al. (2022). "Single-Vesicle Infrared Nanoscopy for Noninvasive Tumor Malignancy Diagnosis."
J Am Chem Soc. IF=16.383
分子表达和结构中的蛋白质异质性决定了肿瘤的发生,是诊断和治疗癌症的生物标志物。小细胞外囊泡(sEVs)是细胞释放的纳米级膜结合囊泡,可转移生物活性分子进行细胞间通讯,并在肿瘤进展和转移中发挥重要作用。因此,肿瘤来源的sEVs中的蛋白质异质性表明了恶性转化的程度,为癌症诊断和恶性肿瘤评估提供了一种非侵入性的生物标志物。我们采用近场红外(nano-FTIR)光谱来研究单个sEV中与恶性肿瘤相关的蛋白质异质性,并证明sEV蛋白异质性在评估肿瘤恶性肿瘤和转移方面的可区分性。研究发现sEVs的酰胺I/II吸附比随着肿瘤的恶性程度增加,sEV蛋白中α-螺旋+无规卷曲(α-螺旋和无规卷曲)的比例随着肿瘤的恶性程度而降低,而β-折叠的比例随着肿瘤的恶性程度而降低。β-折叠和β-转角随肿瘤恶性程度增加。来自乳腺癌患者原发性肿瘤组织的sEV的这些纳米FTIR光谱特征在评估肿瘤转移时显示出高灵敏度和特异性。本研究显示了纳米FTIR在单个sEV表征中的优势,并证明了sEV蛋白异质性在癌症诊断中的重要性。它提供了一种非侵入性的解决方案来阐明癌症的发展并促进潜在癌症生物标志物的开发。
11.复旦大学药学院张志文课题组:微泡启发的输氧纳米系统增强放射治疗介导的肿瘤基质调节和抗肿瘤免疫
Gong, X., et al. (2022). "Microvesicle-inspired oxygen-delivering nanosystem potentiates radiotherapy-mediated modulation of tumor stroma and antitumor immunity."
Biomaterials 290: 121855. IF= 15.304
放射治疗的疗效受到肿瘤中强烈缺氧、错综复杂的基质和抑制性免疫微环境的极大挑战。该研究合理设计了一种载有DiIC18(5)和卤夫酮(M-FDH)的微囊泡供氧多氟碳纳米系统,具有显著改善肿瘤氧合和瘤内分布、协同辐射破坏肿瘤基质和增强联合癌抗肿瘤免疫治疗的能力。M-FDH产生了10.98倍的肿瘤氧合增强,并导致辐射后活性氧(ROS)的有效产生。M-FDH+X射线治疗导致显著的DNA损伤,超过90%的癌症相关成纤维细胞(CAF)和细胞外基质的主要成分被消除,杀肿瘤CD3(+)CD8(+)T细胞显著增强,并彻底消除4T1肿瘤中的抑制性免疫细胞。M-FDH+X射线对抑制肿瘤生长的治疗益处在两种鼠肿瘤模型中得到证实。因此,这项研究提供了一种令人鼓舞的微泡启发策略,以靶向肿瘤中的癌细胞和CAF,并协同放射治疗以实现有效的癌症治疗。
12.苏州大学刘坚教授等:从大肠杆菌中高产、磁性收集细胞外膜囊泡
Shi, R., et al. (2022). "High-Yield, Magnetic Harvesting of Extracellular Outer-Membrane Vesicles from Escherichia coli."
Small: e2204350.IF= 15.153
细胞外外膜囊泡(OMV)因其高生物相容性和进入细胞的能力而作为药物纳米载体具有吸引力。然而,低产量阻碍了广泛使用。该研究描述了一种从大肠杆菌中磁性收获OMV的高产方法。为此,大肠杆菌在磁性氧化铁纳米颗粒(MNP)的存在下生长。大肠杆菌对MNPs的吸收很低,并且不会增加OMVs的分泌。MNPs的摄取可以通过MNPs的聚乙二醇化来增强。大肠杆菌在聚乙二醇化MNP存在下的生长增加了细菌MNP摄取和OMV分泌,同时伴随着与OMV分泌有关的基因的上调。含有MNPs的OMV的磁性收获率比超速离心法高60倍。在功能上,磁性收获的OMV和通过超速离心收获的OMV都以相似的数量被细菌吸收。独特的是,在施加的磁场中,具有MNPs的磁性收获的OMVs在感染性生物膜的整个深度上积累。在没有MNP的情况下通过超速离心收获的OMV仅在生物膜表面附近积聚。总之,MNP的PEG化对于它们在大肠杆菌中的摄取至关重要,并产生磁性OMV,从而实现高产磁性收获。此外,磁性OMV可以磁性靶向人体内的货物递送部位。
13.四川大学万美华等:大黄素通过抑制胰腺外泌体介导的肺泡巨噬细胞活化来减轻严重急性胰腺炎相关的急性肺损伤
Hu, Q., et al. (2022). "Emodin attenuates severe acute pancreatitis-associated acute lung injury by suppressing pancreatic exosome-mediated alveolar macrophage activation."
Acta Pharm Sin B 12(10): 3986-4003. IF= 14.903
14.中山大学附属第一医院张家兴等:细胞外囊泡介导的lncRNA IGFL2-AS1转移在肾细胞癌中赋予舒尼替尼耐药性
Pan, Y., et al. (2022). "Extracellular vesicle-mediated transfer of lncRNA IGFL2-AS1 confers sunitinib resistance in renal cell carcinoma."
Cancer Res. IF= 13.312
15.【综述】香港中文大学夏江教授等:细胞衍生的纳米囊泡介导的大脑药物递送——囊泡工程的原理和策略
Liang, Y., et al. (2022). "Cell-derived nanovesicle-mediated drug delivery to the brain: Principles and strategies for vesicle engineering."
Mol Ther. IF=12.910
16.中国药科大学韩超教授等:来自天然植物的无载体纳米平台可增强生物活性
Li, Z., et al. (2022). "Carrier-free nanoplatforms from natural plants for enhanced bioactivity."
J Adv Res. IF= 12.822
17.厦门大学杨朝勇教授等:流体纳米多孔微界面为肿瘤衍生的细胞外囊泡检测提供多尺度增强的亲和相互作用
Niu, Q., et al. (2022). "Fluid nanoporous microinterface enables multiscale-enhanced affinity interaction for tumor-derived extracellular vesicle detection."
Proc Natl Acad Sci U S A 119(44): e2213236119. IF= 12.779
18.中科院大连化学物理研究所陆瑶研究员等:神经元-巨噬细胞单细胞之间分泌组介导的相互作用图谱
Deng, J., et al. (2022). "Mapping secretome-mediated interaction between paired neuron-macrophage single cells."
Proc Natl Acad Sci U S A 119(44): e2200944119. IF= 12.779
19.陕西师范大学刘成辉教授等:基于CRISPR/Cas12a的多功能生物传感平台与目标保护转录策略相结合
Kang, X., et al. (2022). "A versatile CRISPR/Cas12a-based biosensing platform coupled with a target-protected transcription strategy."
Biosens Bioelectron 219: 114801. IF= 12.545
除了在基因编辑中的关键作用,CRISPR/Cas系统还为下一代生物传感技术的发展带来了新的信号放大机制。该研究通过将基于靶标保护的转录扩增策略与基于Cas12a的信号放大机制相结合,开发了一个通用的CRISPR/Cas12a传感平台,该平台允许对核酸和非核酸靶标进行灵敏检测。在该设计中,合理设计的转录模板序列能够避免核酸外切酶I(ExoI)降解,仅在存在靶标介导的结合事件(包括核酸杂交或基于蛋白质的亲和相互作用)的情况下。这种靶结合诱导的保护作用可以促进后续的转录扩增产生crRNA,并激活后续的Cas12a反式切割信号放大机制,产生靶剂量响应荧光信号。相反,如果目标不存在,无保护的转录模板将被ExoI完全消化,因此不会产生荧光反应。这一新策略很好地消除了T7聚合酶相关的非特异性转录背景,实现了对包括microRNA、蛋白质、外泌体在内的多种生物分子的灵敏检测,拓宽了CRISPR/Cas系统在生物分析和生物传感领域的应用场景。
20.川北医学院郭斌等:生物相容性工程红细胞作为等离子体传感器引发剂,用于在集成系统中对非小细胞肺癌衍生的外泌体miRNA 进行高灵敏度筛选
Fan, Y., et al. (2022). "Biocompatible engineered erythrocytes as plasmonic sensor initiators for high-sensitive screening of non-small cell lung cancer-derived exosomal miRNA in an integrated system."
Biosens Bioelectron 219: 114802. IF= 12.545
21.郑州大学吴拥军教授等:通用DNAzyme walkers触发的CRISPR-Cas12a/Cas13a生物测定法同步检测两种外泌体蛋白及其在癌症智能诊断中的应用
Ding, L., et al. (2022). "Universal DNAzyme walkers-triggered CRISPR-Cas12a/Cas13a bioassay for the synchronous detection of two exosomal proteins and its application in intelligent diagnosis of cancer."
Biosens Bioelectron 219: 114827. IF= 12.545
外泌体蛋白被认为是癌症的有希望的指标。该研究提出了一种新型DNAzyme walkers触发的CRISPR-Cas12a/Cas13a策略,用于同步测定外泌体蛋白:血清淀粉样蛋白A-1蛋白(SAA1)和凝血因子V(FV)。在该设计中,配对抗体用于识别靶标,从而确保特异性。DNAzyme walkers被用来将SAA1和FV的内容物转化为激活剂(P1和P2),一个靶点可以产生丰富的激活剂,从而实现信号的初步放大。此外,P1和P2可以激活CRISPR-Cas12a/Cas13a系统,进而反式切割报告基因,从而实现第二次扩增并产生两个荧光信号。该测定具有高度敏感性(SAA1的检测限低至30.00pg/mL,FV的检测限低至200.00pg/mL)、高度特异性和理想的准确度。更重要的是,它具有通用性,可用于检测外泌体中的非膜蛋白和膜蛋白。此外,该方法可成功应用于检测血浆外泌体中的SAA1和FV,以区分肺癌患者和健康个体。为了探索所开发方法在肿瘤诊断中的应用,开发了基于SAA1和FV表达的深度学习模型。该模型的准确率可以达到86.96%,证明了它具有很好的实际应用能力。因此,本研究不仅为外泌体蛋白的检测和癌症诊断提供了新的工具,而且为CRISPR-Cas系统提出了一种检测非核酸分析物的新策略。
22.北京中医药大学李晓骄阳教授团队:细胞外囊泡在纤维化肝脏疾病中的作用
Li, Y., et al. (2022). "Extracellular vesicles: catching the light of intercellular communication in fibrotic liver diseases."
Theranostics 12(16): 6955-6971. IF=11.6
前期报道:https://www.exosomemed.com/12559.html
23.【综述】西南医科大学附属医院王静、韩云炜团队:肿瘤微环境中的外泌体对巨噬细胞极化的影响
Wang, J., et al. (2022). "The role of exosomes in the tumour microenvironment on macrophage polarisation."
Biochim Biophys Acta Rev Cancer 1877(6): 188811. IF=11.414
前期报道:https://www.exosomemed.com/12469.html
全部文献列表及部分文章原文可在外泌体之家论坛同名贴下下载。(百度:外泌体之家;或网址:www.exosome.com.cn)
以上,10月份国内细胞外囊泡/外泌体领域研究进展的月总结整理。感谢大家关注!愿有所收获。下个月见!
外泌体资讯网 国内外泌体领域进展总结(2022年10月)