免疫疗法已经彻底改变了对非小细胞肺癌(NSCLC)患者的治疗。组织PD-L1(tPD-L1)的高表达目前是预测治疗反应的唯一批准的生物标志物。然而,即使是tPD-L1低(1-49%)和缺失(<1%)的患者也可能从免疫疗法中获益,但迄今为止,这些患者没有可靠的生物标志物可以预测治疗反应。来自德国明斯特大学的研究人员在肿瘤相关细胞外囊泡(EVs)上的研究填补了这一空白,大细胞外囊泡上的PD-L1在一些组织PD-L1低和阴性患者中呈现高表达,这些患者治疗反应较好,因此大细胞外囊泡PD-L1可以作为免疫治疗预测的生物标志物。相关内容以“PD-L1 on large extracellular vesicles is a predictive biomarker for therapy response in tissue PD-L1-low and -negative patients with non-small cell lung cancer”为题在线发表于3月7日的国际细胞外囊泡领域顶级学术期刊Journal of Extracellular Vesicles上。
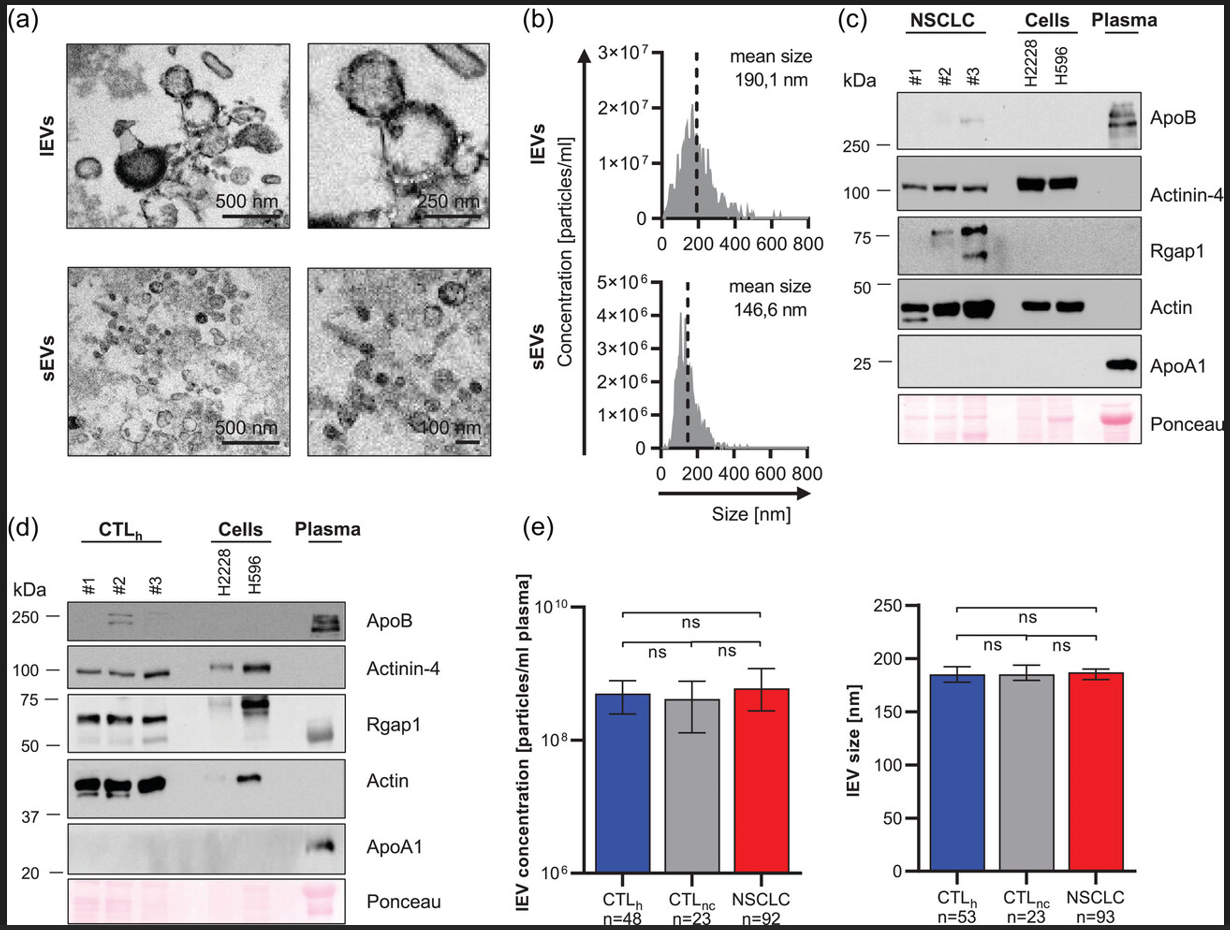
肺癌仍然是全球癌症相关死亡的主要原因。对于缺乏驱动突变的晚期非小细胞肺癌(NSCLC)患者,免疫检查点抑制剂(ICI)如抗程序性细胞死亡蛋白1(PD-1)和程序性细胞死亡配体1(PD-L1)的抗体已经彻底改变了尖端肺癌治疗方式,成为首选的有效疗法。免疫疗法与铂类化疗的联合治疗相比,可以改善腺癌和鳞状细胞癌的总体生存率,部分与肿瘤PD-L1表达无关。此外,与标准的铂类化疗相比,具有肿瘤细胞上高PD-L1表达(肿瘤比例评分,TPS)或肿瘤浸润免疫细胞上高PD-L1表达(组合阳性评分,CPS)的NSCLC患者从单一免疫疗法即可获益。此外,最近的研究表明,双重检查点抑制联合化疗与仅进行化疗相比,可以显著延长晚期NSCLC患者的总体生存期。这些试验强调了ICI前景光明的未来,现在已经普遍包含在肺癌标准治疗中。迄今为止,通过免疫组织化学确定的组织PD-L1(tPD-L1)表达是唯一获批的免疫治疗生物标志物。然而,tPD-L1的预测价值有限,到目前为止,没有一种生物标志物能够有效预测缺乏或低tPD-L1的患者对ICI的反应。与此一致,tPD-L1表达已被证明在原发性肿瘤和淋巴结转移之间存在差异,这就对基于组织活检的PD-L1评分的可靠性提出了质疑。来自血液等液体样本的生物标志物可以解决这个问题,因为它们可以进行全面的组织分析。此外,收集血液易于操作,可以快速和重复地进行,从而在进行放射学分期之前实现对治疗反应的实时监测。细胞外囊泡(EVs)是血液中有前途的液体活检生物标志物。这些小的膜颗粒由所有活细胞释放,通过携带蛋白质、脂质和核酸(如DNA、RNA)从分泌细胞到周围细胞来介导细胞间通信。迄今为止,已经描述了两种不同的EV种群:直径在50-150纳米之间的小型EVs(sEVs,以前称为“外泌体”)和直径在100-1000纳米之间的大型EVs(lEVs,以前称为“微囊泡”)。sEVs在细胞内通过内部囊泡膜内凹形成,而lEVs直接从质膜上出芽生成。许多研究已经证明,肿瘤来源的sEVs在建立有利的肿瘤微环境方面至关重要,从而为转移蔓延铺平了道路。然而,越来越多的研究将同样的肿瘤支持功能归因于lEVs。尽管sEVs和lEVs的载体有所不同,但已经证明肿瘤来源的lEVs会增加相邻癌细胞的增殖和侵袭。此外,sEVs和lEVs还涉及基质和免疫细胞的重编程,从而创建了一个有利的肿瘤微环境。由于肿瘤细胞向外周血释放的EVs数量较高,将EVs用作创新的癌症生物标志物在临床常规测试中具有很大的潜力。由于其较大的尺寸,lEVs易于用常见的诊断工具(如流式细胞术)进行分离和分析。在本研究中,研究人员探索了一系列肿瘤相关抗原在血浆来源的lEVs上的表达,以及它们作为NSCLC中ICI治疗的预后和预测生物标志物的潜力。研究人员利用NSCLC细胞系,确定了一组肿瘤相关抗原,这些抗原在lEVs上富集,相对于较小的EVs表达增加。携带这些抗原的lEVs水平在NSCLC患者(n = 108)的血浆中显著升高,并将它们与对照组(n = 77)区分开来。在测试的抗原中,研究人员专注于程序性细胞死亡配体1(PD-L1),这是免疫疗法的一个众所周知的直接靶点。在血浆lEVs中,PD-L1主要存在于一群CD45 / CD62P lEVs中,因此似乎与血小板源性囊泡有关。基线PD-L1 lEVs水平较高的患者显示出对免疫疗法有显著更好的反应和延长生存期。这在NSCLC患者亚组中尤为明显,因为这些患者tPD-L1表达低或缺失,但是lEVs上的PD-L1水平较高,因此将血浆中PD-L1阳性lEVs识别为免疫疗法的一种新的预测性和预后性标志物。参考文献:PD-L1 on large extracellular vesicles is a predictive biomarker for therapy response in tissue PD-L1-low and -negative patients with non-small cell lung cancer. J Extracell Vesicles. 2024 Mar;13(3):e12418.
外泌体资讯网 J Extracell Vesicles丨大细胞外囊泡上的PD-L1作为非小细胞肺癌患者免疫治疗反应的预测标志




