神经退行性疾病(Neurodegenerative diseases,NDDs),如阿尔茨海默病、帕金森病和肌萎缩侧索硬化症,是一类发病机制复杂的渐进性疾病。传统治疗方法因药物递送难题而面临重大挑战。最新研究将研究焦点转向外周系统,尤其是胞外囊泡(Extracellular vesicles,EVs),探讨它们如何穿过血脑屏障,从而在NDDs中发挥重要作用。
2024年4月12日,中南大学湘雅医院谢辉/王振兴/刘希希等在Journal of Nanobiotechnology期刊上发表了题为“Peripheral extracellular vesicles in neurodegeneration: pathogenic influencers and therapeutic vehicles”的综述文章(2024 Apr 12;22(1):170)。该综述详尽地梳理了外周来源EVs在调控大脑NDDs中的最新科研进展,包括来自骨骼、脂肪组织和肠道微生物的EVs。文章强调了外周EVs在NDDs进展中的双重角色:既可能促进病理发展,又可能延缓病理进程或作为治疗剂的载体。这些研究为开发新的NDDs防治策略提供了启示与方向。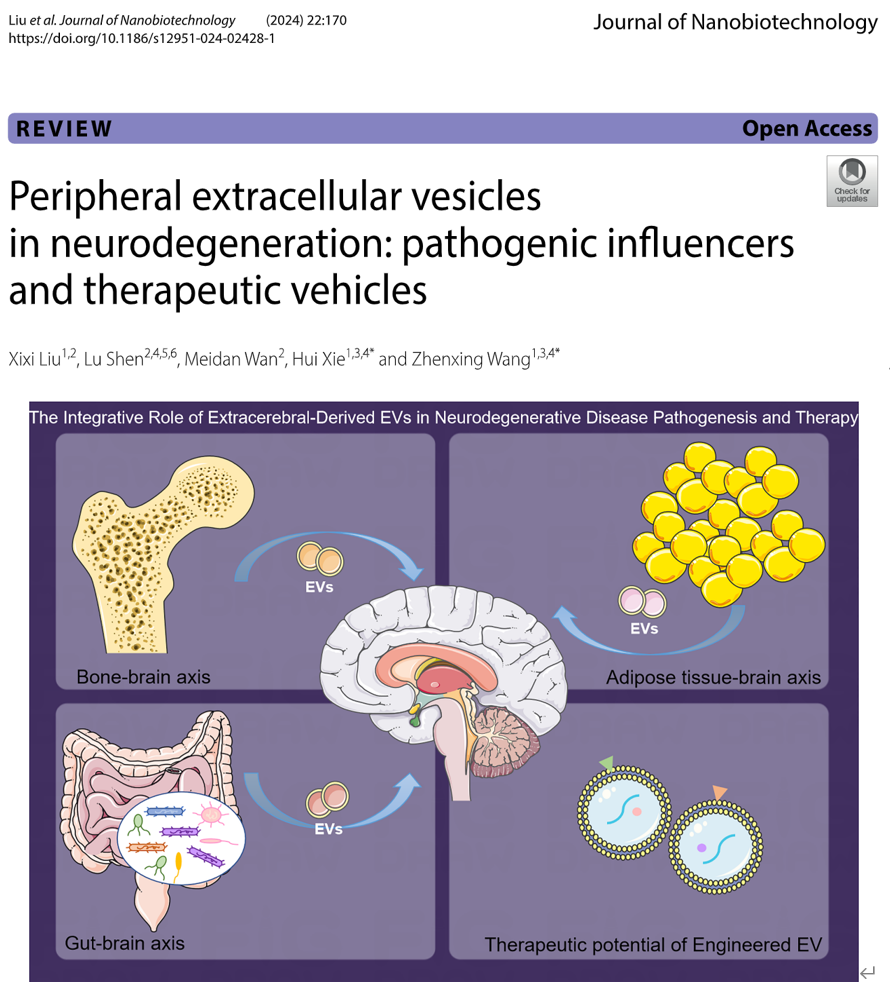
骨骼细胞来源的EVs与NDDs:在“骨-脑轴”复杂通信网络中,骨骼中的骨髓间充质干细胞、骨细胞及免疫细胞来源的EVs携带了多种蛋白质和miRNAs等功能性分子。这些分子通过调控神经细胞的存活、分化及功能,进而发挥维持神经系统稳态的作用。然而,随着增龄导致的骨骼细胞衰老或疾病导致的骨骼细胞凋亡,骨源性EVs所携带的神经保护分子的丰度显著下降,对神经系统的保护作用减弱。脂肪组织衍生的EVs与NDDs:在健康状态下,脂肪组织分泌的EVs富含多种有益的脂肪因子、抗炎因子和生长因子。这些因子协同作用,促进神经发生、增强突触可塑性,进而改善认知功能。然而,在肥胖等代谢紊乱状态下,脂肪组织产生富含促炎脂肪因子与有害的miRNAs或代谢产物的EVs,这些EVs干扰神经系统的正常功能。肠道微生物分泌的EVs与NDDs:衰老或某些疾病状态下,肠道菌群失衡,有益菌减少、有害菌增多。有益菌如乳杆菌产生的EVs具有神经保护作用,通过改善免疫应答、减轻炎症反应等方式缓解神经退行性疾病的病理过程。有害菌如铜绿假单胞菌释放的EVs富含有害成分,如脂多糖、肽聚糖与细菌毒素等。这些EVs可能穿越肠道和血脑屏障,进入中枢神经系统,进而触发免疫反应,导致神经炎症和神经毒性蛋白的积累,加剧神经退行性病变。外周来源EVs作为NDDs的潜在治疗载体:鉴于外周EVs能够跨越血脑屏障,并在NDDs的发展中发挥关键作用。通过调控外周EVs的产生、释放与运输,并优化其携带的治疗分子的种类与含量,有望实现对NDDs的有效干预。此外,利用基因编辑技术对外周EVs进行改造,增强其神经保护能力或降低其神经致病性,将为NDDs的防治带来新策略。尽管EVs具有强大的功能,其生物遗传学特性和分泌机制还有待深入解析,其临床应用仍面临诸多挑战。为推动EVs从实验室研究走向临床应用,需优选产生EVs的细胞并优化EVs制备方案,建立标准。未来,纳米技术、生物工程和分子生物学的融合将有利于建立基于EVs的靶向递送治疗方法。同时,组学技术和系统生物学的不断进步有望揭示外周EVs的分子特征,为其在NDDs治疗中的应用提供更深入的理解与支持。该综述不仅揭示了外周来源EVs在NDDs中的复杂调控作用,还为开发新的治疗策略提供了启示。未来,进一步研究通过调控外周EVs的功能或基于EVs设计出高效的药物输送系统,将助力NDDs的治疗。Peripheral extracellular vesicles in neurodegeneration: pathogenic influencers and therapeutic vehicles, J Nanobiotechnology. 2024 Apr 12;22(1):170. doi: 10.1186/s12951-024-02428-1.原文链接:https://doi.org/10.1186/s12951-024-02428-1外泌体资讯网 J Nanobiotechnol︱中南大学湘雅医院谢辉/王振兴/刘希希:外周来源胞外囊泡在神经退行性疾病中的调控作用与治疗潜力





