口腔粘膜下纤维化(OSF)是一种癌前病变,主要临床症状包括张口受限、吞咽困难等,部分患者甚至可发展为口腔癌,严重影响生活质量。然而,目前缺乏能够改善或逆转OSF病理状态的有效治疗手段。
中南大学湘雅口腔医院李昆团队长期从事脂肪干细胞及脂肪组织工程、口腔黏膜下纤维性变发病机制等相关研究,近期于Journal of nanobiotechnology(中科院1区,5年IF 10.6)杂志上发表了题为“Adipose-Derived Stem Cell Exosomes Attenuates Myofibroblast Transformation via Inhibiting Autophagy through TGF-β/Smad2 Axis in Oral Submucosal Fibrosis”的论文,主要介绍了脂肪干细胞外泌体可通过抑制TGF-β信号通路进而抑制自噬过程,调节肌成纤维细胞表型,在体内外有效逆转OSF病理状态,为OSF和纤维化相关疾病提供了治疗策略的新角度。中南大学湘雅口腔医学院李昆教授为论文的通讯作者,徐金浩、王钰静为文章的共同第一作者。研究工作得到了国家自然科学基金、湖南省自然科学基金等项目的支持。
该团队首次揭示了肌成纤维细胞中自噬与TGF-β的相互作用关系在OSF发生发展中的关键作用。在OSF中,激活TGF-β信号通路显著上调细胞自噬水平,TGF-β受体抑制剂治疗部分逆转这一过程;然而,仅自噬激活或抑制并不能改变TGF-β通路的状态,提出TGF-β在OSF中的肌成纤维细胞转化中起主导作用,自噬的变化可能是由于对TGF-β通路激活的级联反应。
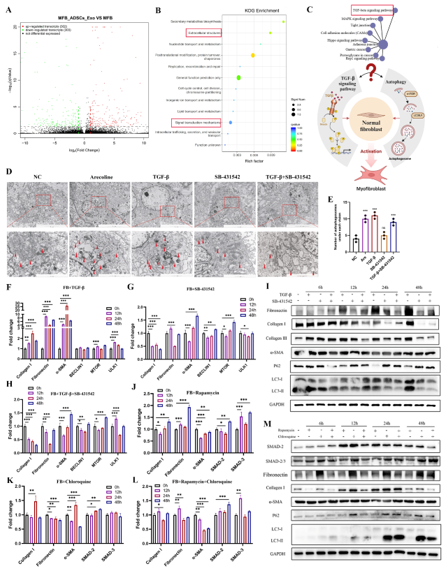
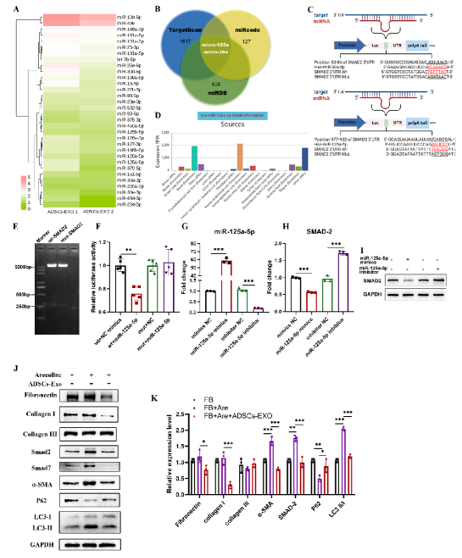
图1. OSF中TGF-β信号通路调节自噬,促进成纤维细胞向肌成纤维细胞表型分化分子层面,该团队对脂肪干细胞外泌体干预后的肌成纤维细胞进行转录组测序,揭示了差异基因与细胞外基质结构、信号转导相关;外泌体miRNA高通量测序、双荧光素酶报告基因等手段揭示了外泌体中的miR-125a-5p可与TGF-β信号通路下游因子Smad2结合,阻断信号通路级联反应,并抑制自噬过程,减少肌成纤维细胞的胶原合成。
图2.脂肪干细胞外泌体中miR-125a-5p可与Smad2结合,抑制肌成纤维细胞胶原合成进一步地,该团队构建小鼠OSF模型,证实脂肪干细胞外泌体局部注射显著减轻OSF小鼠的病理损伤,尤其是缓解黏膜下层的胶原沉积、血管闭塞及上皮萎缩。与体外细胞模型结果一致,外泌体治疗有效地降低了组织TGF-β和自噬水平,这些发现为基于外泌体的纤维化相关疾病的治疗策略开发提供了重要依据。

图3. 脂肪干细胞外泌体通过调节TGF-β及自噬过程有效缓解小鼠口腔黏膜下纤维性变。参考文献:Adipose-derived stem cell exosomes attenuates myofibroblast transformation via inhibiting autophagy through TGF-β/Smad2 axis in oral submucosal fibrosis.J Nanobiotechnology. 2024;22(1):780.
外泌体资讯网 J Nanobiotechnology|中南大学湘雅口腔医院李昆团队:脂肪干细胞外泌体治疗口腔黏膜下纤维性变